
- •Лекция 1 введение в биоорганическую химию
- •Введение
- •Классификация органических соединений
- •Номенклатура органических соединений
- •1.2 Классификация органических соединений
- •Алициклические углеводороды
- •Номенклатура органических соединений
- •Общая схема составления названий
- •Ноос –сн2 – с – сн2 - соон
1.2 Классификация органических соединений
Для описания структуры молекул органических соединений используют различные химические формулы: эмпирические, молекулярные и структурные. Наиболее полную информацию о строении молекулы содержит структурная (графическая) формула, которая отражает природу атомов, входящих в состав молекулы, их число и последовательность связывания, а также тип связей между атомами.
Н Н Н Н
Н – С - С – С – С – Н
Н Н Н Н
Обычно на практике наиболее часто употребляют полуструктурные формулы, т.е. часть связей не изображаются, а приводятся только те связи, которые необходимы для однозначного описания строения
молекулы:
С Н3
– СН2 – СН2 –СН3
СН3 – СН – СН2 –СН3
Н3
– СН2 – СН2 –СН3
СН3 – СН – СН2 –СН3
|
NH2
 Каждый период истории развития
органической химии отмечен попытками
химиков каким-то образом привести
разнообразные химические соединения
в единую систему (теория типов, радикалов
и т. д.)
Каждый период истории развития
органической химии отмечен попытками
химиков каким-то образом привести
разнообразные химические соединения
в единую систему (теория типов, радикалов
и т. д.)
В основе современной классификации органических соединений лежит теория строения А.М. Бутлерова, согласно которой каждое индивидуальное вещество можно описать только одной химической формулой.
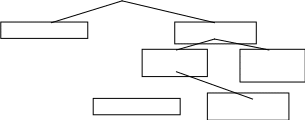 ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ

Ациклические Циклические
Карбоцик- гетероцик-
 лические
лические
лические
лические
алициклические ароматические
В свою очередь, схема классификации ациклических соединений имеет вид:
А





 лкенины
Алкены Алкины Алкадиены
лкенины
Алкены Алкины Алкадиены
А



 лкадиены
лкадиены


 Изолиро- Сопря-
Изолиро- Сопря-
Ванные женные

 Кумули-
Кумули-
Непредельные рованные
П олиены
углеводороды
олиены
углеводороды

Ациклические
углеводороды

Предельные
Углеводороды
Предельные или насыщенные углеводороды (алканы, парафины) содержат только простые углерод-углеродные связи, все остальные валентности атомов углерода в их молекулах “израсходованы” на связи с водородными атомами. Общая формула СnН2n+2. Родоначальник ряда – метан СН4
Непредельные или ненасыщенные углеводороды имеют кратные (двойные или тройные) углерод - углеродные связи.
Алкены (олефины, этиленовые углеводороды) содержат одну двойную связь. Общая формула СnН2n.
Родоначальник ряда – этилен СН2 = СН2
Алкины (ацетиленовые углеводороды) имеют тройную связь. Общая формула СnН2n-2.
Родоначальник ряда – ацетилен СН≡СН
Алкадиены (диолефины, диеновые углеводороды) содержат две двойные связи. Общая формула такая же как у алкинов СnН2n-2, т.е. алкины и алкадиены изомерны друг другу. Различают:
Алкадиены с изолированными двойными связями,например
Н2 С = СН – СН2 – СН = СН2 пентадиен-1,4
Алкадиены с сопряженными двойными связями,например
Н2 С = СН – СН = СН - СН3 пентадиен-1,3
Алкадиены с кумулированными двойными связями,например
Н2 С = С = СН - СН2 - СН3 пентадиен-1,2
Алкенины – соединения с одной двойной и одной тройной связями
Н2 С = СН – С ≡ СН бутен-1-ин-3
Алкадиины – соединения с двумя тройными связями
НС ≡ С – С ≡ СН бутадиин-1,3
Полиены (полиолефины) – соединения со многими двойными связями
Н2 С = СН - СН = СН - СН = СН – СН3 гептатриен-1,3,5
