
- •Kлассификация аминокислот
- •Аминокислоты
- •11) Hooc - ch2 - ch - cooh
- •12) Hooc - ch2 - ch2 - ch - cooh
- •Диаминомонокарбоновые аминокислоты (основные)
- •Iy. Ароматические аминокислоты
- •Y .Гетероциклические аминокислоты
- •Стереоизомерия α-аминокислот
- •15.2. Биосинтетические пути образования аминокислот
- •15.3. Химические свойства
Стереоизомерия α-аминокислот
Все α-аминокислоты, за исключением глицина, имеют асимметрический атом углерода и существуют в виде энантиомеров, относящихся к D- и L-рядам. В белках животных организмов представлены L-аминокислоты, в белках микроорганизмов встречаются и аминокислоты D-ряда. D-аминокислоты животным организмом не усваиваются.
L -аланин
L-треонин L-изолейцин
-аланин
L-треонин L-изолейцин
Три аминокислоты имеют два центра хиральностти: треонин, изолейцин, 4-гидроксипролин.
15.2. Биосинтетические пути образования аминокислот
Биосинтез α-аминокислот осуществляется из α-кетокислот -
продуктов метаболизма углеводов. Возможны два пути превращения кетокислот в аминокислоты
Восстановительное аминирование с участием кофермента НАД-Н
О NH2
║ НАД-Н │
НООС – СН2 – СН2 – С – СООН → НООС – СН2 – СН2 – СH – СООН
α-кетоглутаровая кислота глутаминовая кислота
Трансаминирование (переаминирование), источником группы NH2 для кетокислот является другая аминокислота. Эта реакция протекает при участии кофермента пиридоксальфосфата
R–CH–COOH + HOOC-CH2-C-COOH→ R–C–COOH + HOOC-CH2-CH-COOH
│ ║ ║ │
NH2 О O NH2
Щавелевоуксусная кислота Аспарагиновая
Кислота
15.3. Химические свойства
Аминокислоты являются амфотерными органическими соединениями, поэтому в растворах существуют в виде биполярных ионов
Н3+N – СН – СОО-
R
Аминокислотам присущи все свойства как карбоновых кислот, так и аминов.
Реакции карбоксильной группы - образование функциональных производных кислот (сложных эфиров, амидов, солей,галогенангидридов).
Реакции аминогруппы - образование солей с сильными кислотами, образование N-ацилированных производных.
Кроме того для аминокислот характерен целый ряд специфических реакций, обусловленных наличием в их структуре COOH- и NH2- групп у одного и того же атома углерода. Рассмотрим реакции, протекающие в организме. Все эти реакции - ферментативные, хотя некоторые из них могут быть осуществлены in vitro.
Декарбоксилирование in vivo приводит к образованию биогенных аминов.
HOOC-CH2- CH2-CH-COOH → HOOC-CH2- CH2-CH2-NH2
ГЛУ │ - CO2 γ-аминомасляная кислота (ГАМК)
NH2 природный транквилизатор
В результате реакции декарбоксилирования образуются биогенные амины (триптамин, гистамин, коламин, дофамин, серотонин).
Декарбоксилирование in vitro протекает аналогично
t0C, Ва(ОН)2
HOOC-CH2- CH2-CH-COOH → HOOC-CH2- CH2-CH2-NH2
│ - ВаCO3
NH2
Дезаминирование (удаление NH2-группы ) бывает неокислительным (без участия О2).
Н СООН
Аспартаза \ /
HOOC-CH2-CH-COOH → C ═ C
│ - NH3 / \
NH2 НООС Н
АСП Фумаровая кислота
Окислительное дезаминирование протекает при участии кофермента НАД+
+ НАД+ Н2О
R–CH–COOH → R-C-COOH → R–C–COOH
│ - НАДН ║ - NH3 ║
NH2 NH O
Дезаминирование in vitro
CH3 – CH - COOH + HNO2 → CH3 – CH - COOH + N2 + H2O
│ │
NH2 OH
Применяется для количественного определения аминокислот (метод Ван-Слайка)
3) В организме происходит реакция гидроксилирования некоторых аминокислот, которая не имеет аналогии в химии in vitro например гидроксилирование незаменимой аминокислоты фенилаланина в тирозин.
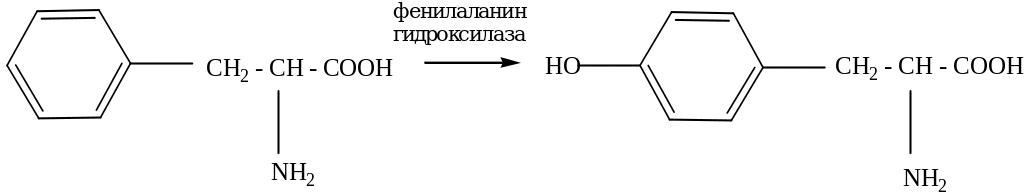
ФЕН ТИР
Отсутствие или недостаток в организме фермента катализирующего эту реакцию приводит к тяжелому заболеванию - фенилкетонурия.
