- •14. Цепные реакции горения. Температура воспламенения. Пламя и его структура.
- •16. Нормальная скорость распространения пламени в ламинарном потоке горючей смеси.
- •17. Структура турбулентного пламени и скорость его распространения.
- •18. Инициирование горения зажиганием.
- •19. Основные характеристики пожаро- и взрывоопасности веществ и материалов.
- •22. Особенности горения газообразных веществ.
- •23.Горение жидких веществ и его особенности.
- •24. Горение твёрдых веществ и его особенности.
- •26. Ударные волны в газах. Взрыв.
- •Законы ударного сжатия.
- •28. Определение энергии взрывчатой системы. Тротиловый эквивалент взрыва.
- •30. Концепция теории горения и взрыва.
1.Предмет ТГВ,ее место и роль в по-дготовке специа- листов. ТГВ- основывается на фундоментальных сведениях из физикохимии,газодинамики, теории тепломассообмена,термодинамики. Роль ТГВ определяется широким использованием процессов горения в энергетике, технике и технологии.ТГВ дает инструментарий для разработки методов и средств предотвращений пожаров в техногенных системах. Пожар-неуправляемое стихийное развитие процессов горения, сопровождающ. материальными потерями и жертвами. Горение –сложный процесс физико-хим-х превращений горючего в-ва в среде окислителя, сопровожд. выделением теплоты и свечением.Взрыв- частный случай процесса горения.Характеризуется высокой υ распространения пламени,t до 1,5 и 3ºС и р=от 1-2 МПа и более.Норм. υ распространения пламени-0,1-1м/с.Взрывное горение(дефлаграционное)-большая скорость,порядка 10-100м/с.Детанационное горение(υ от 1000-5000м/с)-сопровожд.образованием фронта детанационной волны(ударной),в кот резко увеливены и t и р.Процессы горения (управляемое) реализуются в огне-технических системах.(топки,камеры сгорания).Процессы управляемого взрыва реализуются в строительстве ( при дроблении скальных пород, при выработке штольн,получении новых материалов,обработке Ме.) Процессы взрыва применяются в военном деле.
2. Процесс горения как сложный физико-химический процесс. Система, окр среда, компонент.Горючая система. Ее компоненты. Гетерогенная и гомогенная. Горение –сложный процесс физико-хим-х превращений горючего в-ва в среде окислителя, сопровожд. выделением теплоты и свечением.Взрывное горение(дефлаграционное)-большая скорость,порядка 10-100м/с.Детанационное горение(υ от 1000-5000м/с)-сопровожд.образованием фронта детанационной волны(ударной),в кот резко увеливены и t и р.Процессы горения (управляемое) реализуются в огне-технических системах.(топки,камеры сгорания).Горючая система-совокупность материальных тел,нах-ся м/д собой в энергетическом взаимодействии. Гор. система:1.горючие в-ва.2.источники зажигания.3. продукты горения.4.окислители.5.замедлители реакции(флегматизаторы замедлители).Окислители: О2,воздух,F,Cl,S.Флегматизаторы:N,CO2,инертные газы(гелий) Продукты горения: СО2,водяной пар, окислы серы, при высокой t горения-NO2,CO.Горючие системы м.б открытыми и закрытыми,одно и многокомпонентными,одно и многофазными,гомогенными,гетерогенными,конденсированными.Открытыми назыв системы ч/з границы кот. Может проникать в-ва(газонефтепроводы)Закрытые –характериз-ся отсутствием системы (газовые баллоны, емкости хранения газов)Гомогенные- в кот. Одинкаовые физико-хим-е св-ва в различных частях.Гетерогенные- с разнородными физико-хим-ми cв-вами(окислитель+тв. Горючее в-во,ок-ль+жидкое гор.в-во)Гомогенная-часть гетерогенной системы назыв фазой.Фазы разделяются видимыми плоскостями.Конденсированные-газожидкостные системы.Тела,нах-ся в не границы системы,но могут оказывать на него воздействие относятся к окр среде. Горючая система включ источники зажигания-открытое пламя,спички, электрические разрядники.
3.Состав и основные св-ва гор. в-в.Низшая и высшая теплота сгорания тв,жидких и газооб-х веществ. Состав гор вв:различные компоненты;O2,H2,Sл,C,N,W,A.Состав газообразных гор. в-в: СО, H2S,углеводороды,водяной пар,О2,СО2. Углерод-в ископаемых углях его содержится от 50 до 95%от гор массы. Содерж углерода возрастает с геологическим возрастанием топлива.Qс=34000кДж/кг-теплота сгорания. Водород-с геологическим возрастом содерж Н снижаетсяQн=278000кДж/кг.Наиб содерж Н в природных газах(до 25% по объему на сухой объем).Наим содерж.-в антроцитах.(Н менее 4%).Летучая Сера Qs=9300кДж/кг-входит в состав медного и железного колчедана.Сульфидная сера не участвует в горении, а переходит в золу.Состав гор в-в м.б. задан на гор массу,сухую массу,рабочую,аналитическую.Основные харак-ки гор в-в:теплота сгорания(теплотворная способность),выход летучих в-в ,влажность,зольность. Теплота сгорания д/тв и жидких в-в задается на рабочую массу,у газообразных на сухую массу.Под теплотой сгорания поним. Теплота ,котвыделяется при полном сгорании единицы кол-ва в-ва. В высшую: QвысшееР=QнизшееР+Qпарообразов.QвысшееР= QнизшееР+rо/1000*(9Нр+Wр), rо-удельная теплота парообразования при нормальном параметрическом давлении.Q сгор.низшееР= QвысшееР- rо/100*(9Нр+Wр)низшую опред 2-мя способами:экспериментально и расчетным путем.Экспериментально-в спец-х колориметрических установках-бомбы.Расчетный основан на стехиометрических реакциях окисления горючих компонентов.
4. Материальный баланс горения, теоретически необходимое количество воздуха, коэффициент избытка воздуха.
Матер-ый баланс горения – это расчеты кол-в в-ва принимающих участие в процессе горения на основании з-на сохранения масс. Мг+Мок=Мпс
Горючее сост-щее топливо вступаеют в опред-ых колич-ных отношениях наз-ых стехеометрическими.
V020=1,866Ср/100+0,7Sр/100+5,55Hр/100-Qр/100ρO2 [м3/кг]
Ср,Нр,Ор,Sр,– массовое сод-ие С,Н,О,S, в топливе [%]; ρO2 [кг/ м3]
В воздухе сод-ся 21% O2
V0=V020/0,21=0,0889(Ср+0,375Sр)*
*0,265Hр-0,0333Ор
L0=0,115(Ср+0,375Sр)+0,342Hр-0,0431Ор [кг/кг]
V0- теорет-ое необход-ое кол-во кубомотра воздуха для полного сгорания воздуха;
L0- теорет-ое необход-ое кол-во кубометров воздуха до полного сгорания одного кг топлива.
Коэфф. избытка воздуха – это отношение кол-ва воздуха действительно поступ-ий в топку, к теоретич. необходимому: α = Vg/V0
6. расчет состава газа
Состав газообразного топлива.
СО+ Н2+ СН4+СnHm+Н2S+О2+N2+CO2=100 где газы взяты в % при норм.усл.(t=0,P=101325 Па)
Рабочий состав- состав который поступает в топку (%)
CP+HP+SP+OP+NP+AP+WP=100
Сухая масса – рабочий состав без влаги W.
CC+HC+SC+OC+NC+AC=100
Горючая масса- сухая масса без золы А.
CГ+HГ+SГ+OГ+NГ=100
По элементарному составу орг. топлива главным образом содержат С. Но есть использованиебороводородного топлива в ракетной промышленности.
В дереве, торфе - 50% С, в угле - 75% С, в антроцитах - 75% С.
При полном сжигании С выделяется тепло в количестве Qс=33600 (кДж/кг)
Второй важный элемент – Н. В древесине – 6-6,5%, в нефти – 5%, в каменном угле – 4-5,5%.
Тепловая ценность Н в 4 раза > С, Qнв=141500 (кДж/кг)- с учетом конденсации, QН2Н=11900 (кДж/кг). Теплотворная способность Н – высшая.
Третий компонент – S. Нежелательный горючий элемент, бывает органическая-S0, и колчеданная-Sk (Fe+Cu+S). Qs=9000 (кДж/кг).
Сера нежелательна тем, что при низкой ее энергетической характеристики, продукты ее сгорания вредят ОС и машинным механизмам. Поэтому топливо очищают от серы.
Кислород и азот также нежелательные элементы топлива. Кислород связующая часть горючих элементов, снижает энергетические характеристики. Азот в топливе приводит к образованию высокотоксичных оксидов. Азот м/т находится в виде NO, NO2, N2O и т.д. Но самый опасный NO и содержание его в выхлопных газах строго регламинтируется. ↑ Содержание N в топливе ведет к сильному ↑ оксидов азота в выхлопных газах. Кислород и азот вместе называются балластом топлива. В жидких топливах содержание балласта 0.5- 1.5%, в тв. топливах гораздо больше.
Зола – смесь минеральных веществ, которое остается после сгорания горючей части топлива. Содержание золы обосновано дается на сухую массу.
Газообразное топливо – механическая смесь горючих и негорючих газов.
Гор. часть – СО, Н2, СН4, СnНm, H2S; Негор. часть – N, CO2.
14. Цепные реакции горения. Температура воспламенения. Пламя и его структура.
Под цепным воспламенением понимается переход от медленного стационарного протекания цепной химической реакции к протеканию её с нарастающей во времени скоростью.
Существование цепных реакций обусловлено образованием активных центров реакций, в качестве которых выступают атомарные: кислород, водород, ОН, Сl.
Цепные реакции:
1) неразветвляющиеся (взаимодействие Cl2 и Н2)
2)
разветвляющиеся (взаимодействие Н2
и
О2
при
 и
низком давлении)
и
низком давлении)
Неразветвляющиеся: Разветвляющиеся:
1.
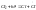 1.
1.

2.
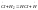 2.
2.
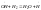
3.
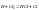 3.
3.
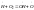
4.
обрыв
цепи 4.
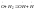 ветвление
ветвление
Температура воспламенения – min темп-ра горючей системы, при кот-й компоненты этой системы вступают в реакцию взаимодействия с образованием пламени.
Темп-ра воспл-я не явл-ся физико-химической постоянной, а зависит от рода горючего окислителя, давления и концентрации.
16. Нормальная скорость распространения пламени в ламинарном потоке горючей смеси.
Экспериментально
установлено, что скорость Uн
зависит от рода горючего и окислителя,
концентрации, темп-ры, давления, наличия
инертных веществ. В ламинарном течении
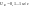 .
.
Скорость распространения пламени – ск-ть перемещения фронта горения относительно горючей смеси. (Фронт пламени имеет толщину, а сама поверхность фронта пламени является искривлённой).
Нормальная ск-ть распр-я пламени – понятие, соответствующее ламинарному движению горючей смеси и кинетическому горению.

Если оно меньше 2300, то режим – ламинарный.
Вектор
нормальной скорости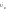 перпендикулярен поверхности фронта.
перпендикулярен поверхности фронта.
Количество теплоты для нагрева на 1 м2 поверхности фронта пламени:
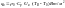
Ср – удельная теплоёмкость при Р = const
17. Структура турбулентного пламени и скорость его распространения.
Механизм распространения турб-го пламени в значительной степени определяется самим механизмом турбулентности.

Где
W
– актуальная скорость;
 -
осреднённая ск-ть;
-
осреднённая ск-ть;
 -
пульсационная ск-ть.
-
пульсационная ск-ть.
Степень
турбулентности:
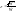
В
обычных турб-х потоках
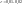 а, в сильно турбулезированных потоках
(камеры сгорания)
а, в сильно турбулезированных потоках
(камеры сгорания)
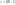 .
.
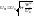
Скорость турб-го пламени зависит от турб-х характеристик потока и опр-ся 3 составляющими:
1) нормальная ск-ть распр-я пламени, которая в турб. потоке имеет теже значения, что и в ламинарном
2) степень турб-ти основного газо-воздушного потока и длина пути перемешивания
3) турбулентными пульсациями, вызванными автоколебаниями пламени
18. Инициирование горения зажиганием.
При нагревании объема смеси до достижения тем-ры восплам-я или самовосплам-я возможно придудит-е зажигаение смеси за счет локального ведел-я теплоты в малом объеме смеси.
Источники: - открытое пламя факела Тт=10000 К
Сущ-ют 2-е теор. Электро-искрового разряда: 1)ионная теория 2)тепловая теор. По ионной теор. актив-ми центрами реак-ии горения явл-ся ионы, свободные атомы и радикалы. По исслед-м ион-е зажиг. имеет место при низких давл-ях: Р=5-10 кПа
Тепловая теор. (разраб-та Зельдовичем) – при электро-искровом разряде выдел-ся теплота зажиг-я в локальном объеме гозовоздуш. смеси с хар-ым радиусом τ ~δ зажиган (толщина)
Ур-е теплового баланса можно записать:
Qзажиг=const*ρ0*Cp(Тг-Т0)δ3зажиг
Нормал. скорость распр-я пламени:
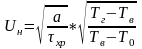
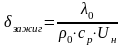
Процесс инициирования горения: самовоспламенение и вынужденное зажигание.
Под вынужд. воспламен. понимают случай, когда основн. масса горючей смеси остается холодной, а нагревание производ-ся в одном небольшом участке среды. Это осущ-ся введением в среду пламени, электрич. искры, нагретого тела.В данном случае возникнов. воспламенения также от Т, Р, [ ], энергии искры, Т и размера зажиг. тела.
Для того, чтобы нач-сь горение газовой смеси необходимо создать опр. нач. усл -воспламенить или зажечь смесь. М/ду воспламенением и взрывом нет принцип. физ. разницы ( чисто внешнее восприятие). На практике применяют 2 способа воспламенения:1) воспламеняемая смесь целиком подогревается до такого сост-я, когда она сам-но восплам-ся во всем V одновременно;2)холод. смесь зажигается в отдельной точке V и далее волна горения распр-ся на весь V;
В зависимости от [ ], энергии искры, Т и т.д. имеется верхний и нижний концентрац. предел воспламенения.