- •23. Собственный механический и магнитный моменты электрона.
- •24 Полный механический и магнитный моменты электрона. Принцип Паули
- •25. Распределение электронов в атоме по состояниям. Таблица Менделеева.
- •7. Давление света.
- •8. Гипотеза де Броиля.Волновой пакет частиц.
- •11. Операторы.
- •12 Собственные волновые функции и собственные значения физических величин. Собственные волновые функции оператора компоненты импульса.
- •15 Уравнение Шредингера для свободной частицы.
- •Частица в одномерной потенциальной яме.
- •20. Линейный гармонический квантовый осциллятор
- •21. Классическая модель атома водорода
- •22. Уравнение Шредингера для водорода. Квантовые числа
- •43.Деление ядер
- •44.Плазма
- •9.Соотношение неопределенностей Гейзенберга.
- •10.Опыт Дэвиссона и Джермера. Смысл волн де Бройля
- •4.Гипотеза Планка. Вывод формулы Планка.
- •5.Внешний фотоэффект.
- •6.Эффект Комптона.
- •34. Эффективная масса электрона
- •35. Полупроводники. Собственная и примесная проводимость.
- •36. Полупроводниковый диод.
- •37. Эффект Зеебека. Эффект Пельтье.
- •38. Конт разн потенц Контакт металл-металл.
- •39. Атомное ядро и его характеристики.
- •40. Ядерные силы и их свойства.
- •41. Радиоактивность. Альфа-распад. Бета-распад.
- •42.Закон радиоактивного распада.
- •26 Механический и магнитный моменты атома. Ls-связь.
- •27 Понятия об энергетических уровнях молекул.
- •28.Рентгеновские спектры. Закон Мозли.
- •29. Принцип тождества микрочастиц
- •30. Электронный газ в одномерном случае. Энергия Ферми.
- •31. Распределение Ферми-Дирака
- •32. Распределение Бозе-Эйнштейна
- •33. Энергетические зоны кристалла
- •45. Термоядерный синтез
- •46. Цепная реакция
- •Особенности теплового излучения, его характеристики.
- •2 Законы Кирхгофа, Стефана-Больцмана, Вина.
- •3. Тепловое излучение. Формула Релея-Джинса.
- •17 Решение уравнение Шредингера для низкого потенциального барьера.
- •18 Решение уравнение Шредингера для высокого потенциального барьера.
- •19)Туннельный эффект
- •13. Принцип причинности. Общее уравнение Шрёдингера.
- •14.Уравнение Шредингера для стационарных состояний
23. Собственный механический и магнитный моменты электрона.
Момент
импульса электрона, движущегося по
орбите, равен
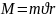 (механический момент). Электрон движется
по орбите создаёт магнитный момент
(механический момент). Электрон движется
по орбите создаёт магнитный момент
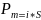 S-площадь
орбиты. За период T ч/з любое сечение
орбиты пройдёт заряд
S-площадь
орбиты. За период T ч/з любое сечение
орбиты пройдёт заряд
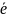 , что соответствует току
, что соответствует току
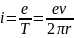
Найдём отношение магнитного момента к механическому
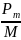 =
=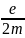 ;
;
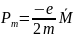
Эксперимент
соотношения для атомов Fe
привело к рез-ту, в 2 раза превысило
результат, записанный выше: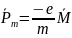
Этот факт привёл к предположению , что обладает собственным механическим и магнитным моментам. Основными экспериментами , подтверждающий этот факт являются опыты Штерна-Герлоха и спектры излучения цельных металлов.
1.Опыты
Штерна-Герлоха атомы H , находится в
S-сост. пропускаемый ч/з неоднородное
магнитное поле, на атомы в неоднородное
магнитное поле должна действовать сила
, в том случае , если атомы обладают
магнитным моментом
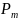 , но в s – состоянии магнитное число m=0.
В соответствии гиромагнитным соотношениям
, нулевому мехоническому моменту e=0
соответствует нулевой магнитный момент.
, но в s – состоянии магнитное число m=0.
В соответствии гиромагнитным соотношениям
, нулевому мехоническому моменту e=0
соответствует нулевой магнитный момент.
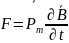
В S состоянии атом орбит механич и магнитными моментами не обладает т.е в опыте Штерна –Герлоха не должно было бы наблюдаться отклонение пучка атома H , тем не менее на экране наблюдался вместо однако пятна 2 (пучёк раздвоился)
Действие магнитного поля на пучёк в S- состоянии можно было объяснить , только предполож. , что атом обладает собст. магнитным моментом, кот. складывается из собственных моментов электронов.
Атом водорода имеет 1 электрон т.к. опыты Штерна- Герлоха привели к заключ., что обладает собственным магнитным моментом изависит от проекции этого момента . Расчит значение собственного магнитного момента электрона. Получим название магнетона Бора.
С собственным магнитным моментом связан собственный магнитный момен.-спин. Ярким подтверждением существованию собственн. магнитному и мех. моментов является спектры щелочных металлов в частном случае спектры Na, в котором вместо 1й линии, соотв переходу 2p->1S наблюдается две линии, соответствующие этому переходу.
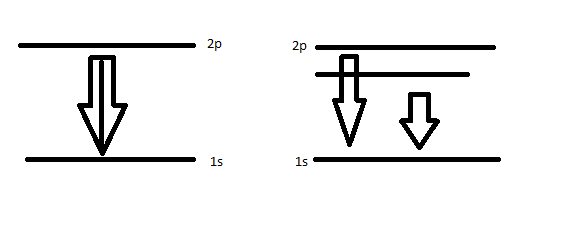
Состоянию p соответствует l=1. В этом случае магнитное число m принимает значения -1,0,1.
Вырожение по магнитному числу m, это выражение снимается в магнитном поле , в котором должно было бы наблюдаться 3 линии соответствующие значению m. Дуплет Na наблюдается и в отсутствии внешнего магнитного поля . Кроме того наблюдается 2 линии , а не 3. Наличие линий объясняется следующим образом: круговые токи в атомах создают слабое магнитное поле, которое оказывает воздействие на собственный магнитный момент электрона и в зависимости от его проекции на направление поля появляется 2 линии. Определим условие квантования механического момента.
Магнетон
Бора опред. проекцию момента на некоторое
направление. Воспользуемся соотношением
для собственных моментов и подставим
туда значения магнитона Бора : ;
;
 ;
;
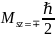 ;
;
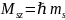 ,
то
,
то
 =>
=>
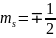
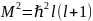
Магнитное
число m
связано с орбитальным числом , чтобы
провести различие м/ у l и квантовым
числом, определяющее условие квантования
собственного мех момента, его обозначают
буквой S , тогда условие квантования
собственного мех момента
запишется в виде
 ,
используем связь
,
используем связь
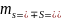 S=
S=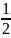
Условие
квантования орбит механического момента
:
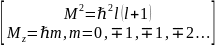
Условие
квантования собств механического
момента:
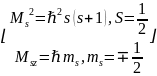
Каждое
состояние характеризуется суммарным
значение момента импульса: Полный момент
импульса:
 ,
j=
,
j= ,
j меняется от l+S до
,
j меняется от l+S до