
- •Учение о доминанте и констелляции нервных центров
- •Свойства доминантного центра
- •Свойства Применяется в качестве лекарственного вещества и для фармакологических исследований. Это соединение получают синтетическим путём в виде хлорида или другой соли. Медицинские
- •Участие в процессах жизнедеятельности
- •Применение Общее применение
- •Норадреналин как нейромедиатор
- •Синтез норадреналина
- •Классификация
- •Физиологическая роль
- •Серотонин как нейромедиатор
- •Функции серотонина
- •Строение
- •Тело клетки
- •Дендриты и аксон
- •Классификация
Билет 1 1.Возбудимые мембраны и мембранный потенциал клетки.
Возбудимые мембраны. Все электрические сигналы возникают на цитоплазматической мембране. Клеточная мембрана представляют собой тонкую липопротеиновую пластинку, содержание липидов в которой составляет около 40%, белков – 60%. Основу биологических мембран составляет фосфолипидный двойной слой, являющийся барьером для заряженных частиц и молекул водорастворимых веществ.Молекулы фосфолипидов состоят из 2 частей: одна из них несет заряд и гидрофильна, другая – не заряжена и гидрофобна. Липиды на гидрофильном («притягивающем воду») конце образуют гидратную оболочку. Гидрофобную («водоотталкивающую») часть образуют жирные кислоты. В фосфолипидный слой встроены молекулы белков. Клеточные мембраны обладают избирательной проницаемостью, т.е. одни вещества пропускают, а другие – нет. Этот обеспечивается благодаря встроенным белкам, образующим каналы. Мембрана легко проницаема для жирорастворимых веществ, проникающих через липидный слой. Потенциал покоя – относительно стабильная разность электрических потенциалов между наружной и внутренней сторонами клеточной мембраны. Его величина обычно варьирует в пределах от -30 до -90 мВ. Внутренняя сторона мембраны в покое заряжена отрицательно, а наружная – положительно из-за неодинаковых концентраций катионов и анионов внутри и вне клетки. Потенциал действия (ПД) - это быстрый электрофизиологический процесс, выражающийся в быстром колебании мембранного потенциала покоя вследствие перемещения ионов в клетку и из клетки и способный распространяться без затухания (декремента). ПД возникает в ответ на достаточное по силе раздражение. Слабое (подпороговое) раздражение может вызвать локальный потенциал. Он подчиняется закону силы: с увеличением стимула величина его также возрастает. В составе ПД различают 3 фазы: 1) деполяризацию, т.е. исчезновение заряда клетки (уменьшение МПП до 0); 2) инверсию, т.е. изменение заряда на обратный и 3) реполяризацию, т.е. восстановление исходного потенциала клетки. В потенциале действия (ПД) различают пик (спайк) и следовые потенциалы. Пик ПД представляет собой кратковременную инверсию внутриклеточного потенциала.
2.Ассиметрия полушарий
Межполушарная асимметрия — одна из фундаментальных закономерностей организации мозга не только человека, но и животных. Проявляется не только в морфологии мозга, но и в межполушарной асимметрии психических процессов. Межполушарная асимметрия психических процессов — функциональная специализированность полушарий головного мозга: при осуществлении одних психических функций ведущим является левое полушарие, других — правое. Исследования асимметрии больших полушарий головного мозга у человека свидетельствует о существовании особого принципа построения и реализации таких важнейших функций мозга, как восприятие, внимание, память, мышление и речь. В настоящее время считается, что левое полушарие у правшей играет преимущественную роль в экспрессивной и импрессивной речи, в чтении, письме, вербальной памяти и вербальном мышлении. Правое же полушарие выступает ведущим для неречевого, например, музыкального слуха, зрительно-пространственной ориентации, невербальной памяти, критичности.В левом полушарии сконцентрированы механизмы абстрактного, а в правом — конкретного образного мышления . Также было показано, что левое полушарие в большей степени ориентировано на прогнозирование будущих состояний, а правое — на взаимодействие с опытом и с актуально протекающими событиями.В процессе индивидуального развития выраженность межполушарной асимметрии меняется — происходит латерализация функций головного мозга. Последние исследования свидетельствуют о том, что межполушарная асимметрия вносит существенный вклад в проявление высокого интеллекта человека. При этом в известных пределах существует взаимозаменяемость полушарий головного мозга. Основные функции полушарий и связь между ними: Логика и распознавание образов, Распознавание цветов, Организация речи. Синдром «расщеплённого мозга» Так как межполушарное взаимодействие служит основой осуществления высших психических функций, нарушение этого взаимодействия у взрослых может приводить к формированию синдрома «расщепленного мозга». Этот синдром проявляется в нарушении сенсорных, речевых, двигательных и конструктивно-пространственных функций. Нарушения, произошедшие в раннем возрасте, могут быть частично скомпенсированы.
Билет 2
1.Потенциал действия и механизм его возникновения.
Все клетки и ткани организма обладают раздражимостью, являющейся общим свойством живой материи. Реакции отдельных клеток на действие раздражителя могут быть разнообразными: изменение интенсивности обмена веществ, рН, изменение проницаемости клеточной мембраны, движение ионов, и др. Раздражение – процесс действия раздражителя (фактора внешней или внутренней среды) на клетку. Частный случай раздражимости – возбудимость.Возбудимыми называются ткани, клетки которых способны в ответ на раздражение генерировать специфическую реакцию – возбуждение. Возбуждение – процесс перехода живой клетки из состояния покоя в состояние активности, сопровождающийся появлением в клетке высокоамплитудного электрического сигнала - потенциала действия (нервного импульса).Потенциал действия (ПД) - это быстрый электрофизиологический процесс, выражающийся в быстром колебании мембранного потенциала покоя вследствие перемещения ионов в клетку и из клетки и способный распространяться без затухания (декремента). ПД возникает в ответ на достаточное по силе раздражение. Слабое (подпороговое) раздражение может вызвать локальный потенциал. Он подчиняется закону силы: с увеличением стимула величина его также возрастает. В составе ПД различают 3 фазы: 1) деполяризацию, т.е. исчезновение заряда клетки (уменьшение МПП до 0); 2) инверсию, т.е. изменение заряда на обратный и 3) реполяризацию, т.е. восстановление исходного потенциала клетки. Длительность ПД составляет 1 мс. По ходу ПД можно выделить восходящую и нисходящую фазы (примерно по 0.5 мс каждая). Восходящая фаза (деполяризация): вход в клетку «порции» Na+. Нисходящая фаза (реполяризация): выход из клетки примерно такой же «порции» К+. В основе этих процессов – открывание и закрывание электрочувствительных Na+- и К+-каналов. Эти каналы имеют створки, реагирующие на изменение заряда внутри нейрона и открывающиеся, если этот заряд становится выше -50 мВ. Открытие электрочувствительного Na+-канала «разрешает» вход Na+ в клетку. Открытие электрочувствительного К+-канала «разрешает» выход К+ из клетки. Na+-каналы открываются очень быстро после стимула и самопроизвольно закрываются примерно через 0.5 мс. К+-каналы открываются медленно – в течение примерно 0.5 мс после стимула; закрываются они в большинстве своем к моменту снижения заряда нейрона до уровня ПП. Именно разная скорость открытия Na+-каналов и К+-каналов позволяет возникнуть сначала восходящей, а затем – нисходящей фазе ПД. (сначала ионы Na+ вносят в нейрон положительный заряд, а затем ионы К+ выносят его, возвращая клетку в исходное состояние). Если заряд внутри нейрона вновь ниже -50 мВ – створка закрывается, т.к. положительные заряды, расположенные на ней, притягиваются к отрицательно заряженным ионам цитоплазмы. В потенциале действия (ПД) различают пик (спайк) и следовые потенциалы. Пик ПД представляет собой кратковременную инверсию внутриклеточного потенциала.Общая длительность пика приблизительно равна 3 мс. Амплитуда пика 110 мВ, т. е. она превышает МПП (-70 мВ) на 40 мВ. Вслед за пиком ПД регистрируются значительно более слабые и длительные отрицательный и далее положительный следовой потенциал.
2. Антиноцицептивная система.
Сегодняшние представления о формировании боли основаны на представлениях о существовании двух систем: ноцицептивной (НС) и антиноцицептивной (АНС). Ноцицептивная система (является восходящей) обеспечивает проведение боли от периферических (ноцицептивных) рецепторов до коры головного мозга. Антиноцицептивная система (является нисходящей) предназначена для контроля над болью. На первом этапе формирования боли происходит активация болевых (ноцицептивных) рецепторов. К активации болевых рецепторов может привести, например, воспалительный процесс. Это вызывает проведение болевых импульсов к задним рогам спинного мозга. На сегментарном спинальном уровне происходит модуляция ноцицептивной афферентации, которая осуществляется влиянием нисходящих антиноцицептивных систем на различные опиатные, адренергические, глютаматные, пуриновые и другие рецепторы, расположенные на нейронах заднего рога. Этот болевой импульс затем передается в вышележащие отделы центральной нервной системы (таламус, кора головного мозга), где происходит обработка и интерпретация информации о характере и локализации боли. Основную роль в перестройке состояния ЦНС играют антиноцицептивные (анальгетические) системы мозга. Антиноцицептивные системы мозга образованы группами нейронов или гуморальными механизмами, активация которых вызывает угнетение или полное выключение детальности различных уровней афферентных; систем, участвующие в передаче и обработке ноцицептивной информации. Происходит это путем изменения чувствительности к медиатору постсинаптической мембраны ноцицептивного нейрона. В результате, несмотря на то, что к нейрону импульсы по ноцицептивным путям подходят, возбуждения они не вызывают. Отличительной особенностью антиноцицептивных факторов является большая продолжительность (несколько секунд) их эффекта.В настоящее время можно говорить о четырех видах антиноцицептивных систем: двух нейронных и двух гормональных. Нейронные системы Нейронная опиатная система. Она получила свое название в связи с тем, что рецепторы медиаторов этих нейронов обладают способностью соединяться с фармакологическими препаратами, полученными из опия. Из-за структурно-функционального сходства с экзогенными опиатами медиаторы указанных антиноци-цептивных нейронов получили название эндорфины. К эндорфинам относится группа веществ пептидной природы, образующихся в нейронах из предшественника — проопиомелонокортина. Пептидами являются также и близкие к эндорфинам энкефалины.
Билет 3
1.Потенциал действия и механизм его проведения.
Все клетки и ткани организма обладают раздражимостью, являющейся общим свойством живой материи. Реакции отдельных клеток на действие раздражителя могут быть разнообразными: изменение интенсивности обмена веществ, рН, изменение проницаемости клеточной мембраны, движение ионов, и др. Раздражение – процесс действия раздражителя (фактора внешней или внутренней среды) на клетку. Частный случай раздражимости – возбудимость.Возбудимыми называются ткани, клетки которых способны в ответ на раздражение генерировать специфическую реакцию – возбуждение. Возбуждение – процесс перехода живой клетки из состояния покоя в состояние активности, сопровождающийся появлением в клетке высокоамплитудного электрического сигнала - потенциала действия (нервного импульса).Потенциал действия (ПД) - это быстрый электрофизиологический процесс, выражающийся в быстром колебании мембранного потенциала покоя вследствие перемещения ионов в клетку и из клетки и способный распространяться без затухания (декремента). ПД возникает в ответ на достаточное по силе раздражение. Слабое (подпороговое) раздражение может вызвать локальный потенциал. Он подчиняется закону силы: с увеличением стимула величина его также возрастает. В составе ПД различают 3 фазы: 1) деполяризацию, т.е. исчезновение заряда клетки (уменьшение МПП до 0); 2) инверсию, т.е. изменение заряда на обратный и 3) реполяризацию, т.е. восстановление исходного потенциала клетки. Механизм проведения ПД: В распространении ПД выделяют 2 этапа: этап распространения электрического поля, снижающий мембранный потенциал и этап генерации новых ПД в новых участках нервного волокна. Электрическое поле обеспечивает силовое воздействие на электрические заряды, находящиеся в этом поле.В зависимости от расположения и концентрации ионных каналов в мембране мышечного или нервного волокна есть 2 варианта проведения ПД: непрерывный и сальтаторный (скачкообразный). Непрерывное проведение ПД происходит в мышечных волокнах и безмиелиновых нервных волокнах (тип С), имеющих равномерное распределение ионных каналов по всей длине волокна. Сальтаторное проведение ПД по миелинизированным волокнам является эволюционно более поздним механизмом, возникшим у позвоночных. Оно происходит в миелинизированных волокнах (тип А и В), для которых характерна концентрация ионных каналов только в небольших участках мембраны (перехватах Ранвье). ПД, возникший в одном перехвате Ранвье, за счет электрического поля деполяризует мембрану соседних участков до критического уровня, что приводит к возникновению в них новых ПД. Сравнение непрерывного и сальтаторного возбуждения показывает, что различие в механизме проведения возбуждения по миелинизированным и немиелинизированным нервным волокнам не принципиально. Однако сальтаторное возбуждение имеет преимущества: 1) оно более экономично в энергетическом плане, поскольку надо меньше энергии для восстановления градиентов ионов Na и K ; 2) возбуждение в миелинизированных волокнах осуществляется с большей скоростью, чем в немиелинизированных, т.к. в них электрическое поле ПД в области миелиновых муфт распространяется значительно дальше – на соседние перехваты Ранвье.
2. Функциональное значение и классификация гормонов.
Гормо́ны — биологически активные сигнальные химические вещества, выделяемые эндокринными железами непосредственно в организме и оказывающие дистанционное сложное и многогранное воздействие на организм в целом либо на определённые органы и ткани-мишени. Гормоны служат гуморальными (переносимыми с кровью) регуляторами определённых процессов в различных органах и системах. Используются в организме для поддержания его гомеостаза, а также для регуляции многих функций (роста, развития, обмена веществ, реакции на изменения условий среды). Функциональное значение гормонов
Гормоны оказывают широкое регулирующее влияние на различные функции организма. Выделяют три основные функции гормонов — они обеспечивают: развитие организма; адаптацию физиологических систем (т. е. способность органов и тканей изменять активность в зависимости от потребности в ней); поддержание важнейших физиологических показателей на постоянном уровне (гомеостатическая функция). Различные биохимические реакции могут протекать правильным образом лишь в присутствии одного или нескольких гормонов, хотя при увеличении их концентрации реакция не ускоряется. В этих случаях проявляется пермиссивное (разрешающее) действие гормона, т. е. сам гормон не влияет на данную систему, но обеспечивает возможность нормального действия другого гормона. Например, тироксин обладает пермиссивным действием по отношению к гормонам, регулирующим рост.Еще одной важной особенностью действия некоторых гормонов является синергизм, т. е. усиление действия одного гормона под влиянием другого. . Классификация гормонов. На основании функциональных критериев различают три группы гормонов: 1) гормоны, которые оказывают влияние непосредственно на орган—мишень; эти гормоны называются эффекторными 2) гормоны, основной функцией которых является регуляция синтеза и выделения эффекторных гормонов;эти гормоны называют тропными 3) гормоны, вырабатываемые нервными клетками и регулирующие синтез и выделение гормонов аденогипофиза; эти гормоны называются рилизинг—гормонами, или либеринами, если они стимулируют эти процессы, или ингибирующими гормонами, статинами, если они обладают противоположным действием. Тесная связь между ЦНС и эндокринной системой осуществляется в основном с помощью этих гормонов.В сложной системе гормональной регуляции организма различают более или менее длинные цепи регуляции. Основная линия взаимодействий: ЦНС → гипоталамус → гипофиз → периферические эндокринные железы. Все элементы этой системы объединены обратными связями. Функция части эндокринных желез не находится под регулирующим влиянием гормонов аденогипофиза (например, паращитовидные железы, поджелудочная железа и др.).
Билет 4
1 Функциональные структуры нейрона и транспорт веществ в нервных клетках.
Функциональные структуры нейрона: Внутренней средой нейрона является гиалоплазма, которая обеспечивает взаимодействие всех клеточных структур друг с другом посредством транспорта веществ, потребляемых и синтезируемых клеткой. В теле нейрона (соме) находятся структуры, обеспечивающие синтез макромолекул, которые затем транспортируются по аксону и дендритам. Большинство внутриклеточных органелл имеют собственные мембраны, построенные по тому же принципу, что и клеточные мембраны. К мембранным органеллам относятся: ядро, эндоплазматический ретикулум, аппарат Гольджи, митохондрии, лизосомы. Немембранные органеллы: рибосомы, микротрубочки, микрофиламенты. Каждая органелла выполняет свои специфические функции. Ядро несет генетическую информацию и обеспечивает синтез белка в клетке. Оно состоит из ядерной оболочки (мембраны), хроматина, ядрышка и кариоплазмы. Оболочка имеет поры, обеспечивающие проход РНК, рибонуклеаз, обмен веществ. Ядрышко – внутриядерное образование, не имеющее мембраны, в котором синтезируется рибосомная РНК и образуются рибосомы. Хроматин состоит из витков ДНК и содержит РНК. Это главные компоненты хромосомы, выполняющие 2 функции: генетическую (хранение и передачу в ряду поколений генетической информации) и метаболическую (управление синтезом белка). Митохондрии (м/х): «электро-станции» клетки (в нейронах – боль-шое кол-во м/х); здесь завершается окисление органических веществ (прежде всего, глюкозы); при этом расходуется О2, выделяется СО2 и из АДФ образуется АТФ. АТФ – аденозинтрифосфорная к-та АДФ – аденозиндифосфорная к-та. АДФ + фосфорная к-та АТФ(реакция запасания энергии; ею управляют особые дыхательные фер-менты, расположенные на складках-кристах внутренней мембраны м/х). АТФ АДФ + фосфорная к-та (реакция выделения энергии; идет в любой части клетки, где необходимо «привести в действие» белки-насосы, ферменты и т.п.) Эндоцитоз и экзоцитоз – это два вида транспорта, посредством которых различные материалы переносятся через мембрану либо в клетку (эндоцитоз), либо из клетки (экзоцитоз). Транспорт веществ в нервных клетках обеспечивает: 1) поступление в клетку веществ, необходимых для синтеза клеточных структур и выработки энергии, 2) выделение продуктов обмена и биологически активных веществ – нейрогормонов, медиаторов, 3) создание электрических зарядов клеток, возникновение и распространение возбуждения. Основные виды транспорта:1) транспорт веществ с помощью насосов (помп); 2) эндоцитоз и экзоцитоз (микровезикулярный транспорт); 3) аксонный транспорт. Аксонный транспорт. Основная масса веществ, образующихся в теле нейрона (ферментов, структурных белков, полисахаридов, липидов) используется в различных его отделах. Транспорт в отростках нейрона - аксонах – получил название аксонного транспорта. С его помощью осуществляется влияние на различные участки нейрона и на иннервируемые клетки. Различают быстрый и медленный аксонный транспорт. Транспорт в отростках нейрона - аксонах – получил название аксонного транспорта. С его помощью осуществляется влияние на различные участки нейрона и на иннервируемые клетки. Различают быстрый и медленный аксонный транспорт. Быстрый аксонный транспорт осуществляется с помощью специальных структурных элементов нейрона: микротрубочек и микрофиламентов. Для транспорта необходима энергия АТФ. Медленный аксонный транспорт осуществляется только в антероградном направлении и представляет собой передвижение всего столба аксоплазмы. С помощью медленного аксонного транспорта перемещаются белки микротрубочек и микрофиламентов (тубулин, актин и др.), ферменты, РНК, белки каналов, насосов. Аксонный транспорт играет важную роль также и при регенерации поврежденных нервных волокон.
Функции продолговатого мозга.
Продолговатый мозг и мост выполняют ряд функций. Здесь находятся центры: дыхательный, сосудодвигательный, пищевого поведения и др.

Оливные ядра связаны с зубчатыми ядрами мозжечка и являются промежуточными ядрами равновесия. Оливные ядра достигают наибольшей выраженности у человека в связи с вертикальным положением тела, так как прямохождение нуждается в совершенном вестибулярном аппарате.
В продолговатом мозге находится ретикулярная формация (reticulum – сеть), образованная переплетением нервных волокон и лежащих между ними нервных клеток. Двигательная часть ретикулярной формации содержит центры, обеспечивающие контроль за кровообращением и дыханием.
Ретикулоспинальный тракт Через него ретикулярная формация оказывает влияние как на двигательную деятельность спинного мозга (осуществление спинальных рефлексов), так и на вегетативную регуляцию (сосудодвигательная, дыхательная, пищеварительная функции).
В продолговатом мозге выделяют дыхательный центр - совокупность нейронов, способных генерировать дыхательный ритм
Билет5
1.Организация дыхательного центра.
Регуляция дыхательной функции осуществляется иерархической системой нервных структур, расположенных на разных этажах нервной системы: -мотонейроны спинного мозга; - продолговатый мозг; - варолиев мост; - средний мозг; -гипоталамус; -лимбико-ретикулярный комплекс; - кора больших полушарий.
В продолговатом мозге выделяют дыхательный центр - совокупность нейронов, способных генерировать дыхательный ритм
Импульсы от нейронов продолговатого мозга идут к мотонейронам спинного мозга, которые посылают информацию к дыхательным мышцам по диафрагмальным и межреберным нервам. Центр диафрагмальных нервов находится в основном в 3-4-ом шейных сегментах спинного мозга. Центры межреберных нервов, иннервирующих мускулатуру грудной клетки, локализуются в грудном отделе спинного мозга.
Вышележащие отделы ЦНС, принимающие участие в регуляции дыхания В регуляции дыхания принимают участие также варолиев мост, средний мозг, гипоталамус, лимбико-ретикулярный комплекс, кора большого мозга. Периодичность в работе дыхательного центра продолговатого мозга может обеспечиваться за счет регулирующих влияний со стороны т.н. пневмотаксического центра, который находится в области варолиева моста и состоит из двух типов нейронов - инспираторных и экспираторных.
Пневмотаксический центр периодически затормаживает инспираторную часть дыхательного центра и стимулирует экспираторные нейроны, осуществляя таким образом прекращение вдоха и начало выдоха. Мост играет важную роль в регуляции продолжительности фаз вдоха, выдоха и паузы между ними. Нейроны моста при взаимодействии с нейронами продолговатого мозга обеспечивают нормальный цикл дыхания.
Средний мозг играет важную роль в регуляции тонуса всей мускулатуры организма, в том числе и дыхательной. Гипоталамус выполняет интегрирующую роль в вегетативном обеспечении соматической деятельности, в том числе участвует в регуляции частоты и глубины дыхания при физической деятельности, повышении температуры внешней и внутренней среды.
Кора большого мозга – произвольное изменение частоты и глубины дыхания. Благодаря коре большого мозга при выполнении физических упражнений интенсивность дыхания становится адекватной потребностям организма (более экономное дыхание).
2.Жизненный цикл медиатора.
В начале XX в. среди физиологов господствовало представление, что сигналы от клетки к клетке передаются через синапс с помощью электрических импульсов. Однако исследования немецкого физиолога О.Леви, русского ученого А.Ф.Самойлова и английского исследователя Г. Дейла показали, что из окончаний нейронов выделяются химические вещества, которые передают информацию к постсинаптической клетке. Эти вещества получили название нейромедиаторов. Медиатор (посредник, трансмиттер) - это химическое вещество, передающее возбуждение с нервного окончания на клетку. Медиаторами синапсов ЦНС являются многие химические вещества, разнородные в структурном отношении. По химическому строению медиаторы можно разделить на несколько групп: амины, аминокислоты, пептиды и др.
2 Жизненный цикл медиатора.
1 - синтез и накопление в пресинаптическом окончании;2 - выброс в синаптическую щель при появлении ПД;3 - действие на рецепторы постсинаптической мембраны (запуск возбуждения или торможения постсинаптической клетки);4 - инактивация (прекращение действия медиатора на рецептор). Для синтеза необходимы: (1) вещество-предшественник (или несколько веществ); (2) белок-фермент (или несколько ферментов);(3) АТФ. Синтез происходит в соме либо прямо в пресинаптическом окончании. Если синтез идет в соме, то далее: (а) ЭПС переносит медиатор в комплекс Гольджи; (б) комплекс Гольджи образует везикулы с медиатором; (в) везикулы по аксону (с опорой на белковые микротрубочки-«рельсы») переносятся в пресинаптическое окончание, где и накапливаются. Если синтез идет прямо в пресинаптическом окончании, то далее медиатор «загружается» в пустые везикулы (с помощью особых белков-насосов). Комплекс Гольджи в этом случае поставляет пустые везикулы (1); значительная часть пустых везикул отделяется от пресинаптической мембраны (2) после выброса медиатора (3). Выброс (экзоцитоз) медиатора в синаптическую щель происходит после появления ПД, который вызывает открывание электрочувствительных Са2+-каналов (примерно на 2-3 мс). В результате в пресинаптическое окончание успевает войти несколько сот ионов Са2+ , которые активируют белки, запускающие экзоцитоз. Для экзоцитоза одной везикулы требуется несколько (не < 4-х) ионов Са2+. Увеличение концентрации Са2+ в межклеточной среде ведет к его более активному входу в пресинаптическое окончание и росту выброса медиатора.
Билет6
Нейроны-пейсмекеры (водители ритма).
Нейрон может находиться в различных состояниях: а) в состоянии покоя – практически отсутствуют колебания мембранного потенциала, ПД не генерируется; б) в состоянии активности – генерировать потенциалы действия (для нейронов характерна генерация серии или пачки импульсов). Состояние активности может быть индуцировано за счет поступления к нейрону импульсов от других нейронов или быть спонтанным (автоматия). В этом случае нейрон играет роль пейсмекера (водителя ритма). Такие нейроны имеются в ряде центров, например, в центре дыхания; в) в состоянии торможения – оно проявляется в том, что нейрон прекращает свою импульсную активность (нейрон – пейсмекер, или нейрон, получающий возбуждающие воздействия). В основе торможения лежит явление гиперполяризации нейрона (это характерно для постсинаптического торможения).
В нервной клетке при развитии потенциала действия возникает период рефрактерности или невозбудимости. Это явление заключается в том, что на фоне потенциала действия и еще некоторое время после его завершения, нельзя вызвать второй разряд клетки, невзирая на силу применяемого раздражения. Время, в течение которого нервная клетка невозбудима, называется абсолютной рефрактерностью. Затем клетка приобретает возможность реагировать на прилагаемые раздражения, но впервые возникающий после периода абсолютной рефрактерности потенциал имеет меньшую амплитуду, так как возникает при меньшем уровне заряда мембраны. Периоды появления неполных ответов называются периодами относительной рефрактерности.
Принцип доминанты.
Во все моменты жизнедеятельности создаются условия, при которых выполнение какой-либо функции становится более важным, чем выполнение других функций. Выполнение данной функции подавляет другие функции.
Учение о доминанте и констелляции нервных центров
Доминанта, по мнению Ухтомского, есть комплекс определённых симптомов во всём организме — и в мышцах, и в секреторной работе, и в сосудистой деятельности. Она представляется не как топографически единый пункт возбуждения в центральной нервной системе, но как «определённая констелляция центров с повышенной возбудимостью в разнообразных этажах головного и спинного мозга, а также в автономной системе». Констелляция нервных центров — это совокупность нервных центров, объединенных единством действий.
Роль нервного центра может существенно изменяться: из возбуждающей становиться тормозящей для одних и тех же приборов в зависимости от состояния, переживаемого нервным центром в данный момент. В различных ситуациях нервный центр может приобретать разное значение в физиологии организма. «Вновь приходящие волны возбуждения в центрах будут идти по направлению главенствующего сейчас очага возбуждения».
Ухтомский считал, что доминанта способна трансформироваться в любое «индивидуальное психическое содержание». Однако доминанта не является прерогативой коры головного мозга, это общее свойство всей центральной нервной системы. Он видел разницу между «высшими» и «низшими» доминантами. «Низшие» доминанты носят физиологический характер, «высшие» — возникающие в коре головного мозга — составляют физиологическую основу «акта внимания и предметного мышления».
Многочисленные исследования, проведённые Ухтомским, его коллегами и независимыми учёными свидетельствовали о том, что доминанта играет роль общего рабочего принципа нервных центров.
Для Ухтомского доминанта была тем, что определяет направленность человеческого восприятия. Доминанта служила тем самым фактором, который интегрирует ощущения в целую картинку (здесь можно провести параллель с гештальтом). Ухтомский считал, что все отрасли человеческого опыта, в том числе и наука, подвержены влиянию доминант, при помощи которых подбираются впечатления, образы и убеждения.
Чтобы овладеть человеческим опытом, чтобы овладеть самим собою и другими, чтобы направить в определённое русло поведение и саму интимную жизнь людей, надо овладеть физиологическими доминантами в себе самих и окружающих.
— Ухтомский А. А. Доминанта и интегральный образ. - 1924.
Свойства доминантного центра
повышенная возбудимость;
способность к суммации;
возбуждение характеризуется высокой стойкостью(инертностью);
способность растормаживаться.
Билет7
Рефлекс – основа регуляции функций.
Рефлекс - основная форма нервной деятельности
Вся деятельность нервной системы осуществляется рефлекторным путем. С помощью рефлексов осуществляется взаимодействие различных систем целого организма и его приспособление к меняющимся условиям среды.
При повышении кровяного давления в аорте рефлекторно меняется деятельность сердца. В ответ на температурные воздействия внешней среды у человека суживаются или расширяются кровеносные сосуды кожи, под влиянием различных раздражителей рефлекторно меняется сердечная деятельность, интенсивность дыхания и т. д.
Благодаря рефлекторной деятельности организм быстро реагирует на различные воздействия внутренней и внешней среды.
Раздражения воспринимаются особыми нервными образованиями - рецепторами. Существуют различные рецепторы: одни из них раздражаются при изменении температуры окружающей среды, другие - при прикосновении, третьи - при болевом раздражении и т. п. Благодаря рецепторам центральная нервная система получает информацию обо всех изменениях окружающей среды, а также об изменениях внутри организма.
При раздражении рецептора в нем возникает нервный импульс, который распространяется по центростремительному нервному волокну и достигает центральной нервной системы. О характере раздражения центральная нервная система "узнает" по силе и частоте нервных импульсов. В центральной нервной системе происходит сложный процесс переработки поступивших нервных импульсов, и уже по центробежным нервным волокнам импульсы от центральной нервной системы направляются к исполнительному органу (эффектору).
Для осуществления
рефлекторного акта необходима целостность
рефлекторной дуги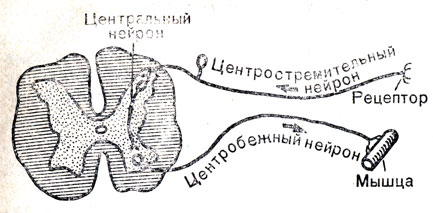
Нервные импульсы при любом рефлекторном акте, приходя в центральную нервную систему, способны распространяться по разным ее отделам, вовлекая в процесс возбуждения многие нейроны. Поэтому правильнее говорить, что структурную основу рефлекторных реакций составляют нейронные цепи из центростремительных, центральных и центробежных нейронов.
Агонисты и антагонисты медиаторов.
Агонист: вещество, действующее как медиатор; обычно – сильнее и длительнее. Молекула состоит из ключевой и защитной частей. Ключевая часть сходна с медиатором и включает рецептор, защитная часть мешает работать системам инактивации. Антагонист: вещество, противодействующее эффектам медиатора. Молекула состоит из защитной части и неполной ключевой части. Последняя из них занимает активный центр рецептора, но не включает его, работая как «сломанный» ключ и мешая медиатору. Антагонисты и агонисты – вещества, поступающие в организм извне.Многие из них – токсины, которые возникли в ходе эволюции растений для защиты от животных. Как следует разбавив их, человек получает лекарственные препараты; не разбавив – яды и наркотики.
Билет8
Синапсы. Их классификация и строение.
Синапсы (строение и классификация) Синапс (от греч. Synapsis – соприкосновение, соединение) - это специализированные структурные соединения между нейронами или нейроном и эффекторной клеткой, обеспечивающие передачу сигнала. Через синапсы передаются возбуждающие или тормозные влияния между 2 возбудимыми клетками.
Структура синапса:
1) пресинаптическая мембрана (электрогенная мембрана в терминале аксона, образует синапс на мышечной клетке);
2) постсинаптическая мембрана (электрогенная мембрана иннервируемой клетки, на которой образован синапс);
3) синаптическая щель (пространство между преси-наптической и постсинаптической мембраной, заполнена жидкостью, которая по составу напоминает плазму крови).
Существует несколько классификаций синапсов.
1. По локализации:
1) центральные синапсы;
2) периферические синапсы.
Центральные синапсы лежат в пределах центральной нервной системы, а также находятся в ганглиях вегетативной нервной системы.
Различают несколько видов периферических синапсов:
1) мионевральный;
2) нервно-эпителиальный.
2. Функциональная классификация синапсов:
1) возбуждающие синапсы;
2) тормозящие синапсы.
3. По механизмам передачи возбуждения в синапсах:
1) химические;
2) электрические.
Передача возбуждения осуществляется при помощи медиаторов. Различают несколько видов химических синапсов:
1) холинэргические. В них происходит передача возбуждения при помощи ацетилхолина;
2) адренэргические. В них происходит передача возбуждения при помощи трех катехоламинов;
3) дофаминэргические. В них происходит передача возбуждения при помощи дофамина;
4) гистаминэргические. В них происходит передача возбуждения при помощи гистамина;
5) ГАМКэргические. В них происходит передача возбуждения при помощи гаммааминомасляной кислоты, т. е. развивается процесс торможения.
Синапсы имеют ряд физиологических свойств:
1) клапанное свойство синапсов, т. е. способность передавать возбуждение только в одном направлении с пресинаптической мембраны на постсинап-тическую;
2) свойство синаптической задержки, связанное с тем, что скорость передачи возбуждения снижается;
3) свойство потенциации (каждый последующий импульс будет проводиться с меньшей постсинапти-ческой задержкой);
4) низкая лабильность синапса (100–150 имульсов в секунду).
Гипоталамо-аденогипофизарная система.
Основное назначение гипоталамо—аденогипофизарной системы — осуществление связей между гипоталамусом и гипофизом. В 40—50—е гг. XX столетия Г. Харрис обратил внимание на наличие системы воротного кровоснабжения, связывающей гипоталамус с гипофизом. В дальнейшем были выяснены функциональные связи между гипоталамусом и гипофизом. В мелких нейросекреторных клетках гипоталамуса, располагающихся в так называемой гипофизотропной зоне, происходит выработка либеринов и статинов, которые регулируют функцию железистых клеток аденогипофиза. Аксоны нейросекреторных клеток оканчиваются в медиальном возвышении, являющемся нейрогемальной областью гипоталамо—аденогипофизарной системы.
Гормоны из гипофизотропной зоны поступают в аденогипофиз через воротные вены гипофиза. Воротная (портальная) система кровообращения начинается ветвями верхней гипофизарной артерии, которые распадаются на мелкие капилляры. Возвратные ветви этих сосудов сливаются, образуя воротные вены, которые несут кровь к капиллярному сплетению аденогипофиза. Аксоны нейросекреторных клеток гипофизотропной зоны оканчиваются на стенках этих сосудистых петель. Из капилляров гипофизотропные гормоны попадают к своим мишеням — клеткам аденогипофиза, вырабатывающим гормоны (см. рис. 6.3).
Функция железистых клеток гипофиза находится под регулирующим влиянием в основном шести либеринов и трех статинов гипоталамуса (табл. 6.2).
Свое название они получили от названий тех гормонов гипофиза, выделение которых они регулируют. Так, гормон, влияющий на тиреотропные клетки гипофиза, называют тиреотропин—рилизинг—гормоном (ТРГ), или тиреолиберином. Все эти гормоны являются малыми пептидами. Структура большинства гормонов расшифрована и осуществлен синтез ряда из них.
На основе рилизинг—гормона лютеинизирующего гормона созданы различные синтетические аналоги люлиберина, отличающиеся более сильным и длительным действием. Это имеет большое значение для дальнейшего изучения физиологической роли этих веществ и находит применение в клинической медицине, сельском хозяйстве, рыбоводстве.
В последние годы установлено, что некоторые из гипофизотропных гормонов синтезируются не только в гипоталамусе, но и в других отделах мозга и даже в других органах. Например, тиреолиберин у амфибий образуется в коже и в плазме крови. У млекопитающих ТРГ обнаружен также в таламусе, мозжечке и других структурах мозга. Множественную локализацию биосинтеза имеет соматостатин, обнаруживаемый кроме гипоталамуса во внегипоталамических областях мозга, а также в кишке и поджелудочной железе, где он тоже выполняет роль фактора, тормозящего секрецию. Эти вещества обнаружены и у ряда беспозвоночных животных.
Функциональная роль нейрорегуляторных пептидов в тех случаях, когда они вырабатываются вне гипоталамуса, выяснена пока далеко не полно. Возможно,что в ряде случаев они являются нейротрансмиттерами. Среди гормонов гипоталамуса найдены пептиды, обладающие морфиноподобным действием. Энкефалины и эндорфины играют роль в регуляции поведения. В гипоталамусе обнаружены и другие пептиды — субстанция Р, нейротензин, ВИП (VIP, вазоактивный интестинальный (кишечный) пептид), бомбезин и др. Часть из них ранее выделяли из кишки и считали гормонами, регулирующими ее деятельность. В мозгу они регулируют обмен веществ, церебральный кровоток и пищевое поведение.
В гипоталамусе, как и в других участках мозга, постоянно синтезируются моноамины, являющиеся необходимым звеном нервных и секреторных процессов.
Предполагают, что нонапептидные гормоны оказывают непосредственное влияние на органы—мишени. Гипофизотропные олигопептиды, по—видимому, возникли позже в эволюции в связи с развитием в системе нейрогормональной регуляции эндокринной железы I порядка — гипофиза.
Билет9
Гипоталамо-нейрогипофизарная система.
Основным структурным элементом гипоталамо-нейрогипофизарной системы являются супраоптическое и паравентрикулярные ядра гипоталамуса, которые в ответ на поступление информации от рецепторов, контролирующих показатели гомеостаза (осмотическое давление, объем циркулирующей крови, артериальное давление), и от высших нервных центров продуцируют вазопрессин и окситоцин. Эти гормоны по аксонам нейроэндокринных клеток спускаются в нейрогипофиз, откуда поступают в кровь.
Вазопрессин (антидиуретический гормон) оказывает следующие влияния:
1) действуя на дистальные извитые канальцы и собирательные трубки почек, усиливает реабсорбцию воды (антидиуретический гормон);
2) вызывает сокращение гладких мышц кровеносных сосудов;
3) усиливает гликогенолиз и глюконеогенез в печени;
4) способствует консолидации следов памяти и мобилизации сохраняемой информации (гормон памяти);
5) является эндогенным анальгетиком (угнетает боль).
Окситоцин оказывает следующие функциональные эффекты:
1) стимулирует выделение молока (лактацию), вызывая сокращение миоэпителиальных клеток мелких протоков молочных желез;
2) инициирует и усиливает сокращения беременной матки;
3) ухудшает запоминание и мобилизацию информации (амнестический гормон).
Глутаминовая кислота и ГАМК – главные медиаторы ЦНС: синтез, типы рецепторов, инактивация.
Медиаторы-аминокислоты - главные медиатора ЦНС. Глутаминовая кислота (Glu) – главный возбуждающий медиатор; проведение основных потоков информации в ЦНС (сенсорные сигналы, двигательные команды, память). Гамма-аминомасляная кислота (ГАМК) – главный тормозный медиатор; запрет проведения «ненужной» информации (внимание, двигательный контроль). Глицин – вспомогательный тормозный медиатор (менее 1%; основная функция – торможение мотонейронов).
Нормальная деятельность ЦНС обеспечивается тонким балансом Glu и ГАМК. Нарушение этого баланса (как правило, в сторону уменьшения торможения) негативно влияет на многие нервные процессы – вплоть до возникновения мощных локальных очагов возбуждения.
Глутаминовая кислота
Пищевая аминокислота – входит в состав белков пищи и белков нашего тела.
В водных растворах существует в ионизированном виде, то есть в форме отрицательно заряженного остатка глутамата («глютамата»).
Во всех тканях организма (в т.ч. в мозге) очень много Glu. В связи с этим долгое время не могли поверить, что столь распространенное вещество является медиатором ЦНС.
Но пищевой глутамат почти не преодолевает ГЭБ, и для выполнения медиаторных функций Glu синтезируется непосредственно в пресинаптических окончаниях из глутамина.
После синтеза Glu загружается в везикулы (◄ ), выбрасывается в синаптическую щель при приходе ПД и влияет на рецепторы ( ↓↓↓ ), запуская ВПСП.
Введение Glu непосредственно в мозг (в желудочки) вызывает возбуждение ЦНС и судороги. Сходные эффекты наблюдаются при отравлении агонистами Glu, часть из которых является токсинами растений.
Рецепторы глутамата В настоящее время выделяют три типа ионотропных и не менее трех типов метаботропных рецепторов к Glu. Все они запускают ВПСП, повышая проводимость Na+. Метаботропные рецепторы (mGluR1, mGluR2, …) действуют через вторичные посредники. Ионотропные рецепторы : NMDA-рецепторы, АМРА-рецепторы, каинатные рецепторы.
Каждый такой рецептор состоит из 4-х белковых молекул; в открытом положении он проницаем для Na+, Са2+, К+.
Уникальная особенность NMDA-рецепторов состоит в том, что их канал может блокироваться ионом Mg2+ («магниевая пробка»). В такой ситуации рецептор выключен, и ВПСП не возникает. Однако, если заряд в нейроне оказывается выше уровня -30 мВ, Mg2+ удаляется из канала («выбивание пробки»), и рецептор переходит в рабочее состояние.
Этот механизм – один из важнейших способов резко усилить эффективность работы синапса, создать новый путь для передачи информации. Подобные изменения лежат в основе процессов обучения и формирования памяти; характерны для коры больших полушарий и, особенно, гиппокампа, избирательно связанного с кратковременной памятью.
Антагонисты Glu. Основные клинические проблемы связаны с избыточной активностью Glu-синапсов. Соответственно, востребованы антагонисты Glu. В настоящее время на практике применяют антагонисты наиболее изученного NMDA-рецептора (мемантин, кетамин). Мемантин: блокирует канал рецептора в его верхней части; снижает тревожность и вероятность эпилептических припадков. Кетамин (калипсол): блокирует канал рецептора в его нижней части. Вызывает кратковременный, но глубокий наркоз (используется в ветеринарии). Инактивация Glu:
Из синаптич. щели Glu переносится в глиальные клетки, где превращаетсяв глутамин (Gln) (с помощью фермента
глутамин синтетазы).
Глутамин затем может перемещаться в преси-наптическое окончание и вновь становиться Glu в митохондриях (далее – упаковка в везикулу).
Часть Glu возвращается из синаптической щели прямо в пресинаптич. окончание («обратное всасывание»).
ГАМК
Непищевая аминокислота.
Синтез – из глутаминовой кислоты за счет отщепления СО2 (фермент глутамат декарбоксилаза).
ГАМК может использоваться в качестве медиатора, но может терять аминогруппу (фермент ГАМК-трансфераза) и быстро окисляться с выдел. энергии.
ГАМК на 10% проходит ГЭБ. Однако при ее системном введении (таблетки «Аминалон») наблюдается не столько торможение ЦНС, сколько «питание» нейронов и улучшение их общего состояния (ноотропное действие ГАМК).
Ноотропы выделяют в особую группу лекарственных препаратов. Их объединяет способность стимулировать высшие психические функции (память, мышление). Первым ноотропом стал ноотропил (пирацетам), созданный путем химической модификации ГАМК.
Рецепторы ГАМК
Выделяют два основных типа рецепторов ГАМК:
(GABA – gamma-aminobutyric acid)
ГАМКА – ионотропные, образуют хлорный канал, вызывают ТПСП.
ГАМКБ – метаботропные, связаны с калиевым каналом, чаще расположены на пресинаптической мембране; тормозят экзоцитоз различных медиаторов.
Лучше изучен ГАМКА рецептор, агонисты которого (прежде всего, барбитураты и бензодиазепины) имеют огромное клиническое значение.
Антагонисты ГАМК: вызывают судороги.
Бикукулин – мешает ГАМК присоединяться к рецептору А-типа; токсин североамериканского травянистого растения дицентры клобучковой.
Пикротоксин – блокирует хлорный канал; токсин плодов индийского кустарника Anamirta cocculus.
Лучше изучен ГАМКА рецептор, агонисты которого (прежде всего, барбитураты и бензодиазепины) имеют огромное клиническое значение.
Антагонисты ГАМК: вызывают судороги. Одно и то же вещество (например, валиум) в зависимости от дозы может оказывать: успокаивающее (транквилизирующее) действие противоэпилептическое действие снотворное действие, наркоз.
Билет10
Постсинаптическое торможение.
Постсинаптическое торможение - это снижение возбудимости постсинаптической мембраны(утолщенный участок мембраны дендрита в области синапса . Постсинаптическая мембрана содержит крупные белковые молекулы, действующие как рецепторы медиаторов , и многочисленные лиганд- зависимые каналы и поры, обычно закрытые, через которые в постсинаптический нейрон могут поступать ионы.) нейрона, препятствующее распространению импульса.
Нервный импульс в тормозных нейронах вызывает гиперполяризационный сдвиг потенциала, в результате чего уровень мембранного потенциала(Нервные клетки ограничены липопротеиновой мембраной , являющейся электрическим изолятором. Между содержимым клетки и внеклеточной жидкостью существует разность потенциалов, так называемый мембранный потенциал) начинает сильнее отличаться от порогового потенциала(Мембранный потенциал , при котором начинается потенциал действия , называется пороговым потенциалом.) , необходимого для генерации потенциала действия .
Поэтому гиперполяризация постсинаптической мембраны называется тормозным постсинаптическим потенциалом .
Механизм высвобождения медиатора в тормозных синапсах и возбуждающих синапсах , видимо, аналогичен. Тормозным медиатором в мотонейронах и некоторых других синапсах служит аминокислота глицин . Медиатор, действуя на постсинаптическую мембрану, открывает поры, или каналы, через которые могут проходить все мелкие ионы. Если стенка поры несет электрический заряд, то он препятствует прохождению одноименно заряженных ионов.
При одновременном возникновении возбуждающих и тормозных синаптических процессов амплитуда возбуждающего постсинаптического потенциала уменьшается в зависимости от амплитуды тормозного постсинаптического потенциала .
Функции среднего мозга.
Средний мозг выполняет следующие функции:
двигательную,
сенсорную (зрение, слух),
регулирующую в продолжительности актов жевания и глотания Средний мозг является продолжением ствола мозга. К нему относятся: четверохолмие, ножки мозга, черное вещество, красные ядра. Через средний мозг проходят нервные восходящие пути, несущие импульсы от спинного и продолговатого мозга к вышележащим отделам: мозжечку, зрительным буграм промежуточного мозга, коре больших полушарий. Нисходящие нервные пути проводят возбуждение к продолговатому и спинному мозгу. В среднем мозге, (как и в продолговатом), расположены нервные образования ретикулярной системы. Ядра (скопления нейронов) среднего мозга выполняют целый ряд важнейших физиологических функций. Первичные слуховые и зрительные центры четверохолмия осуществляют ориентировочные реакции. Они подготавливают организм к восприятию внезапного раздражения, перераспределяя мышечный тонус. Красные ядра находятся в центральной части среднего мозга. В их функцию входит регуляция мышечного тонуса, т. е. поддержание и распределение этого тонуса в зависимости от положения и движения тела. Красное ядро тесно связано с ретикулярной системой ствола мозга и с корой больших полушарий. К красным ядрам подходят нервные пути от подкорковых ядер, мозжечка, коры больших полушарий. От клеток красных ядер идет путь к мотонейронам спинного мозга. Животное, у которого сохранены спинной, продолговатый и средний мозг, способно нормально распределять мышечный тонус, сохранять и восстанавливать нормальную позу. Это обусловлено в основном работой красного ядра и ретикулярной системы. Распределение мышечного тонуса и обеспечение равновесия тела осуществляются рефлекторным путем.
Билет11
Регуляция питьевого поведения.
Питьевое поведение включает процесс поиска, добывания воды и сам процесс питья. Данный вид поведения определяется недостатком воды или избытком солей, точнее, повышением осматического давления внутренней среды организма. Жажда возникает также при гиповолюмии, при нормальном осмотическом давлении. Например, при значительной потере крови формируется специфическая мотивация, т.е. ощущение жажды.
Повышение осмотического давления жидкостей организма воспринимается специальными рецепторами, локализующихся в различных органах и в ЦНС- осморецепторами. Осмотическое давление- один из жёстких показателе организма, коорый регулируется весьма точно. Отклонения его параметров от нормы опасно для жизни, т.к. при этом нарушается обмен веществ.
Количество воды и солей регулируется посредством изменения объёма выведения их из организма: при избыточном количестве они выводятся в большом количестве, при недостатке соли и воды задерживаются в организме. В частности, антидиуретический гормон (АДГ), вырабатываемый в ядрах гипоталамуса, уменьшается от выведения воды, если её недостаток в крови при этом вырабатывается больше АДГ, вода задерживается в организме- почки меньше выделяют воды.
Центр питьевой потребности: параветрикулярные и супраоптические ядра. Здесь находятся осморецепторы клетки, реагирующие на содержание NaCl в крови (идеально около 0,7 %). При росте концентрации NaCl – выделение вазопрессина (экономия воды на уровне почек) и чувство жажды ( запуск соответствующих поведенческих реакций).
Осморецепторы располагаются также в тканях и кровеносных сосудах печени, почек, селезёнки, сердца и др. часть осморецепторов регистрируют не общее осмотическое давление жидкости, а концентрацию каких-то ионов. Волюморецепторы (барорецепторы низкого давления) расположены в предсердиях, правом желудочке, полых и других крупных венах вблизи сердца. Импульсы от волюморецепторов поступают в ЦНС по афферентным волокнам блуждающего нерва. Импульсация в ЦНС по блуждающим нервам возрастает, выработка АДГ тормозится, воды выводится больше, при уменьшении объема жидкости возникают противоположные реакции и соответствующие изменения диуреза (АДГ уменьшает диурез).
Нейроны супраоптических и паравентрикулярных ядер гипоталамуса тесно связаны своими отростками с другими нейронами лимбико-ретикулярных отделов мозга и с корой большого мозга. Возникающее в них возбуждение посредством восходящих активирующих влияний широко распространяется по структурам мозга, включая субкомиссуральный орган, прозрачную перегородку, миндалевидный комплекс, бледный шар, кору большого мозга. Благодаря этому гипоталамические нейроны держат в функциональной зависимости от своего состоянии другие отделы мозга. При возбуждении этих нейронов гиперосмолярной кровью формируются ощущение жажды и мотивация, определяющая поиск и прием воды, а при возбуждении гипоосмолярной кровью возникает ощущение, определяющее поиск и употребление соли, солевая мотивация.
В регуляции объёма циркулирующейжидкости принимает также участие ренин-ангиотензин-альдостероновая система. Ренин-ангиотензин-альдостероновая система осуществляет регуляцию сосудистого тонуса и объёма циркулирующей крови (соответстенно, артериального давления). Регуляция артериального давления осуществляется в почке путём синтеза ренина. Ангиотензин способствует задержке соли и воды почками главным образом двумя путями :
Непосредственно влияет на почки, вызывая задержку соли и воды
Стимулирует секрецию альдостерона надпочечниками.
Альдостерон, в свою очередь, увеличивает реабсорбцию соли и воды в почечных канальцах.
Медиатор ацетилхолин (Ацх). Роль Ацх в вегетативной и центральной нервной системе.
Ацетилхолин (лат. Acetylcholinum) — нейромедиатор, осуществляющий нервно-мышечную передачу, а также основной нейромедиатор впарасимпатической нервной системе. Четвертичное аммониевое основание.
В организме очень быстро разрушается специализированнымферментом — ацетилхолинэстеразой.
