
- •Введение
- •1.1.Теоретичиские основы процесса
- •Основные параметры и их влияние на процесс
- •1.2. Характеристика сырья и продуктов
- •1.3. Технологическая схема процесса.
- •1.4. Общий материальный баланс установки.
- •Материальный баланс установки
- •2. Расчётная часть.
- •2.1. Расчёт реактора.
- •Материальный баланс.
- •Количество циркулирующего катализатора и расход водяного пара.
- •Тепловой баланс реактора.
- •Левая часть уравнения отвечает приходу тепла (в кВт):
- •Правая часть уравнения отвечает расходу тепла (в кВт):
- •Из теплового баланса реактора определим температуру сырья при подаче его в узел смешения с катализатором.
- •5. Размеры реактора.
- •Катализатора на выходе из десорбера.
- •Выбор распределительного устройства парокатализаторного потока в реакторе.
- •2.2. Расчёт трубчатой печи.
- •1. Расчёт процесса горения.
- •2. К.П.Д. Печи, её тепловая нагрузка и расход топлива.
- •3. Поверхность нагрева радиантных труб и размеры камеры радиации (топка).
- •4. Расчёт конвективной поверхности нагрева печи.
- •2.3 Расчет сепаратора.
- •2.4. Расчёт холодильника.
- •1. Уравнение теплового баланса:
- •2. Расчет плотностей теплообменивающихся сред:
- •9. Поверхность одной трубы.
- •Список литературы
2.2. Расчёт трубчатой печи.
Для установки каталитического крекинга наиболее эффективными являются трубчатая печь беспламенного горения с излучающими стенами
Исходные данные для расчёта.
Состав топлива печи:
СН4 – 98%;
С2Н6 – 0,3%;
С3Н8 – 0,2%;
н-С4Н10 – 0,1%;
СО2 – 0,3%;
N2 – 1,1%.
Производительность установки по сырью – Gс = 650 тыс т/год = 81000кг/ч.
Температура входа сырья – 200 0С = 473 К.
Температура выхода сырья – 240 0С = 513К.
Плотность сырья – 0,9074 г/см3.
е = 0 (массовая доля отгона при t=350 0С).
Давление – 200000 Па.
Плотность газа – 0,730 кг/м3 (при нормальных условиях)
1. Расчёт процесса горения.
Для начала пересчитаем состав топлива в % масс. следующим образом:
xi= (Мi * xi) * 100%/ ∑(Мi * xi) , где
xi – массовая доля;
x’i – массовая доля;
Мi –молекулярная масса.
∑(Мi * xi) =16,36;
x![]() =
(16
* 0,98) *100%/ 16,36 =95,84%;
=
(16
* 0,98) *100%/ 16,36 =95,84%;
x![]() =
(30
* 0,003) *100%/ 16,36 =0,55%;
=
(30
* 0,003) *100%/ 16,36 =0,55%;
x![]() =
(44
* 0,002) *100%/ 16,36 =0,54%;
=
(44
* 0,002) *100%/ 16,36 =0,54%;
x![]() =
(58
* 0,001) *100%/ 16,36 =0,35%;
=
(58
* 0,001) *100%/ 16,36 =0,35%;
x![]() =
(44
* 0,003) *100%/ 16,36 =0,84%;
=
(44
* 0,003) *100%/ 16,36 =0,84%;
x![]() =
(28 * 0,011) *100%/
16,36 =1,88%.
=
(28 * 0,011) *100%/
16,36 =1,88%.
Результаты пересчёта сведены в таблице 1.16.
Таблица 1.16.
-
Компоненты
Молекулярная
Масса
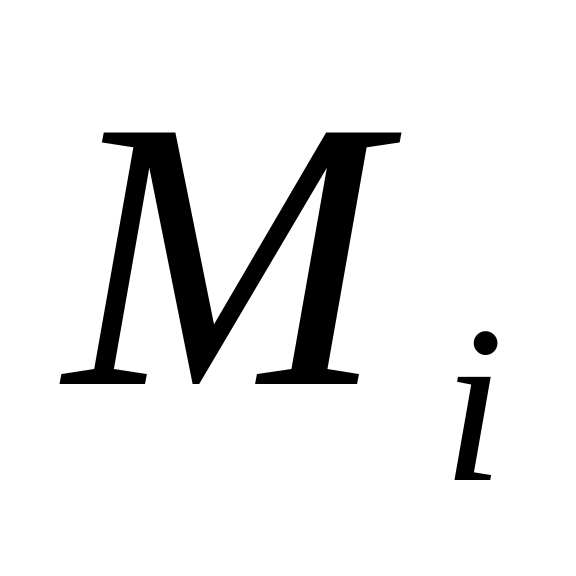
Мольная
(объёмная) доля

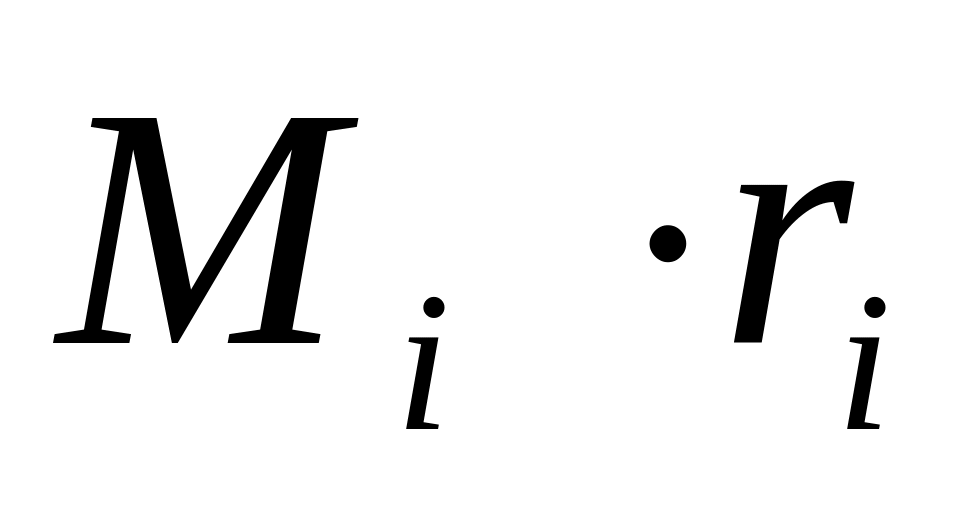
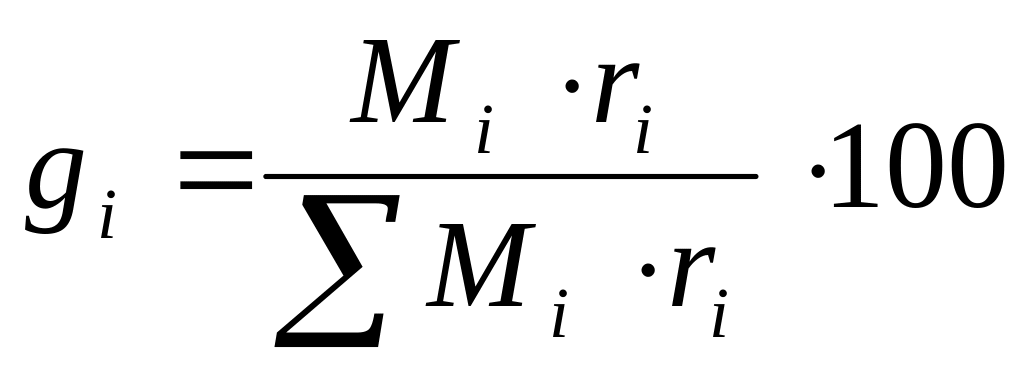
СН4
16
0,980
15,680
95,84
С2Н6
30
0,003
0,090
0,55
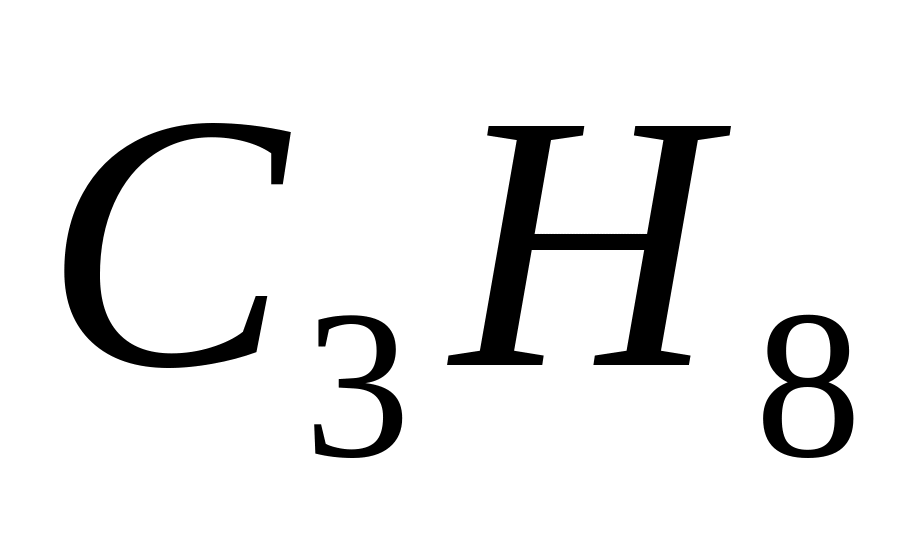
44
0,002
0,088
0,54
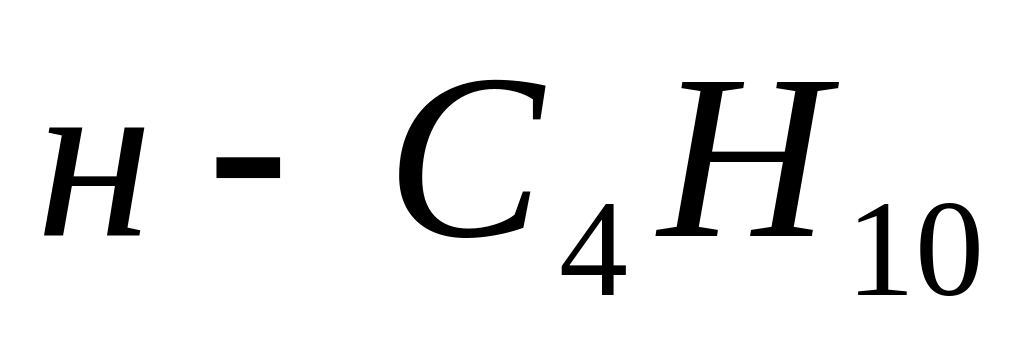
58
0,001
0,058
0,35
СО2
44
0,003
0,132
0,84
N2
28
0,011
0,308
1,88
Сумма:
−
1,000
16,36
100,0
Определим теплоту сгорания без учёта конденсации паров:
Q
![]() =360,33
*
СН4+631,8*С2Н6+913,8*С3Н8+1195,0*н-С4Н10
=360,33
*
СН4+631,8*С2Н6+913,8*С3Н8+1195,0*н-С4Н10
где
![]()
![]() и т.д. – содержание соответствующих
компонентов в топливе, объёмн. %.
и т.д. – содержание соответствующих
компонентов в топливе, объёмн. %.
Q =360,33*98+631,8*0,3+913,8*0,2+1195,0*0,1=35800кДж/м3
или
Q = 35800/0,730 = 49040 кдж/кг
Определяем элементарный состав топлива в массовых процентах.
Содержание углерода:
С=∑Сi=∑[gi*12*ni/Mi]=(95,84*12*1/16)+(0,55*12*2/30)+(0,54*12*3/44)+(0,35*12*4/58)+(0,84*12*1/44)=73,3% (ni – число атомов углерода в данном компоненте)
Содержание водорода:
Н=∑Нi=∑[gi*mi/Mi]=(95,84*4/16)+(0,55*6/30)+(0,54*8/44)+(0,35*1/58)=24,23% (mi – число атомов водорода в данном компоненте)
Содержание кислорода:
О=gСО2*16*Р/МСО2 = 0,84*16*2/44=0,61% (Р – число атомов кислорода в молекуле углекислого газа)
Содержание азота:
N= gN2*14*K/МN2=1,88*14*2/28=1,88% (К – число атомов азота в молекуле газа)
Проверка:
С+H+O+N=73,3%+24,23%+0,61%+1,88%=100%
Определяем теоретическое количество воздуха, необходимое для сжигания 1 кг газа, по формуле:
L0 = (0,0267 * С+ 0,08 * Н+ 0,01 [S–О] ) / 0,23= =(0,0267*73,3+0,08*24,23+0,01[0-0,61])/0,23=16,94 кг/кг
Для печей с излучающими стенками коэффициент избытка воздуха α=1,03÷1,07. Принимаем α=1,06. Тогда действительное количество воздуха:
LД= α*L0=1,06*16,94=17,96
или
LД/ρВ=17,96/1,293=13,89 м3/кг
где
![]() кг/м3
– плотность воздуха при нормальных
условиях (273 К и 0,1∙106
Па).
кг/м3
– плотность воздуха при нормальных
условиях (273 К и 0,1∙106
Па).
Определим количество продуктов сгорания, образующихся при сжигании 1 кг топлива:
mCO=0,0367*С = 0,0367*73,3=2,69 кг/кг
mН2О=0,09*Н=0,09*24,23=2,18кг/кг
mО=0,23L0*(α-1)=0,23*16,94*(1,06-1)=0,23 кг/кг
mN2=0,77*L0*α+0,01*N=0,77*16,94*1,06+0,01*1,88=13,84кг/кг
Суммарное количество продуктов сгорания:
∑mi=2,69+2,18+0,23+13,84=18,94кг/кг
Проверка:
∑mi=1+α*L0=1+1,06*16,94=18,95кг/кг
Содержанием влаги в воздухе пренебрегаем.
Найдём объёмное количество продуктов сгорания (в м3) на 1 кг топлива (при нормальных условиях):
VСО2=mCО2*22,4/МСО2=2,69*22,4/44=1,37м3/кг
VН2О=mН2О*22,4/МН2О=2,18*22,4/18=2,71м3/кг
VО2=mО2*22,4/МО2=0,23*22,4/32=0,16м3/кг
VN2=mN2*22,4/МN2=13,84*22,4/28=11,07м3/кг
Суммарный объём сгорания:
ΣVi=1,37+2,71+0,16+11,07=15,31м3/кг
Плотность продуктов сгорания при 273 К и 0,1∙106 Па:
ρ0=Σmi /ΣV=18,95/15,31=1,24кг/м3
Определим энтальпию продуктов сгорания на 1 кг топлива при различных температурах по уравнению:
qT=(Т-273)*(mCО2*сСО2+mН2О*сН2О+mО2*сО2+mN2*сN2),
где Т –
температура продуктов сгорания, К;
![]() − средние массовые теплоёмкости
продуктов сгорания, определяемые из
таблицы, кДж/(кг∙К).
− средние массовые теплоёмкости
продуктов сгорания, определяемые из
таблицы, кДж/(кг∙К).
q273=0;
q300=(300-273)*(2,69*0,8286+2,18*1,8632+0,23*0,8452+ +13,84*0,9326)=561 кДж/кг
q500= (500-273) *(2,69 * 0,9207+ 2,18 * 1,9004+ 0,23 * 0,9391+13,84*1,0362)=4807 кДж/кг
q700= (700-273) *(2,69 * 0,9906+ 2,18 * 1,9557+ 0,23 * 1,0104+13,84*1,1149)=9260 кДж/кг
q1100= (1100-273) *(2,69 * 1,0902+ 2,18 * 2,0847+ 0,23 * *1,1119+13,84*1,2269)=18837 кДж/кг
Результаты сведены в таблице 1.17.
-
Т, К
273
300
500
700
1100
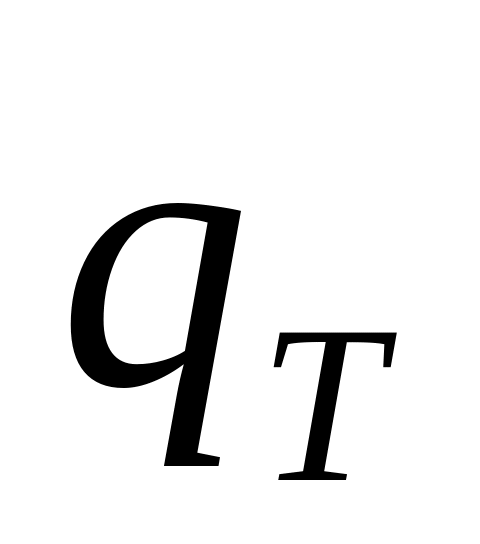 ,
кДж/кг
,
кДж/кг0
561
4807
9260
18837
П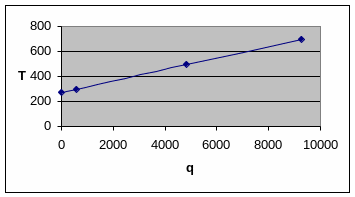 о
данным этой таблицы строим график q –
T
о
данным этой таблицы строим график q –
T
