
- •2.Физико-химические свойства углеводородосодержащих веществ и методы их расчета
- •2.1. Контроль качества нефтей
- •2.2. Классификация нефтей
- •2.3. Плотность и молекулярная масса
- •2.4. Вязкость нефтей и нефтепродуктов
- •2.5. Особенности свойств нефтеконденсатных смесей
- •Температура, с
- •2.6. Фазовые состояния углеводородных систем при изменении давления и температуры
- •2.6.1. Критические параметры углеводородов
- •Давление
- •2.6.2. Давление насыщенных паров
- •2.7. Теплофизические свойства нефти и нефтепродуктов в процессах тепломассопереноса
2.3. Плотность и молекулярная масса
Плотностью называется количество покоящейся массы в единице объема. Определение плотности нефти и нефтепродуктов весьма облегчает возможные расчеты, связанные с расчетом их массового количества. Учет количества нефти и нефтепродуктов в объемных единицах вызывает некоторые неудобства, т. к. объем жидкости меняется с изменением температуры. Плотность имеет размерность кг/м3. Поэтому, зная объем и плотность, при приеме, отпуске и учете нефти и нефтепродуктов можно выражать их количество в массовых единицах, т. к. масса не зависит от температуры.
На практике часто имеют дело с относительной плотностью нефти и нефтепродукта, которая определяется отношением их массы при температуре определения к массе чистой воды при +4С, взятой в том же объема. Плотность воды при +4С имеет наибольшее значение и равна 1000 кг/м3. Относительную плотность принято определять при +20С, что обозначается символом ρот. Относительная плотность нефтей и нефтепродуктов при +20С колеблется в пределах от 0,7 до 1,07.
У
(2.4)![]()
где – плотность вещества, кг/м; g – ускорение силы тяжести.
С
(2.5)
![]()
где – поправка на изменение плотности при изменении температуры на 1С; 20 – плотность нефти или нефтепродукта при t = +20С.
Значения ρ некоторых простых углеводородов приведены в табл. 2.3. Плотность нефтей и нефтепродуктов для практических измерений считается аддитивной величиной.
П
48
г
(2.6)![]()
![]() На
практике плотность нефтепродуктов,
нефтей и их смесей определяют
ареометрическим, пикнометрическим
способом или взвешиванием, например,
на весах Вестфаля-Мора (см. рис. 2.2.).
На
практике плотность нефтепродуктов,
нефтей и их смесей определяют
ареометрическим, пикнометрическим
способом или взвешиванием, например,
на весах Вестфаля-Мора (см. рис. 2.2.).
Плотность газа можно определить из соотношения молекулярной массы, выраженной в килограмм-молекулах (кмоль), к общему объему одной килограмм-молекулы, который согласно закону Авогадро составляет 22,412 м3:
![]()
Из закона Авогадро также следует, что плотности газов относятся между собой, как их молекулярные массы.
Рис. 2.2. 1)
Стандартный нефтяной ареометр 2)
Весы Вестфаля-Мора.
1)
2)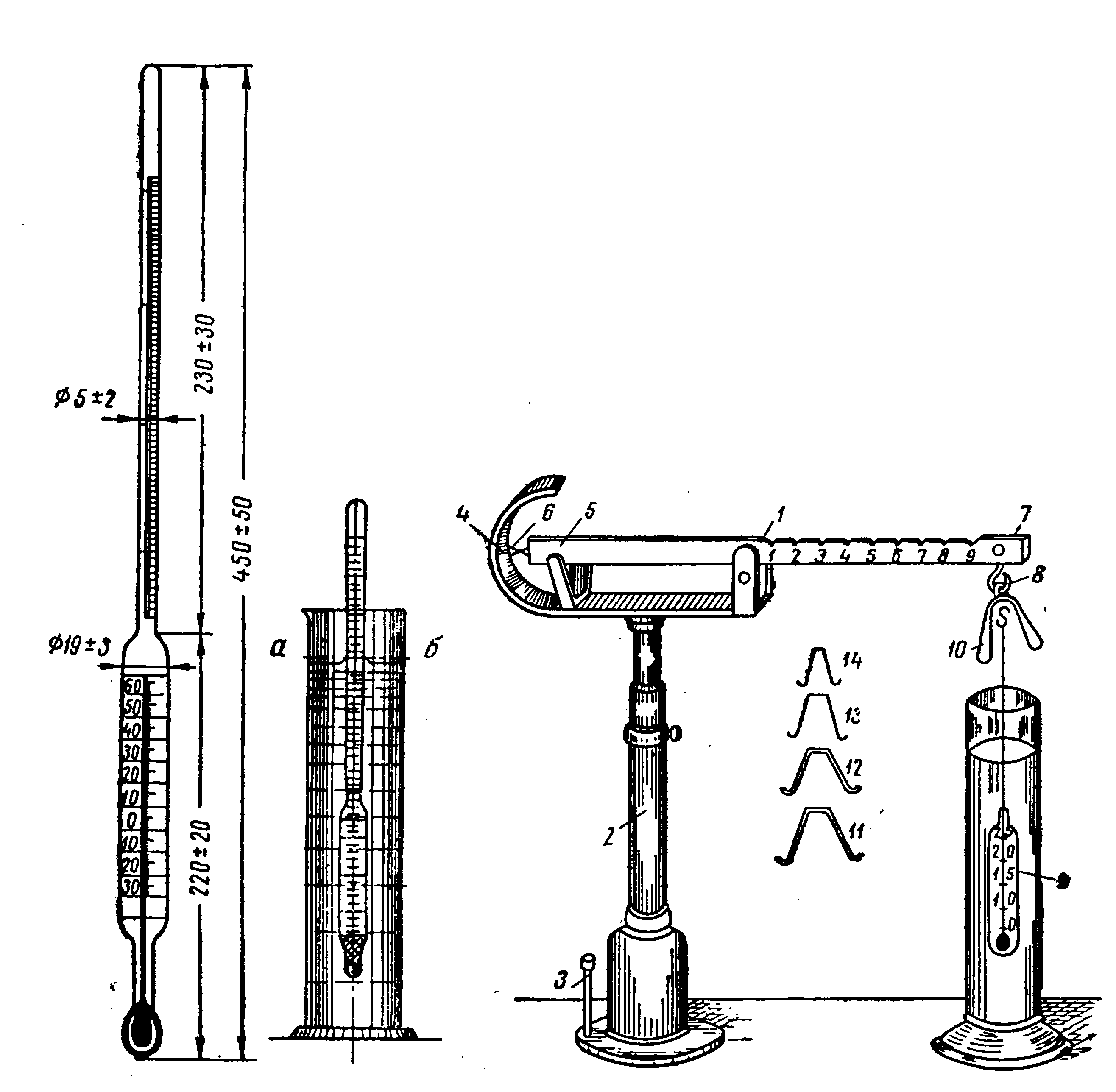
1 – коромысло; 2 – неподвижный штатив; 3 – регулировочный винт; 46 – неподвижное острие; 57 – левое и правое плечо; 9 – поплавок; 1014 – разновесы-рейтеры
О
49
![]()
Значения ρ и ρОТН некоторых простых углеводородов приведены в табл. 2.4 Важность данной характеристики особенно подчеркивается в условиях эксплуатации различного оборудования. Так, например, при утечках в помещениях газы с ОТН < 1 распространяются прежде всего в верхней зоне помещения, а газы с ОТН > 1 (например сжиженные) попадают в каналы, подвалы и т.п. Плотность смеси газов также подчиняется закону аддитивности.
Таблица 2.4
Плотность чистых углеводородов
Углево-дород |
Плотность при температуре, С |
|||||||||
-10 |
-5 |
0 |
5 |
10 |
15 |
20 |
30 |
40 |
50 |
|
СН4 |
329,1 |
317,3 |
303,3 |
297,0 |
287,7 |
278,8 |
270,2 |
- |
- |
- |
С2Н5 |
441,6 |
431,5 |
420,9 |
403,2 |
395,4 |
381,5 |
364,4 |
- |
- |
- |
С3Н8 |
545,4 |
539,0 |
532,6 |
526,0 |
519,2 |
512,3 |
505,1 |
485,5 |
468,9 |
451,3 |
n-С4Н10 |
611,9 |
505,5 |
501,0 |
595,3 |
589,9 |
584,3 |
578,6 |
557,3 |
565,2 |
542,6 |
i-С4Н10 |
592,6 |
585,8 |
581,0 |
575,1 |
539,1 |
553,1 |
553,9 |
544,8 |
591,8 |
518,2 |
n-С5Н12 |
554,8 |
630,0 |
645,2 |
670,3 |
635,4 |
530,5 |
625,7 |
615,3 |
506,2 |
595,4 |
С5Н12 |
650,9 |
647,9 |
642,1 |
633,8 |
630,8 |
625,5 |
620,4 |
615,0 |
512,4 |
609,4 |
С6Н14 |
585,0 |
580,5 |
676,1 |
671,7 |
657,2 |
662,7 |
658,1 |
650,0 |
640,9 |
631,5 |
С7Н16 |
706,9 |
702,7 |
698,5 |
694,4 |
690,2 |
686,0 |
681,7 |
675,8 |
673,1 |
670,2 |
С9Н18 |
724,0 |
720,1 |
716,1 |
712,2 |
708,2 |
704,2 |
700,2 |
696,2 |
690,8 |
687,1 |
С9Н20 |
741,2 |
737,5 |
735,8 |
730,1 |
723,3 |
722,6 |
718,9 |
714,0 |
710,1 |
705,2 |
С10Н22 |
719,3 |
745,6 |
742,0 |
738,4 |
734,7 |
731,1 |
727,4 |
723,2 |
718,8 |
715,9 |
Плотность большинства нефтей (в том числе северных месторождений Тюменской области (СРТО), (см. табл. 2.5. и 2.6), исследованных в ТюмГНГУ, находится в пределах 825÷900 кг/м3.
Н
50
Таблица 2.5
Физико-химические свойства нефтей
Месторождение нефти |
Плотность при 20С, кг/м3 |
Кинематическая вязкость, сСт, при: |
Температура, С |
||
t=20С |
t=50C |
застывания |
кипения |
||
Ромашкинское |
862 |
14,22 |
5,9 |
- |
+65 |
Туймазинское |
852 |
7,072 |
3,24 |
-59 |
- |
Мухановское |
840 |
7,65 |
3,46 |
-8 |
- |
Узеньское |
860 |
при t=40 24,0 |
11,18 |
+31 |
+77 |
Трехозерное |
848 |
9,75 |
2,98 |
- |
+85,5 |
Тетерево-Мартымьинское |
825 |
4,12 |
2,17 |
- |
+61 |
Правдинское |
854 |
10,76 |
4,75 |
- |
+72 |
Салымское |
826 |
4,54 |
2,17 |
ниже -16 |
+50 |
Южно-Балыкское |
868 |
16,58 |
8,53 |
- |
+81 |
Мамонтовское |
878 |
21,51 |
8,15 |
- |
+90 |
Усть-Балыкское |
874 |
17,48 |
8,37 |
- |
+71,7 |
Лянторское |
887 |
16,14 |
7,11 |
- |
+80 |
Зап.-Сургутское |
885 |
41,60 |
12,11 |
- |
+84 |
Холмогорское |
860 |
7,83 |
3,53 |
- |
+64 |
Покачаевское |
865 |
5,52 |
3,88 |
-9 |
+79 |
Мегионское |
850 |
7,82 |
3,56 |
- |
+77 |
Советское |
852 |
6,13 |
3,41 |
- |
+62 |
Самотлорское |
851 |
4,94 |
2,49 |
- |
+59 |
Варьеганское |
832 |
4,37 |
1,78 |
-1 |
+32 |
Первомайское |
844 |
4,30 |
2,14 |
ниже –16 |
+57 |
П
51
Проведенные
в ТюмГНГУ экспериментальные исследования
испаряющихся нефтей, показывают, что
при одном и том же уровне
потерь плотность нефти будет зависеть
от скорости испарения и от доли потерь
легкой фракции.
Скорость испарения нефти определяется
также (как установлено выше) температурой
tН, скоростью
ветра
![]() В,
продолжительностью испарения τ и
высотой взлива hВЗ.
В,
продолжительностью испарения τ и
высотой взлива hВЗ.
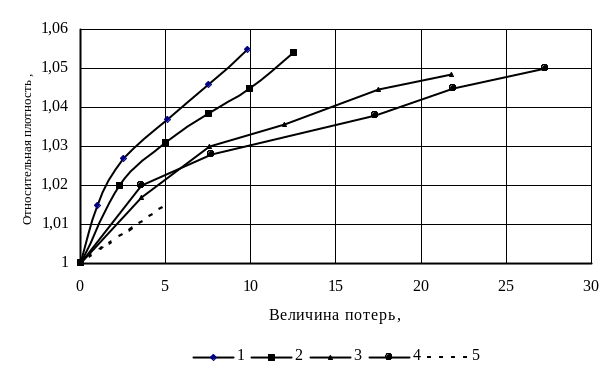
1
2
3
4
5
%
Рис.2.3. Зависимость относительной плотности нефти
от величины потерь, %
Многочисленные экспериментальные данные (более 400) по изменению плотности нефтей были обработаны также методом наименьших квадратов, и в результате была получена аналогичная эмпирическая зависимость
![]() (2.7)
(2.7)
г
52
Т
53
Следует отметить высокое значение коэффициента множественной корреляции R = 0,97 для полученных зависимостей. Поэтому они могут быть использованы для определения плотности нефтей после потери при испарения доли нефти 0,29 0,56.
жидкие углеводороды отличаются по физико-химическим свойствам и, естественно, что методы их определения также различны. При проведении исследований (ВНИИгаз, СибНИИНП, ТюмНИИГИПРОгаз, ВНИИНП, БашНИИНП и др.) обычно используют стандартизированные установки, приборы и методики, применяемые в производстве.
Очевидно, что в зависимости от состава изменяются и свойства конденсата. На рис. 2.4 показана зависимость плотности от температуры различных конденсатов Уренгойского месторождения.
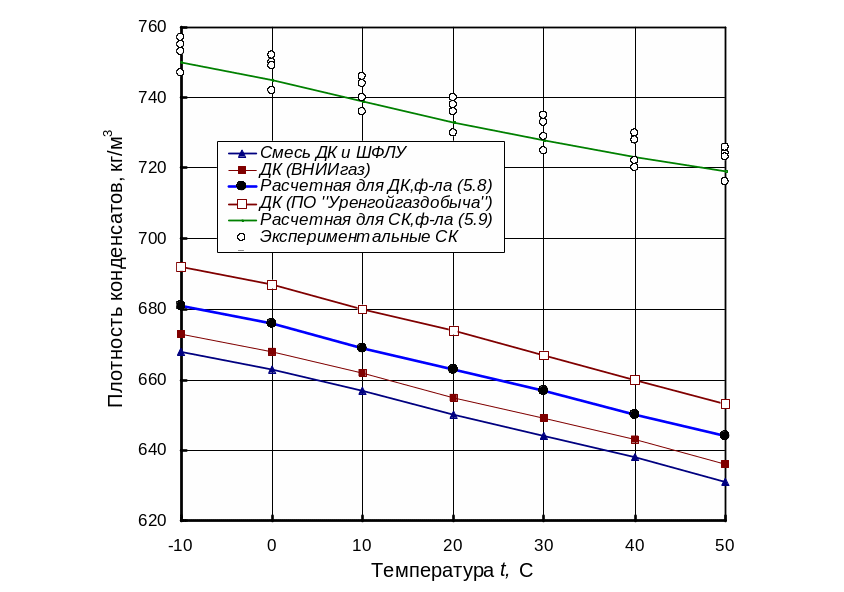
Рис. 2.4. Зависимость плотности конденсатов от температуры
54
З
(2.8)![]()
где t и 20 – плотность при t = 20С, кг/м3,
а
(2.9)![]()
Состав жидкой смеси (конденсата) характеризуется массовыми или молярными концентрациями входящих в нее индивидуальных углеводородов.
П
(2.10)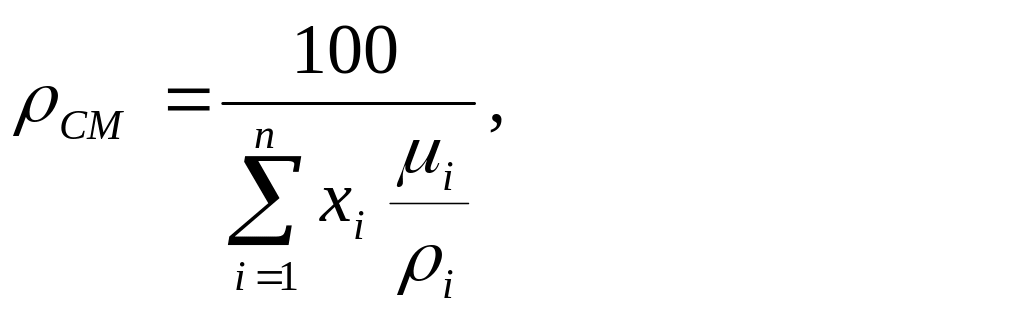
е
(2.11)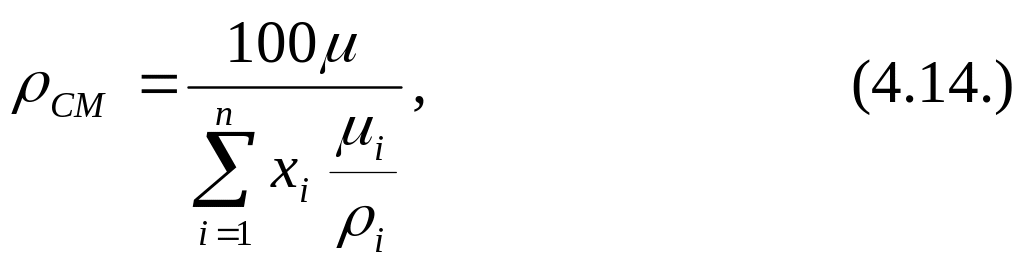
где
![]() – молекулярная масса конденсата;
i,
i
– молекулярные массы и плотности
индивидуальных компонентов.
– молекулярная масса конденсата;
i,
i
– молекулярные массы и плотности
индивидуальных компонентов.
Однако формулами (2.10÷2.11) можно воспользоваться при наличии информации о концентрациях всех входящих в смесь углеводородов. На практике же, как правило, состав определяется полностью, а до бутана (С4Н10) или, в лучшем случае, до гексана (С6Н14) включительно, а все остальные компоненты объединяются в остаток (или псевдокомпонент) С5+В (или С7+В). Решение проблемы осложняется еще и тем обстоятельством, что, как показывает анализ данных, не только различаются по составу разные конденсаты, но с течением времени меняется состав одного и того же конденсата.
С
(2.12)
где Gi
= хi
i.
55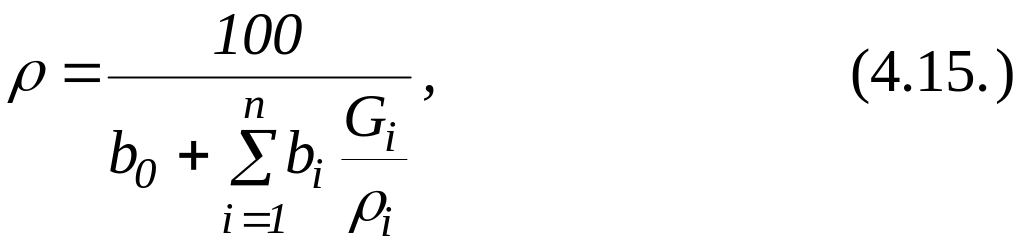
С учетом найденных коэффициентов искомую зависимость можно представить в следующем виде:
(2.13)
![]()
Все расчеты были проведены на ЭВМ с помощью специально составленной программы. Полученное уравнение адекватно описывает эксперимент.
В качестве примера на рис. 2.5 приведены графические корреляционные зависимости плотности конденсатов различных месторождений от температуры кипения.
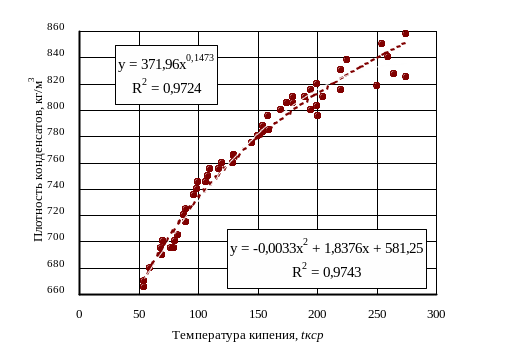
Рис.2.5. Зависимость плотности конденсатов от средней
температуры кипения
56
С
(2.14)![]()
где tНК, tСРК, tКК – температуры начала, середины и конца кипения соответственно, С; a, b – эмпирические коэффициенты, позволяют рассчитывать плотности различных фракций конденсата. Причем отмечено, что чем уже фракция по температуре кипения, тем меньше ошибка расчета, хотя и максимальная погрешность, как правило, не превышает 5%.
Из представленной табл. 2.7 видно, что легкие фракции с одинаковыми интервалами кипения имеют примерно одинаковую молекулярную массу. С увеличением температуры кипения фракций увеличивается и разница в молекулярных массах.
на практике в отношении нефти и ее фракций часто пользуются термином молекулярная масса, опуская слово «средняя», причем у нефтяных фракций она увеличивается по мере возрастания температуры кипения.
Таблица 2.7
Молекулярная масса нефтяных фракций
Показатель |
Температура начала кипения, tНК |
||||||
50÷100 |
101÷150 |
151÷200 |
201÷250 |
251÷300 |
301÷350 |
351÷400 |
|
Молекулярная масса, |
90 |
110 |
130 |
155 |
187 |
220 |
260 |
Зная среднюю температуру кипения фракций (или данные о плотности и вязкости продукта) в ряде случаев представляется возможным определить абсолютные значения .
Е![]() сли
известна средняя температура кипения
нефтяных фракций, то молекулярную массу
можно вычислить по уравнению Б.П.
Войнова:
сли
известна средняя температура кипения
нефтяных фракций, то молекулярную массу
можно вычислить по уравнению Б.П.
Войнова:
где tК – средняя температура кипения фракции, рассчитанная как среднеарифметическая от температур, при которых перегоняются одинаковые объемы продукта.
С
(2.15)![]()
где ρ20 – плотность нефти при 20С кг/м3.
Д![]() ля
арланских высокосернистых нефтей и ее
фракций Креймер Л.М. предлагает зависимость
следующего вида:
ля
арланских высокосернистых нефтей и ее
фракций Креймер Л.М. предлагает зависимость
следующего вида:
г
57
Теоретически молекулярная масса смеси аддитивно складывается из молекулярных масс отдельных компонентов. Однако для этого необходимо знать молярные (объемные) концентрации всех компонентов, входящих в данную смесь. Последнее, как уже указывалось выше, на практике не всегда возможно. Кроме того, как в стабильном, так и в деэтанизированном конденсате практически всегда находятся углеводородные газы, которые «смазывают» законы, полученные для чистых веществ, существенно изменяя такие параметры, как давление насыщенных паров, вязкость и температуру начала кипения. Вероятно, этим можно объяснить разброс экспериментальных значений и рассчитанных по формулам.
В ТюмГНГУ в результате анализа на ЭВМ, данных пассивных и активных экспериментов (всего около 500) получены математические модели, позволяющие по известной плотности смеси определить молекулярную массу газового конденсата.
Д
(2.16)![]()
(2.17)![]() для
СК ( ρ
740800 кг/м3 )
для
СК ( ρ
740800 кг/м3 )
Отклонения экспериментальных данных от расчетных по формулам (2.16÷2.17) можно проследить по графикам рис. 2.6.
(2.18)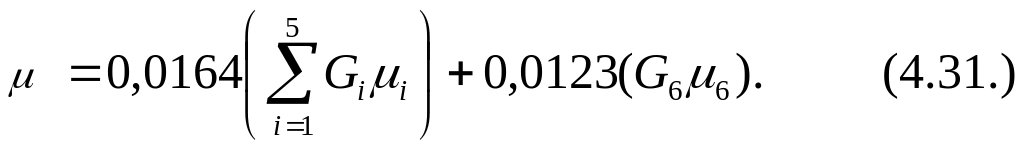
где i – молекулярные массы индивидуальных углеводородов;
Gi – процентное содержание индивидуальных углеводородов в смеси.
По данным статистического анализа модель удовлетворительно описывает эксперимент с коэффициентом множественной коррекции R = 0,98 и может быть использована в инженерных расчетах.
58
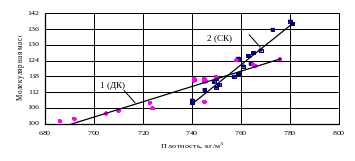
Рис. 2.6. Зависимость молекулярной массы конденсата от плотности
– для деэтанизированного (ДК); – для стабильного(СК) конденсата;
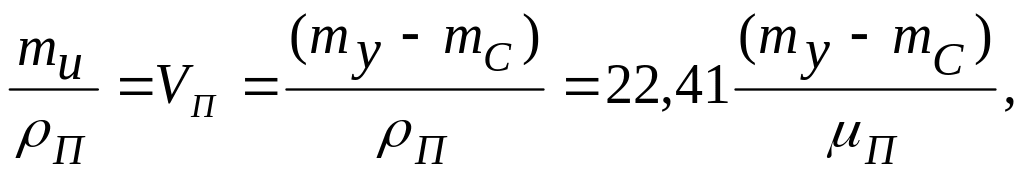 На
простом примере покажем простоту
механизма использования рассмотренного
показателя
.
Допустим, при аварийно-восстановительных
работах была допущена утечка нефтепродукта
массой mу,
собранной оказалась часть mС.
Молекулярная масса паров углеводородов,
испарившихся с поверхности –
П.
Согласно этим исходным данным
представляется возможным определить
объем паров VП,
испарившихся с поверхности жидкого
углеводорода (при нормальных условиях),
используя например, закон Авогадро:
На
простом примере покажем простоту
механизма использования рассмотренного
показателя
.
Допустим, при аварийно-восстановительных
работах была допущена утечка нефтепродукта
массой mу,
собранной оказалась часть mС.
Молекулярная масса паров углеводородов,
испарившихся с поверхности –
П.
Согласно этим исходным данным
представляется возможным определить
объем паров VП,
испарившихся с поверхности жидкого
углеводорода (при нормальных условиях),
используя например, закон Авогадро:
где П – молекулярная масса паров углеводорода; ρП – плотность паров при рат и 273С; mи – масса испарившейся части.
