
- •Глава 1.Взаимодействие биополимеров с лигандами и между собой
- •1.1.Термодинамика взаимодействия биополимеров с лигандами
- •1.1.1.Взаимодействие биополимеров с недостатком лиганда
- •1.1.2.Взаимодействие биополимера с избытком лиганда
- •1.1.3.«Направленные» конформационные переходы
- •1.1.4.Кооперативное связывание лигандов
- •1.2.Биологическое «узнавание»
Глава 1.Взаимодействие биополимеров с лигандами и между собой
Практически все процессы в живой клетке начинаются с взаимодействия биополимеров с низкомолекулярными лигандами или с взаимодействия биополимеров друг с другом. Образование комплекса является сигналом к последующему биохимическому действию — ответу системы. Так, взаимодействие фермента с субстратом (образование фермент-субстратного комплекса) приводит к превращению субстрата в продукты реакции, а узнавание гормона рецептором — к протеканию определенных внутриклеточных процессов. В подавляющем большинстве случаев экспериментально удается регистрировать именно этот «ответ» системы. Как правило, взаимодействие специфического лиганда с биополимером не сопряжено с преодолением существенных энергетических барьеров и является быстрым процессом. Поэтому исследователи имеют дело с равновесными процессами, требующими термодинамического подхода. Ниже мы рассмотрим некоторые простые случаи взаимодействия биополимеров с лигандами.
1.1.Термодинамика взаимодействия биополимеров с лигандами
Как уже было сказано выше, в большинстве случаев не удается измерить концентрации всех компонентов равновесия. Как правило, известны начальные концентрации биополимера и лиганда и отклик («ответ») биологической системы. Константы равновесия, рассчитанные из этих данных, являются эффективными (кажущимися) и их физический смысл изначально не определен. Придать им физический смысл можно лишь в рамках определенной термодинамической модели
Ниже мы рассмотрим некоторые простые термодинамические модели, широко используемые для описания взаимодействия биополимеров с лигандами.
1.1.1.Взаимодействие биополимеров с недостатком лиганда
Одно место связывания
В некоторых особых случаях (например, при взаимодействии с ДНК или олигонуклеотидами интеркалирующих1 красителей) вследствие существенного отличия физических свойств связанного и несвязанного лигандов удается экспериментально измерить концентрацию связанного лиганда [Lb], а. Следовательно, и концентрацию не прореагировавшего, свободного лиганда [Lf] ([Lf] = [L]o – [Lb], где [L]o — исходная концентрация лиганда). Такой случай описывается, как правило, с помощью модели Скетчарда.
![]()

( 4.0)
где P — биополимер, а PL — его комплекс с лигандом.
Константа равновесия
![]()
( 4.0)
Учитывая, что [PL] = [Lb], а [P] = [P]o – [PL] = [P]o – [Lb], получим:
Рис.
4.1. Кривая
связывания лиганда биополимером,
имеющим одно место связывания. Кружки
— экспериментальные данные, сплошная
кривая — результат нелинейной регрессии
(фиттинга) этих данных по уравнению ( 4 .0)
При повышение концентрации лиганда
[Lb]
асимптотически приближается к [P]o
(насыщение всех мест связывания).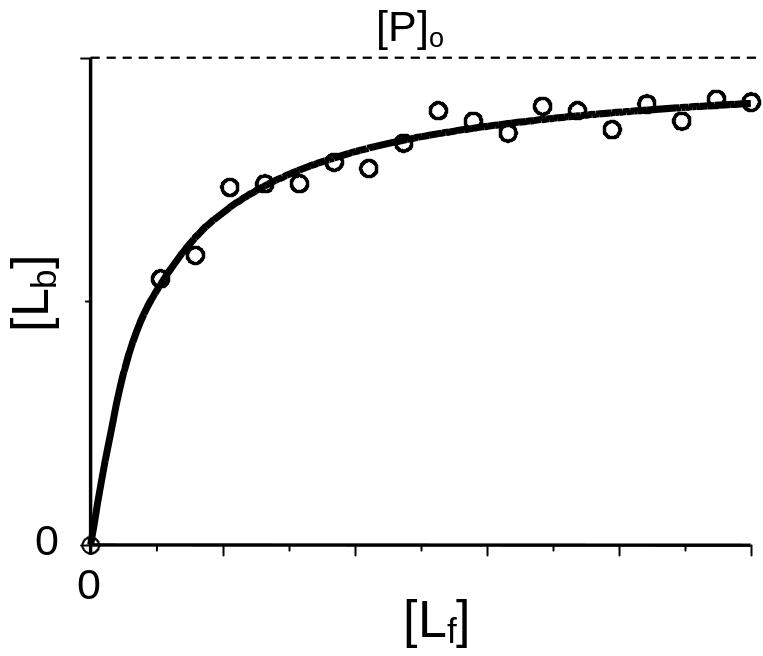
![]()
( 4.0)
![]()
( 4.0)
Уравнение ( 4 .0) представляет собой гиперболическую зависимость, проходящую через начало координат (Рис. 4 .1). При повышении концентрации лиганда концентрация связанного лиганда асимптотически стремится к [P]o.
На практике для анализа связывания чаще используют линейную анаморфозу уравнения ( 4 .0):
![]()
( 4.0)
принято называть уравнением Скетчарда. В случае биополимера с одним местом связывания уравнение Скетчарда дает прямую линию, тангенс угла наклона которой равен –K (Рис. 4 .2).
N одинаковых независимых мест связывания
Часто встречается ситуация, когда биополимер имеет не одно, а несколько мест связывания. Если эти места одинаковы и не зависят друг от друга (связывание одной молекулы лиганда не влияет на константу связывания следующей молекулы лиганда), то общие закономерности связывания мало отличаются от рассмотренных в предыдущем разделе.
Рис.
4.2. Те
же данные, что и на предыдущем рисунке,
но представленные в виде графика
Скетчарда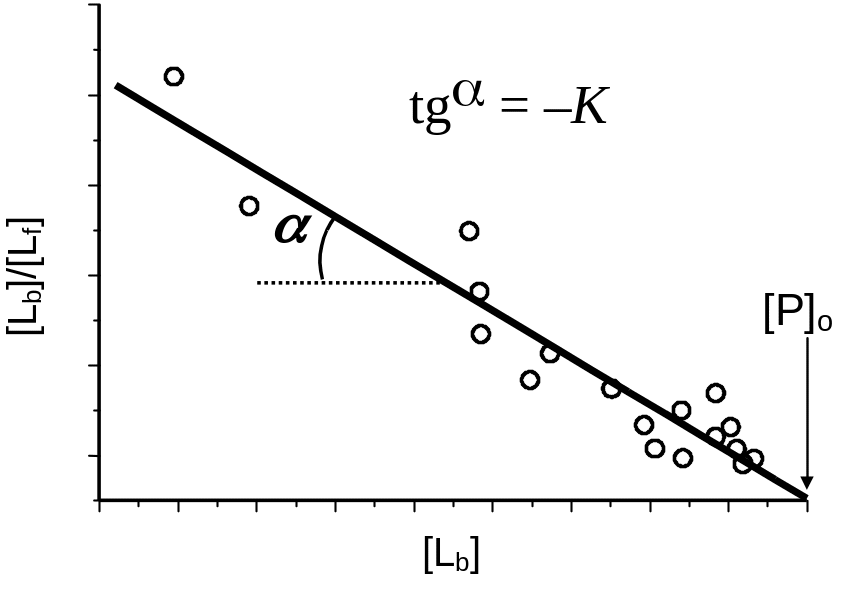
![]()
( 4.0)
![]()
( 4.0)
Так же как и в предыдущем разделе, кривая связывания представляет собой гиперболу, а график Скетчарда — прямую линию. Отличие заключается лишь в том, что кривая связывания стремится не к [P]o, а к n, а прямая Скетчарда отсекает на оси абсцисс отрезок, равный n.
Два типа независимых мест связывания
Нередко биополимер обладает несколькими типами мест связывания, различающихся сродством к лиганду (разной константой связывания). В простейшем случае двух типов независимых мест связывания кривая связывания описывается суммой двух гипербол (при трех типах мест связывания — суммой трех гипербол и т.д.) (уравнение ( 4 .0):
![]()
![]()
( 4.0)
Рис.
4.3. Графика
Скетчарда для случая связывания лиганда
с биополимером, имеющим два типа
независимых места связывания.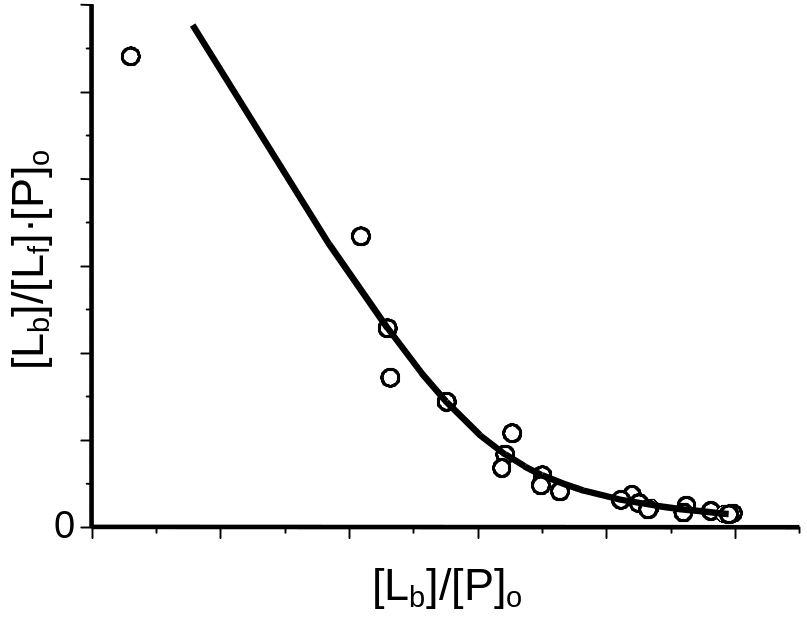
Вообще говоря, линейные анаморфозы и, в частности, график Скетчарда дают менее точные и достоверные результаты, чем непосредственно нелинейная регрессия экспериментальных данных. Однако предварительный анализ таких графиков может быть весьма полезен для выяснения типа связывания и оценки величины начальных параметров для нелинейной регрессии.
Остается вопрос: можно ли так же хорошо описать экспериментальные данные, предполагая наличие у макромолекулы более, чем двух типов мест связывания? Конечно, большее число параметров позволяет подогнать к модели любые данные и получить более хорошее соответствие между расчетом и экспериментом. Однако для объяснения результатов (в пределах экспериментальной ошибки) лучше всего использовать наиболее простую модель. Такой подход дает возможность описать систему минимальным (и, по-видимому основным) числом параметров.
В заключение следует сказать, что вогнутая кривая Скетчарда характерна не только для макромолекул с двумя или большим числом типов мест связывания, но и для антикооперативного связывания лиганда. Проблемы кооперативного связывания мы рассмотрим ниже.
