
- •Учебно-методическое пособие для студентов математического факультета заочной формы обучения
- •Введение
- •Общие методические указания
- •Учебная программа по физике
- •1. Физические основы механики
- •Кинематика материальной точки и твердого тела
- •Динамика материальной точки и твердого тела
- •Работа и механическая энергия
- •Механика жидкостей
- •Механические колебания и волны
- •Основы молекулярной физики и термодинамики
- •Основные положения молекулярно-кинетической теории
- •Основы термодинамики
- •Жидкости и твердые тела
- •3. Электричество и магнетизм
- •3.1. Электростатика
- •3.2. Постоянный электрический ток
- •3.3. Магнетизм
- •3.31. Магнитное поле
- •4. Оптика. Квантовая физика
- •4.12. Интерференция и дифракция света
- •4.24. Энергетические зоны в кристаллах
- •4.3. Элементы физики атомного ядра и ядерной физики
- •Литература
- •Учебные материалы по курсу «физика»
- •1. Физические основы механики
- •Кинематика материальной точки и твердого тела
- •Динамика материальной точки и твердого тела
- •1.3. Работа и механическая энергия
- •Механика жидкостей
- •1.5. Механические колебания и волны
- •2. Основы молекулярной физики и термодинамики
- •2.1. Основные положения молекулярно-кинетической теории газов
- •2.2. Основы термодинамики
- •2.3. Жидкости и твердые тела
- •Примеры решения задач
- •Контрольная работа № 1
- •Учебные материалы по курсу «физика»
- •3. Электричество и магнетизм
- •3.1. Электростатика
- •3.2. Постоянный электрический ток
- •3.3. Магнетизм
- •3.31. Магнитное поле
- •3.32. Электромагнитная индукция
- •3.33. Магнитные свойства вещества
- •3.34. Основы теории Максвелла для электромагнитного поля
- •3.35. Квазистационарные токи
- •3.36. Электромагнитные волны
- •4. Оптика. Квантовая физика
- •4.1. Оптика
- •Геометрическая оптика
- •4.12. Интерференция и дифракция света
- •4.13. Поляризация света
- •4.14. Взаимодействие света с веществом
- •4.15. Квантовая природа излучения
- •4.2. Элементы атомной физики, квантовой механики и физики твердого тела
- •4.21. Атомная физика
- •4.22. Единство волновых и корпускулярных свойств электромагнитного излучения
- •4.23. Общее уравнение Шредингера. Модели строения атомов. Энергетические уровни свободных атомов
- •4.3. Элементы физики атомного ядра и ядерной физики
- •Примеры решения задач
- •Контрольная работа №2
- •Приложение
- •Десятичные и кратные дольные единицы
- •Содержание
- •210038, Г. Витебск, Московский проспект, 33.
4.2. Элементы атомной физики, квантовой механики и физики твердого тела
4.21. Атомная физика
57. Обобщенная формула Бальмера, описывающая серии в спектре водорода:
![]() ,
,
где
– частота спектральных линий в
спектре атома водорода;
![]() – постоянная Ридберга; т определяет
серию (т=1,2,3,… ); n определяет
отдельные линии соответствующей серии
(п=m+1, т+2,
...): m= 1 (серия
Лаймана), m=2
(серия Бальмера), т=3 (серия Пашена),
m=4 (серия Брэкета),
m=5 (серия Пфунда),
т=6 (серия Хемфри).
– постоянная Ридберга; т определяет
серию (т=1,2,3,… ); n определяет
отдельные линии соответствующей серии
(п=m+1, т+2,
...): m= 1 (серия
Лаймана), m=2
(серия Бальмера), т=3 (серия Пашена),
m=4 (серия Брэкета),
m=5 (серия Пфунда),
т=6 (серия Хемфри).
58. Первый постулат Бора (постулат стационарных состояний):
![]()
![]() ,
,
где m![]() – масса электрона; v
– скорость
электрона на n-ой
орбите радиусом r
– масса электрона; v
– скорость
электрона на n-ой
орбите радиусом r![]() .
.
59. Второй постулат Бора (правило частот):
![]() ,
,
где E
и E![]() – соответственно энергии
стационарных состояний атома до и после
излучения (поглощения).
– соответственно энергии
стационарных состояний атома до и после
излучения (поглощения).
60. Энергия электрона на n-й стационарной орбите:

![]() ,
,
где Z – порядковый номер элемента в системе Менделеева; – электрическая постоянная.
4.22. Единство волновых и корпускулярных свойств электромагнитного излучения
61. Связь дебройлевской длины волны частицы с импульсом р:
![]() ,
,
где m – масса частицы; v – ее скорость.
62. Фазовая скорость свободно движущейся со скоростью vфаз частицы массой m:
![]() ,
,
где
![]() – энергия
частицы (
– круговая частота);
– энергия
частицы (
– круговая частота);
![]() – ее импульс (
– ее импульс (![]() – волновое число).
– волновое число).
63. Групповая скорость свободно движущейся частицы:
![]() .
.
64. Соотношения неопределенностей:
для координаты и импульса частицы:
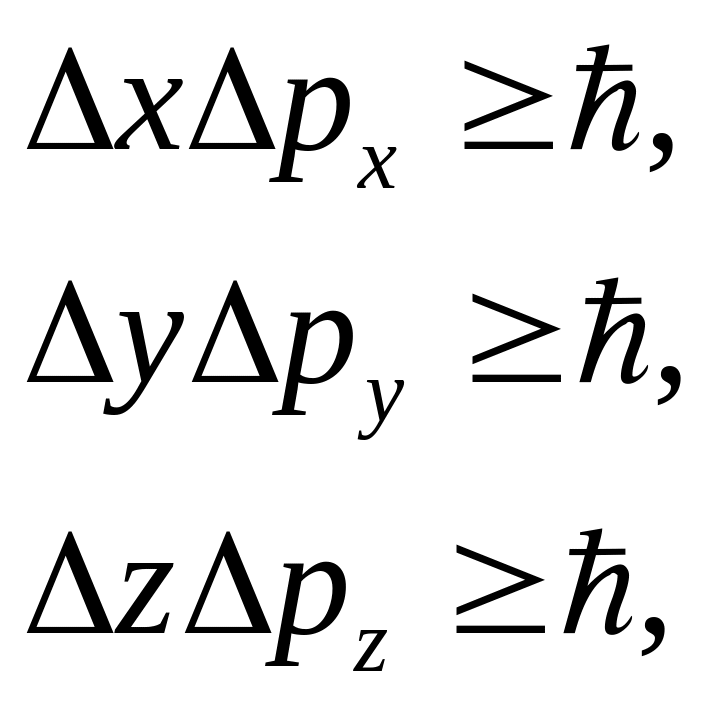
где
![]() – неопределенности координат,
– неопределенности координат,
![]() –неопределенности
соответствующих проекций импульса
частицы на оси координат;
–неопределенности
соответствующих проекций импульса
частицы на оси координат;
для энергии и времени:
![]()
где
![]() – неопределенность энергии
данного квантового состояния;
– неопределенность энергии
данного квантового состояния;
![]() – время пребывания системы в
данном состоянии.
– время пребывания системы в
данном состоянии.
4.23. Общее уравнение Шредингера. Модели строения атомов. Энергетические уровни свободных атомов
65. Вероятность нахождения частицы в
объеме
![]() :
:
![]()
где
![]() – волновая функция, описывающая
состояние частицы;
– волновая функция, описывающая
состояние частицы;
![]() – функция, комплексно сопряженная
с
– функция, комплексно сопряженная
с
![]() ;
;
![]() –
квадрат модуля волновой функции.
–
квадрат модуля волновой функции.
66. Для стационарных состояний:
![]()
где
![]() – координатная
(амплитудная) часть волновой функции.
– координатная
(амплитудная) часть волновой функции.
67. Условие нормировки вероятностей:
![]()
где интегрирование производится по
всему бесконечному пространству, т.е.
по координатам x,y,z
от
![]() до
до
![]() .
.
68. Вероятность обнаружения частицы в
интервале от х![]() до х2:
до х2:

69. Среднее значение
физической величины L,
характеризующей частицу, находящуюся
в состоянии, описываемом волновой
функцией
![]() :
:
![]()
70. Общее уравнение Шредингера (уравнение Шредингера, зависящее от времени):
![]()
где
![]() – волновая
функция, описывающая состояние частицы;
– волновая
функция, описывающая состояние частицы;
![]() ;
m –
масса частицы;
;
m –
масса частицы;
![]() – оператор
Лапласа
– оператор
Лапласа
![]()
![]() – мнимая
единица;
– мнимая
единица;
![]() –
потенциальная энергия частицы в силовом
поле, в котором она движется.
–
потенциальная энергия частицы в силовом
поле, в котором она движется.
71. Уравнение Шредингера для стационарных состояний:
![]()
где
![]() – координатная часть
волновой функции
– координатная часть
волновой функции
![]() – потенциальная энергия
частицы; E –
полная энергия частицы.
– потенциальная энергия
частицы; E –
полная энергия частицы.
72. Волновая функция, описывающая одномерное движение свободной частицы:
![]()
где А – амплитуда
волн де Бройля;
![]() – импульс частицы;
– импульс частицы;
![]() – энергия частицы.
– энергия частицы.
73. Собственные значения энергии
![]() частицы, находящейся на n-м
энергетическом уровне в одномерной
прямоугольной «потенциальной яме» с
бесконечно высокими «стенками»:
частицы, находящейся на n-м
энергетическом уровне в одномерной
прямоугольной «потенциальной яме» с
бесконечно высокими «стенками»:
![]() ,
,
где l – ширина ямы.
74. Собственная волновая функция, соответствующая вышеприведенному собственному значению энергии:
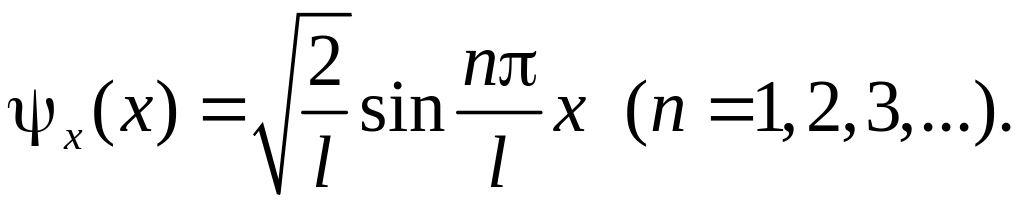
75. Коэффициент прозрачности D прямоугольного потенциального барьера конечной ширины:
![]()
где D![]() – множитель, который можно
приравнять единице; U – высота
потенциального барьера; Е – энергия
частицы.
– множитель, который можно
приравнять единице; U – высота
потенциального барьера; Е – энергия
частицы.
76. Уравнение Шредингера для линейного гармонического осциллятора в квантовой механике:
![]()
где
![]() –
потенциальная энергия осциллятора;
– собственная частота
колебаний осциллятора; m – масса
частицы.
–
потенциальная энергия осциллятора;
– собственная частота
колебаний осциллятора; m – масса
частицы.
77. Собственные значения энергии гармонического осциллятора:

![]()
78. Энергия нулевых колебаний гармонического осциллятора:
![]()
79. Потенциальная энергия U(r) взаимодействия электрона с ядром в водородоподобном атоме:

где r – расстояние между электроном и ядром; Z – порядковый номер элемента; – электрическая постоянная.
80. Собственное значение энергии электрона в водородоподобном атоме:
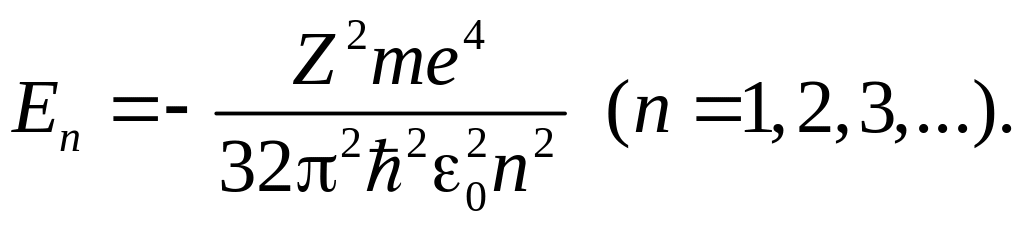
81. Энергия ионизации атома водорода:
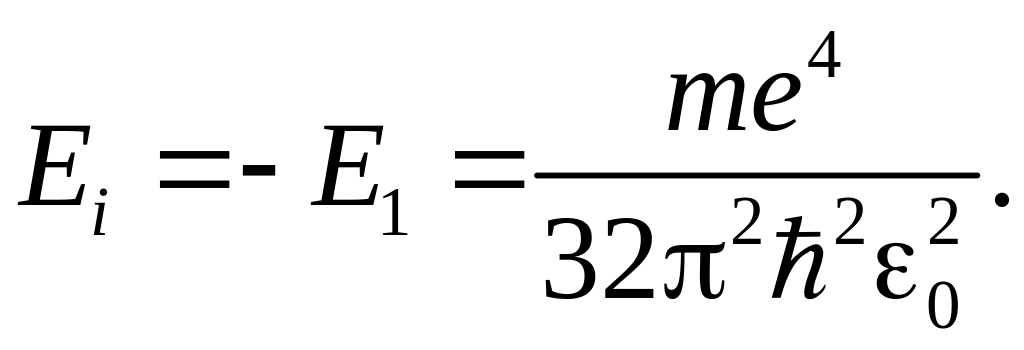
82. Момент импульса (механический орбитальный момент) электрона:
![]()
где l – орбитальное
квантовое число, принимающие при заданном
n следующие значения:
![]() (всего n значений).
(всего n значений).
83. Проекция момента импульса на направление z внешнего магнитного поля:
![]() ,
,
где m![]() – магнитное квантовое
число, принимающее при заданном l
следующие значения:
– магнитное квантовое
число, принимающее при заданном l
следующие значения:
![]() (всего (2l+1) значений).
(всего (2l+1) значений).
84. Правила отбора для орбитального и магнитного квантовых чисел:
![]() и
и
![]()
85. Спин (собственный механический момент импульса) электрона:
![]()
где s – спиновое квантовое число (s=1/2).
86. Проекция спина на направление z внешнего магнитного поля:
![]() ,
,
где
![]() – магнитное спиновое квантовое
число (m
– магнитное спиновое квантовое
число (m![]() =
=![]() ).
).
87. Принцип Паули:
![]() или 1,
или 1,
где
![]() – число электронов, находящихся в
квантовом состоянии, описываемом набором
четырех квантовых чисел: n – главного,
l – орбитального, m
– магнитного спинового,
m
– магнитного.
– число электронов, находящихся в
квантовом состоянии, описываемом набором
четырех квантовых чисел: n – главного,
l – орбитального, m
– магнитного спинового,
m
– магнитного.
88. Максимальное число электронов Z(n), находящихся в состояниях, определяемых данным главным квантовым числом n:
![]()
89. Коротковолновая граница сплошного рентгеновского спектра:
![]()
где e – заряд электрона, U – разность потенциалов, приложенная к рентгеновской трубке.
90. Закон Мозли, определяющий частоты спектральных линий характеристического рентгеновского излучения:

где R –
постоянная Ридберга; Z
– порядковый номер
элемента в периодической системе;
![]() – постоянная
экранирования; т определяет
рентгеновскую серию (т=1,2,3,...); n
определяет отдельные линии соответствующей
серии (n=m+1,m+2,...).
– постоянная
экранирования; т определяет
рентгеновскую серию (т=1,2,3,...); n
определяет отдельные линии соответствующей
серии (n=m+1,m+2,...).
91. Закон Мозли для линии
![]() :
:

