
286 Г/моль ‑ 106 г/моль
х г ‑ 6 г
х = mкр = (2866)/106 = 16,19г.
3) определим массу воды, которую необходимо прибавить к кристаллогидрату, по формуле
mв-ва = mр-ра – mкр.
mв-ва = 100 ‑ 16,19 = 83,81г.
4) Поскольку при приготовлении раствора количество воды отмеряют не на весах, а при помощи мерной посуды, найдем объем, который занимают 83,81 г воды по уравнению:
Vводы=![]()
Плотность воды при 25С составляет 0,999 г/см3. Тогда объем воды:
Vводы = 83,81/0,999 = 83,89 см3.
Поскольку при помощи мерного цилиндра возможно отмерить такой объем возможно с точностью до одного миллилитра, округлим полученное значение до 84 см3.
Ответ: потребуется 16,19 г Na2CО3∙10Н2О и 84 см3 воды.
Часто данные, указанные справочнике, находятся между интересующих нас значений. Для более точных расчетов применяют метод интерполяции.
Пример 2. Метод интерполяции
Рассчитать плотность 3% раствора НCl, пользуясь следующими справочными данными
1) С% ρ
2,36 1,01
. . . . . . . .
4,39 1,02
___________________
∆С%=2,03 ∆ρ=0,01.
Рассчитать как изменится плотность с изменением концентрации.
При увеличении С% на 2,03 плотность увеличится на 0,01.
2) насколько увеличится концентрация по сравнению с табличным значением
∆С%=3-2,36=0,64.
3) при увеличении концентрации на 2,03, плотность изменится на 0,01, а при увеличении концентрации на 0,64, плотность изменится на х.
2,03 – 0,01
0,64 – х
Отсюда х найдем по уравнению
Х=![]()
4) по сравнению с табличным значением плотность раствора увеличится на 0,003, тогда плотность будет равна
ρ3=1,01+0,003=1,013г/мл.
3 Порядок выполнения работы
1) Рассчитать необходимую массу кристаллогидрата и объем воды согласно индивидуальному заданию.
2) Приготовить раствор
В чистый сухой стакан на технических весах отбирают рассчитанную навеску кристаллогидрата.
Рассчитанное количество дистиллированной воды наливают в цилиндр. Приливают воду из цилиндра в стакан с навеской. Не допускается высыпать соль в цилиндр!
3) Точность приготовления полученных растворов проверяют, измеряя их плотность. Для этого используют специальный прибор – ареометр. Он представляет собой запаянную стеклянную ампулу с определенным количеством груза – свинцовой дроби, и шкалой. Обычно применяют набор ареометров, отличающихся массой груза, а, следовательно, и диапазоном измеряемых плотностей.
Правила пользования ареометрами.
а) необходимо по справочнику уточнить предполагаемый диапазон измеряемых плотностей и выбрать из всего набора несколько ареометров (2…3) таким образом, чтобы шкала следующего ареометра начиналась с того значения, на котором закончилась шкала предыдущего ареометра. Выбранные ареометры поставить в стакан с уложенной на дно фильтровальной бумагой. Класть на стол ареометры нельзя!
б) налить исследуемый раствор в стеклянный цилиндр. Размер цилиндра должен позволять разместить в нем ареометр;
в) из выбранных ареометров взять наиболее легкий, для измерения меньших плотностей и аккуратно, придерживая, опустить его в цилиндр с раствором. Не допускается резко отпускать ареометр! Если ареометр всплывает и шкала его не погружается в раствор, необходимо его вынуть, обтереть фильтровальной бумагой и поставить в стакан с уложенной на дно фильтровальной бумагой. Затем взять следующий ареометр, шкала которого начинается с последнего значения предыдущего ареометра, и снова провести измерения.
Если ареометр утонул, его шкала полностью погрузилась под слой жидкости, значит, неверно был выполнен пункт а). В этом случае ареометр необходимо извлечь из раствора. Для этого над раковиной цилиндр с раствором прикрывают рукой и переворачивают, вынимая ареометр. Моют ареометр и руки. Растворы солей, используемый в данной работе, не едкие.
г) Правильным считается такое положение ареометра при измерении, когда его шкала погружена в раствор. Показания читают по нижнему мениску.
д) После выполнения измерений ареометры промывают водопроводной и дистиллированной водой над раковиной, аккуратно вытирают фильтровальной бумагой и возвращают в ящик.
4) Зная плотность полученного раствора, определить по справочнику его истинную концентрацию. Для более точных расчетов использовать метод интерполяции.
5) Рассчитать погрешность приготовления раствора.
Абсолютной погрешностью ΔС% является модуль разности между экспериментально полученным значением С%эксп и заданным значением С%зад:
Δ С% = | С%эксп ‑ С%зад |.
Абсолютная погрешность измеряется в тех же единицах, что и определяемая величина.
Относительной погрешностью δ называют отношение абсолютной погрешности к заданному значению:
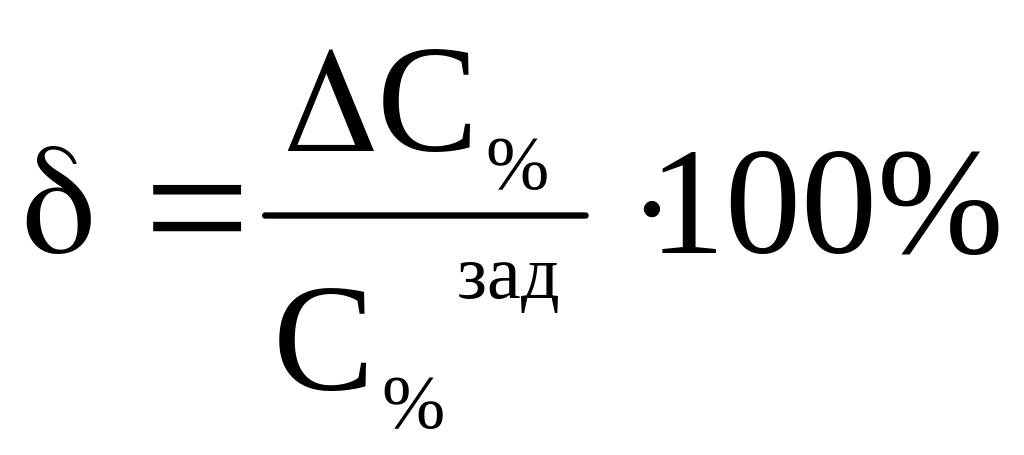 , % .
, % .
В выводах к проделанной работе следует указать истинное значение концентрации раствора и погрешность приготовления раствора.
