
- •Лабораторная работа «определение теплоемкости веществ
- •Краткие сведения из теории
- •Объемная теплоемкость газов выражается через мольную, как
- •Аналитические зависимости для теплоемкостей Cv и Cp получают, используя уравнения для внутренней энергии и энтальпии:
- •Выражение для теплоемкости при постоянном давлении получается из уравнений (2) и (4).
- •После дифференцирования обеих частей уравнения (19) по времени получим
- •V. Методика обработки результатов экспериментов.
- •V. Определение погрешностей эксперимента
- •VII. Требования к отчету.
Выражение для теплоемкости при постоянном давлении получается из уравнений (2) и (4).
При Р= const, dр=0 получим
dq = (i/T)p·dT (8)
отсюда
Cp = (i/T)p (9)
То есть теплоемкость тела при постоянном давлении является функцией температуры и давления. Для идеального газа, когда энтальпия является функцией только температуры i = f(T), теплоемкость запишется
Cp = di/dT. (10)
Учитывая, что теплоемкость непостоянная и зависит от температуры и других термических параметров, различают истинную и среднюю теплоемкости.
Истинной теплоемкостью называется отношение элементарного количества сообщается термодинамической системе в каком-либо процессе к бесконечно малой разности температур.
С= lim Q1-2/T = dQ/dT. (11)
Средней теплоемкостью процесса в интервале температур от Т1 до Т2 называют частное от деления теплоты на приращение температуры системы, то есть
Cm = Q1-2/ (T2- T1). (12)
Опытным путем было установлено, что теплоемкость газа непостоянная, а представляет собой функцию температуры; в общем случае эта зависимость (рис.1) может быть представлена уравнением
C = C0 + a·t + b·t2 + d·t3+…, (13)
где С0 – теплоемкость при 0 С; a, b, d…, - постоянные коэффициенты.
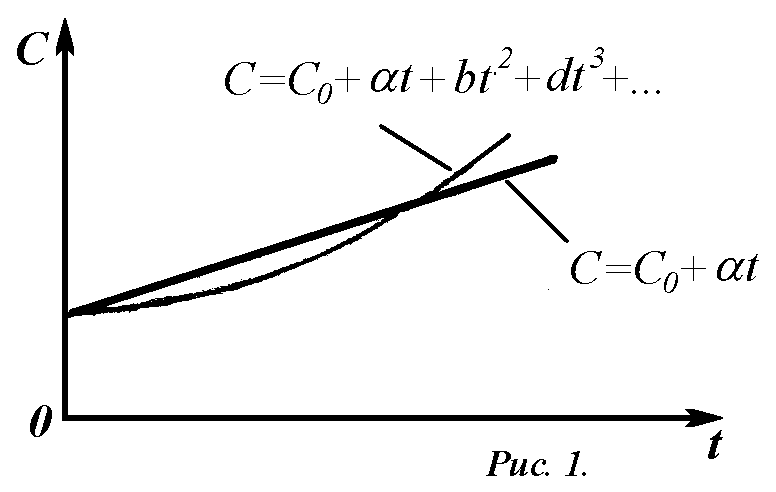
Так как коэффициенты b, d… весьма малы и влияние на значение С членов с температурой в степени выше первой весьма мало, то для технических расчетов часто принимают линейную зависимость теплоемкости от температуры и выражают ее формулой
C = C0 + a·t; (14)
Средняя теплоемкость в пределах от Т1 до Т2 определяется из уравнения
C = (C ·t2 – C ·t1)/(t2-t1). (15)
В основу работы измерителя теплоемкости НТ-С-400 положен сравнительный метод динамического С-калориметра с тепломером и адиабатической оболочкой.
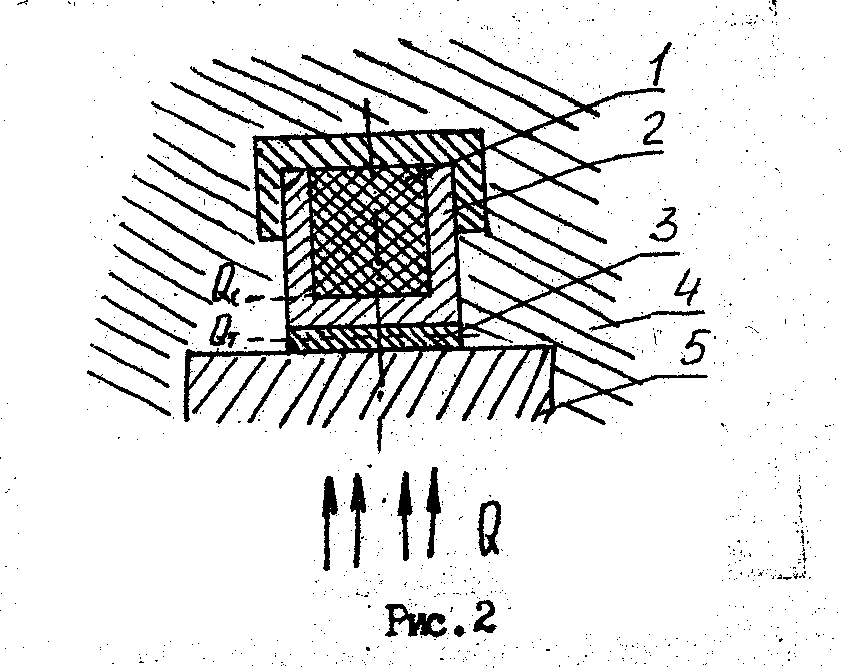
На рис.2 показана тепловая схема метода. Испытуемый образец 1 размещается внутри металлической ампулы 2 и монотонно разогревается вместе с ней за счет непрерывно поступающего к ампуле через тепломер 3 теплового потока.
Тепловая связь ампулы 2 и образца 1 с внешней средой допускается только через тепломер 3, поэтому открытие участка поверхности ампулы отделено от среды адиабатической оболочкой 4. весь процесс нагревания можно разделить на три стадии.
Первая стадия режима охлаждения (неупорядоченного) характеризуется большим влиянием начального распределения температуры, и зависимость между Т и описывается уравнением
T = An·vn·l-m ·, (16)
где An – постоянный коэффициент,
vn = cos (n·/) – функция только координаты х,
mn = n2 · a/2 – комплекс, представляющий собой постоянное вещественное положительное число,
n = 1, 2, 3 …
Вторая стадия охлаждения называется регулярным режимом, а зависимость между Т и описывается уравнением
T = A1·v1·l-mt (17)
Третья стадия охлаждения соответствует стационарному режиму, когда температура во всех точках тела равна температуре охлаждающей среды.
Рассмотрим регулярный режим нагрева тела. Прологарифмировав выражение (17) и опустив
lnT = ln (A·v) – m· (18)
или
lnT = -m· + c(x, y, z) (19)
