
- •Химическая термодинамика
- •Часть 1
- •Термохимия
- •Цель работы
- •Теоретическая часть
- •Экспериментальная часть
- •Порядок выполнения работы
- •Обработка результатов эксперимента
- •Расчет теплоты образования твердого раствора kCl . RBr
- •Определение изменения температуры в калориметрическом опыте
- •Расчет теплоты образования кристаллогидрата
- •Контрольные вопросы
- •II. Изучение равновесия гомогенной реакции в растворе
- •Цель работы
- •Теоретическая часть
- •Экспериментальная часть
- •Порядок выполнения работы
- •Обработка экспериментальных данных
- •Контрольные вопросы
- •III. Определение коэффициента распределения иода между органическим и неорганическим растворителями
- •Цель работы
- •Теоретическая часть
- •Экспериментальная часть
- •3.2. Порядок выполнения работы
- •Обработка результатов эксперимента
- •Контрольные вопросы
- •IV. Изучение взаимной растворимости в трехкомпонентных системах
- •Цель работы
- •Теоретическая часть
- •Экспериментальная часть
- •Порядок выполнения работы
- •Обработка экспериментальных данных
- •Контрольные вопросы
- •Литература
- •Содержание
- •Термохимия
Экспериментальная часть
Приборы и реактивы: калориметрическая установка, секундомер, мерный стакан, KCl, KBr, твердый раствор KCl ∙ KBr , CuSO4 ∙ 5H2O, CuSO4.
Порядок выполнения работы
Определение константы калориметра
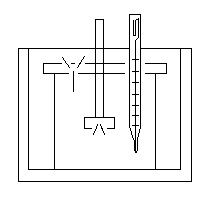
Собрать калориметрическую установку (рис. 1). В калориметрический стакан налить 150 см3 дистиллированной воды. На технических весах отвесить 2 г измельченного KCl. Проверить мешалку и, убедившись, что она не задевает частей калориметра, включить мотор. Спустя 2 – 3 минуты после начала перемешивания начать отсчет температуры через каждые 30 секунд. По истечении 5 минут равномерного измерения температуры (предварительный период) через отверстие в крышке калориметра, в котрое вставлена воронка, быстро ввести исследуемую соль (главный период), не прекращая отсчета температуры через каждые 30 секунд. После установления равномерного хода температуры измерения проводят еще 2 – 3 минуты (заключительный период).





 2 5 3
4 6
Рис. 1
2 5 3
4 6
Рис. 1
1 Схема калориметрической установки:
 1
– калориметрический стакан,
1
– калориметрический стакан,
2 – теплоизолирующая крышка,
3 – мешалка,
4 – термометр Бекмана,
5 – воронка,
6 – изотермическая оболочка
Полученные экспериментальные данные заносят в таблицу 1.
Таблица 1
Предварительный период |
Главный период |
Заключительный период |
|||
τ, мин
|
t, 0C |
τ, мин |
t, 0C |
τ, мин |
t, 0C |
0,5 …. |
|
4,0 …. |
|
7,0 ….. |
|
Определение теплоты растворения КBr и твердого раствора RCl .RBr
Провести опыты с навесками КBr, а затем KCl . KBr аналогично определению постоянной калориметра. Массы взять такими же, как в опыте с KCl. Данные занести в таблицу 2 по приведенному образцу таблицы 1.
Определение теплоты растворения CuSO4 и CuSO4 . 5H2O
Провести опыты с навеской CuSO4 , а затем CuSO4 . 5Н2О аналогично определению постоянной калориметра Массы навесок взять соответственно 3 г и 3 ,75 г. Данные занести в таблицу 2 по приведенному образцу таблицы 1.
Обработка результатов эксперимента
