
99 кругов АДА
.pdf
-долей лиц репродуктивного возраста;
-соотношением полов в популяции;
-колебаниями численности во времени;
-изменчивостью индивидуальной плодовитости.
Эффект «бутылочного горлышка»: резкое сокращение численности популяции, после которого следует её быстрый рост, в результате частоты аллелей сильно отличаются от таковых в материнской популяции
Эффект «основателя (родоначальника)»: предельный случай дрейфа генов, когда происходит возникновение новой популяции от ограниченного числа особей, регистрируется в географически и социально изолированных популяциях
30. Естественный отбор. Типы естественного отбора и их влияние на генетическое разнообразие популяций.
Естественный отбор единственный фактор, который действует в популяции направленно.
Дифференциальное воспроизведение различных генетических вариантов.
Естественный отбор вызывает адаптивные изменения в генетической структуре популяций, в результате различий в соотносительном вкладе разных генотипов из репродуктивной части популяции в генофонд последующего поколения за счет дифференциального выживания или плодовитости.
Направленный естественный отбор (w1>w2>w3): селективным преимуществом обладают носители определенного аллеля в только гомозиготном состоянии, или в гомозиготном и гетерозиготном состоянии. Происходит фиксация благоприятного аллеля. Снижение генетического разнообразия
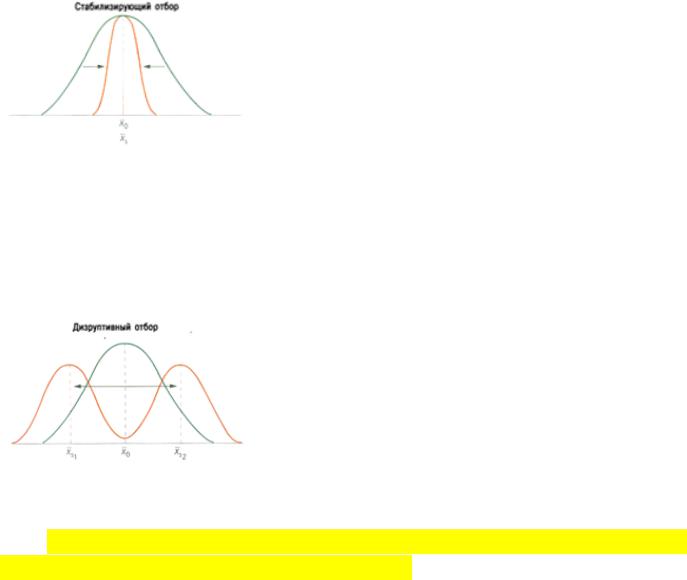
Балансирующий (стабилизирующий, сверхдоминирование w1<w2>w3): селективным преимуществом обладают ГЕТЕРОЗИГОТЫ. Устанавливается равновесные частоты аллелей, которые определяются исключительно величинами приспособленности носителей разных генотипов
Дизруптивный (разнообразящий w1>w2<w3): наименьшей приспособленностью обладают гетерозиготы. Фиксироваться будет тот аллель, который изначально в популяции регистрировался с более высокой частотой. Снижение генетического разнообразия
31. Естественный отбор. Компоненты приспособленности. Подходы к оценке интенсивности естественного отбора.
Относительная приспособленность (w) дифференциальная выживаемость – вероятность выживания до репродуктивного периода и дифференциальная плодовитость – способность передавать свои гены последующим поколениям.
Наследственные болезни в большинстве случаев снижают приспособленность их носителей: больные имеют меньшие шансы дожить до репродукции и/или оставить потомство.
Геномные и хромосомные мутации резко снижают приспособленность своих носителей и приводят к их элиминации из популяции.

Аутосомно-доминантные заболевания уменьшают среднюю репродуктивную способность их носителей.
Для аутосомно-рецессивных заболеваний естественный отбор обычно направлен против гомозигот по генам этих заболеваний, приводя к их полной или частичной элиминации.
32. Генетический груз популяций. Источники возникновения и составляющие компоненты генетического груза.
Генетический груз – величина показывающая, насколько средняя приспособленность ниже оптимальной для популяции.
L = Wmax – W/ Wmax
Основные компоненты:
1.Мутационный груз – снижение приспособленности за счет накопления в популяции мутантных генов.
2.Сегрегационный груз – снижение приспособленности за счет балансирующего отбора
3.Субституционный груз – снижение приспособленности за счет направленного отбора
Иначе говоря, фактическая средняя приспособленность популяции ниже той, которая была бы, если бы вся популяция состояла только из наиболее приспособленных генотипов. Менее приспособленные генотипы составляют как бы груз, который тянет популяцию вниз. В то же время из поколения в поколение протекает эволюция популяции в сторону ослабления влияния генетического груза.
Генетический груз популяции - распространенность неблагоприятных мутаций, которые проявляются как наследственные болезни или как факторы, снижающие устойчивость (приспособленность) людей к воздействию внешней среды, другими словами, определяют предрасположенность к заболеваниям
33. Эффекты инбридинга и подразделенности популяций на генетическое разнообразие популяций.
Панмиксия – полная случайность внутрипопуляционных скрещиваний, что означает независимость вероятности формирования брачных пар от генетической конституции супругов.

Ассортативные браки – неслучайное, предпочтительное заключение браков между определенными когортами мужчин и женщин
Инбридинг (близкородственные браки) – частный случай ассортативных браков, когда выбор брачного партнера осуществляется по признаку родства будущих супругов.
Коэффициент инбридинга (F) – вероятность, с которой у потомка от близкородственного брака в данном локусе будет находиться два идентичных по происхождению гена, полученные от общего предка.
Высокий риск проявления рецессивных наследственных болезней:
•Чем выше степень родства родителей инбредного потомства, тем большая часть генома общих предков может у него перейти в гомозиготное состояние
•Чем реже ген рецессивного заболевания встречается в популяции, тем выше шансы, что соответствующее заболевание обнаружится в близкородственном браке
34.Современная концепция экогенетики. Основные составляющие экогенетики, как науки.
Экогенетика - это наука, которая изучает различные генетически обусловленные реакции людей на определённые агенты среды. (рабочая гипотеза: биохимические особенности определяют характер реакции организма на любое внешнее воздействие)
Полиморфизм – генетический субстрат
В её задачи входит объяснение различной чувствительности отдельных людей к действию потенциально опасных внешних агентов и изучение индивидуальных особенностей адаптации к окружающей среде.
Это факторы и природные и антропогенные: экстремальные температуры, давления и УФ, выхлопы автомобилей, дымы и промышленные загрязнения, тяжелые металлы, инсектициды, различные виды излучений. Основы экологической генетики человека лежат в общебиологических закономерностях эволюции.
Отвечает на вопросы:
а) каким образом данный фактор действует на генетический материал; б) насколько широко подвергается человеческая популяция воздействиям этого фактора;

в) каково вероятное увеличение частоты мутаций по сравнению с частотой спонтанных мутаций; г) каковы долговременные последствия увеличения частоты мутаций для популяции.
Методы, которые использует: близнецовые сопоставления, внутрисемейный корреляционный анализ и сравнение характера реакций в различных этнических группах населения
35. Экогенетика: характеристика экогенетических патологических реакций на факторы окружающей среды.
При воздействии повреждающих или новых факторов окружающей среды на человека могут наблюдаться нежелательные эффекты в виде: 1) изменения наследственных структур (индуцированный мутационный процесс); 2) патологических проявлений экспрессии генов на специфические факторы среды; 3) изменений генофонда популяций в результате нарушения генетического равновесия между основными популяционными процессами (мутационный процесс, отбор, миграция, дрейф генов).
Эффекты 1-го типа — это прежде всего индуцированный окружающей средой (в широком смысле слова) мутационный процесс. Этот процесс ведет к повышению темпов наследственной изменчивости человека на индивидуальном и популяционном уровнях.
Эффекты 2-го типа у человека проявляются на индивидуальном уровне в виде патологических реакций (болезней), а на популяционном уровне — в виде большей или меньшей приспособленности (адаптация, акклиматизация). Патологические проявления аллелей под влиянием среды факторов называются экогенетическими реакциями, или болезнями.
Эффекты 3-го типа — изменения генофонда популяций являются долговременными (десятки и даже сотни поколений). Биологически стабильному виду свойственно постоянное равновесие основных генетических процессов (мутационный процесс, отбор, миграция, дрейф генов). Современный период характеризуется большей скоростью и объемом изменений среды обитания. Наследственность человека на популяционном уровне так быстро меняться не может. Следствием высоких темпов и большого объема изменений среды обитания человека

(измененные экологические условия) могут стать изменения в генофонде конкретных популяций или человечества в целом.
36. Экогенетика. Основные фазы детоксикации ксенобиотиков.
Некоторые специфические мутации являются основой высокой чувствительности их носителей к определённым факторам внешней среды. Потенциально токсические факторы окружающей среды повреждают не всё население, а только его часть, генетически предрасположенную к таким мутациям. Доказано, что у человека существует генетический контроль метаболизма поступающих в организм химических соединений (биотрансформации).
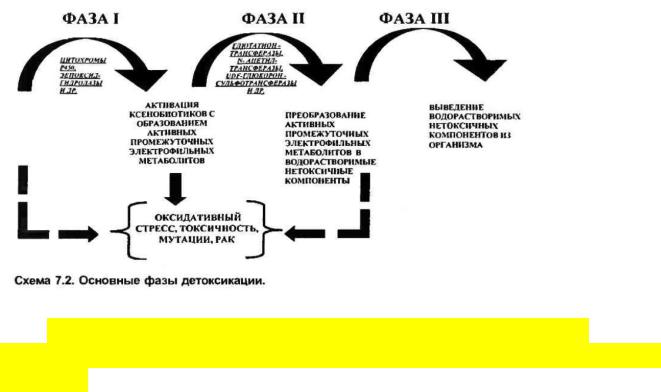
Современные данные позволяют говорить о трёх фазах детоксикации ксенобиотиков, из которых первые две осуществляются с помощью генетически детерминированных ферментов.
Во время I фазы ксенобиотики инактивируются с образованием промежуточных электрофильных метаболитов. Если активация не будет осуществляться по причине потери ферментативной активности мутантного продукта, то ксенобиотики будут давать отрицательный эффект сначала на клеточном, а потом и на организменном уровне.
Активированные ксенобиотики в форме промежуточных электрофильных метаболитов при контакте с другой группой ферментов (главным образом с различными трансферазами) преобразуются в водорастворимые нетоксичные компоненты, которые могут выводиться из организма. Однако если II фаза детоксикации не состоится по причине мутантной формы фермента, то продукты I фазы детоксикации (промежуточные электрофильные метаболиты), как и неактивные ксенобиотики, вызывают окислительный стресс, дают токсические эффекты, обусловливают мутации, рак и другие нежелательные последствия.
На основе многочисленных доказательств природы экогенетических вариаций можно сделать вывод, что они обусловлены балансированным полиморфизмом в генах ферментов, участвующих в обеих фазах детоксикации.
III фаза детоксикации обеспечивается работой физиологических систем выделения (кожа, почки, кишечник).
В патологических экогенетических реакциях в широком плане твёрдо установлена роль следующих полиморфных локусов, участвующих (прямо или опосредованно) в биотрансформации чужеродных веществ: цитохром Р450, N-ацетилтрансфераза, пароксоназа сыворотки, холинэстераза сыворотки, глюкозо-6-фосфатдегидрогеназа, лактаза, ингибиторы протеаз.
37. Фармакогенетика. Генетический контроль метаболизма лекарственных. Фармакогенетические особенности при наследственных болезнях.
Фармакогенетика изучает значение наследсвенности в реакции организма на лекарство.
Врач сталкивается с разными осложнениями лекарственной терапии:
1.Повышенной чувствительностью индивида к лекарству, как это бывает при передозировке лекарства, хотя больному назначена доза, соответствующая возрасту и полу
2.Полной толерантностью больного к лекарству, даже несмотря на увеличение дозы
3.Парадоксальными реакциями на лекарство, включающими совсем другие типы осложнений, чем это следовало бы ожидать, исходя из механизмов действия лекарств
Любые фармакогенетические реакции развиваются на основе широкого генетического полиморфизма в человеческих популяциях, эволюционно сформировавшегося до появления применяемых теперь фармакологических средств.

Прогрессу способствовали два принципиальных подхода: понимание фармакогенетических закономерностей на основе различия в метаболизме лекарств и объяснения различий в реакциях на лекарства различиями органов-мишеней, клеток или рецепторов
Реакциями на лекарство у лиц с наследственными болезнями могут быть извращенными в результате б/х-ческих дефектов Печеночная порфирия обостряется при приёме барбитуратов, ноксирона,
амидопирина, сульфаниламидных и противосудорожных препаратов Подагра усиливается при приеме этанола, диуретиков При наследственных геморрагиях (гемофилия, болезнь фон Виллебранда)
кровотечение усиливается при приеме ацетилсалициловой кислоты Адреналин и глюкагон не вызывают гипергликемии у пациентов с болезнью Гирке
38. Размер генома человека. Физические и генетические меры размерности генома.
Размеры генома человека можно выразить в терминах генетической карты – сантиморганидах и в терминах физической карты – в парах оснований. Важной количественной характеристикой является и общее число структурных генов.
Приблизительные оценки показывают, что гаплоидный геном человека содержит примерно 3,3 милиарда п.о. Размер генома в сантиморганидах, оцененный по цитогенетическим данным (числу хиазм), равен примерно 3000 сМ. Почти все хромосомы превышают по размеру 100 сМ. Самая маленькая из них У-хромосома – насчитывает 50 сМ, а самая крупная – первая хромосома – 250 сМ.
Размер генома человека можно оценить и в метрических мерах длины. Расстояние между 2мя соседними основаниями в цепочке ДНК составляет 3,4 ангстрема или 3,4*10^-8 см. Умножив 3,3 миллиарда на эту цифру, получим длину всей ДНК человека – около 110 см.
По непрямым оценкам, человек имеет от 50 до 100 тысяч структурных генов, т.е. генов, кодирующих амин.последовательность белков и нуклеотидную последовательность различных видов РНК. Наиболее вероятная оценка общего числа генов находится в пределах 70-80 тысяч. Приведенные выше оценки позволяют сопоставить генетические и физические единицы размерности генома. Расстояние в 1 сМ на генетической карте эквивалентно физической дистанции, в среднем, около 1 миллиона п.о. (1 Мб)

39. Мера генетической карты, меры физической карты. Соответствие физических и генетических мер.
Размеры генома можно выразить в терминах генетической карты – в сантиморганидах и в терминах физической карты – в парах оснований. Можно сопоставить генетические и физические оценки генома. Расстояние в 1 сМ на генетической карте эквивалентно физической дистанции, в среднем, около 1 миллиона пар оснований (1 мегабаза). Оговорка «в среднем» здесь совсем не случайна, поскольку рекомбинация на различных участках хромосомы происходит с неодинаковой частотой. Она ниже в прицентромерных участках и повышается при удалении от неё, во-вторых существуют «горячие точки» рекомбинации – небольшие районы хромосомы, для которых характерна очень высокая частота разрывов.
40. Методы анатомирования генома. Картирование и секвенирование. Физическое и генетическое картирование.
Одной из основных целей исследования генома человека является построение его точной и подробной карты. Генетическая карта – это схема, описывающая порядок расположения на хромосоме генов и др. генетических маркеров, а также расстояние между ними. Мелкомасштабная карта с миним. Деталей – картина дифференциального окрашивания хромосом. Самая крупномасштабная карта генома – является полная последовательность нуклеотидов.
Карты генома принято разделять на карты генетического сцепления и физические карты. Различаются они методами построения. Карты генетического сцепления строятся на основе анализа данных по наследованию гена или маркера в ряду поколений, физические карты основываются на прямом исследовании генетической информации – хромосом, генов, молекул ДНК (сегментирование хромосом с помощью дифференциальной окраски)
Секвенирование – процесс выявления последовательности нуклеотидов ДНК.
41. Принципы генетического картирования. Карты генетического сцепления.
Генетические карты показывают относительное расположение на хромосоме генов и других маркеров. Требование к маркеру –

межиндивидуальные различия по нему и легкость выявления этих различий.
Для того, чтобы маркер можно было использовать при картировании, он должен быть полиморфным, т.е должны существовать альтернативные формы признака, которые можно было бы легко различить и описать у членов семьи.
Карты генетического сцепления строят на основе совместного наследования генов или маркеров. Два маркера, расположенные на одной хромосоме, вблизи друг от друга имеют тенденцию передаваться от родителей ребенку совместно. Чем ближе расположены маркеры друг к другу, тем вероятнее, что процесс рекомбинации разделит их.
На генетической карте расстояния между маркерами измеряется в сантиморганидах (сМ). Когда частота рекомбинации между двумя маркерами равна 1%, говорят, что они находятся на расстоянии 1 сМ. Генетическое расстояние в 1 сМ примерно равно физической дистанции в 1 миллион пар оснований (1 Мб - мегабаза)
42. Принципы физического картирования. Мелко- и крупномасштабные физические карты генома
Локализация генов при анализе генетического сцепления или межвидовой гибридизации клеток представляет собой непрямые методы картирования, поскольку основывается на корреляции между признаком и хромосомой при передаче в ряду поколений или клеточных клонов.
Генетические карты, которые строятся на основе прямого исследования генетического материала, называют физическими. Чем более детальная карта, тем меньший участок генома можно картировать. С самым низким разрешения – хромосомная.
Она и карты кДНК относятся к мелкомасштабным физическим картам. При определении положении гена на хромосоме первоначально стоит задача приписать его к определенному хромосомному сегменту – бэнду или группе бэндов, который можно идентифицировать цитогенетически. Сейчас для этого используют метод гибридизации in situ. Клонированную копию нужного гена помечают радиоактивной/флуоресцентной меткой. Меченный фрагмент ДНК – зонд. Затем зонд инкубируют с метафазным препаратом хромосом и, после того как он свяжется с комплиментарной цепочкой ДНК на интактной хромосоме, устанавливают его точную локализацию.
Карта кДНК отражает расположение на хромосоме кодирующих последовательностей. ДНК-копию (кДНК) синтезируют в лаборатории, используя в качестве матрицы молекулы мРНК, вносят метку и локализуют
