
- •3. Термодинамика поверхностных процессов
- •3.1. Поверхностное натяжение и методы его определения
- •3.2. Адсорбция на поверхности жидкости. Уравнение изотермы адсорбции Гиббса
- •3.2.1. Применения изотермы адсорбции Гиббса. Поверхностно-активные и поверхностно-неактивные вещества
- •3.2.2. Зависимость поверхностного натяжения от концентрации пав. Уравнения Шишковского
3. Термодинамика поверхностных процессов
3.1. Поверхностное натяжение и методы его определения
Явления на поверхности обусловлены особым состоянием молекул в поверхностном слое.
Молекулы поверхностных слоев и молекулы в объемной фазе испытывают различные силы межмолекулярного притяжения. Каждая молекула во внутренних слоях жидкости подвергается одинаковому воздействию других окружающих ее молекул. Силы межмолекулярного взаимодействия здесь уравновешены.
Молекулы поверхностного слоя на границе с газом взаимодействуют, с одной стороны, с себе подобными, а с другой, с молекулами второй фазы. На поверхности раздела фаз уравновешены взаимодействия молекул, направленные внутрь вещества и по плоскости самой поверхности (рис. 3.1). Взаимодействие молекулы жидкости с молекулами газа намного меньше, чем с молекулами жидкости. В результате этого равнодействующая молекулярных сил в поверхностном слое не равна нулю в отличие от молекул в объемной фазе.
На поверхности твердого тела или жидкости имеется свободная поверхностная энергия за счет нескомпенсированных сил. За счет этой энергии происходит притяжение поверхностью молекул других веществ.
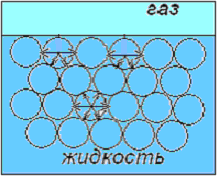
Рис. 3.1. Схема действия межмолекулярных сил внутри жидкости и на ее поверхности
Указанные особенности условий существования молекул поверхностного слоя приводят к тому, что для увеличения поверхности требуется затратить работу.
Величина, численно равная работе обратимого изотермического процесса образования единицы поверхности твердого тела или жидкости, называется поверхностным натяжением .
|
Поверхностное натяжение – величина, характеризующая поверхность и обозначается .
Единицы измерения поверхностного натяжения Н/м; Дж/м2], [дин/см]; [эрг/см2]. |
Единица измерения Н/м соответствует представлению о силе, отнесенной к единице длины контура поверхности, направленной по касательной к плоскости поверхности и стремящейся ее уменьшить.
Термодинамическое определение поверхностного натяжения при р и Т = const выражается уравнением:

Поверхностное натяжение – это фактор интенсивности поверхностной энергии, обусловленной нескомпенсированностью межмолекулярных сил на межфазной поверхности, т.е. представляет собой удельную (приходящаяся на единицу поверхности) свободную энергию Гиббса поверхности.
Поверхностное натяжение – это работа, которую нужно совершить над системой для увеличения поверхности раздела на единицу. Это энергия разрыва межмолекулярных связей и переноса молекул изнутри фазы на поверхность раздела.
Поверхностное натяжение зависит от природы системы, концентрации раствора, температуры, состояния поверхностного слоя. С увеличением температуры увеличивается количество молекул, имеющих достаточную энергию для выхода на поверхность раздела фаз, следовательно, поверхностное натяжение уменьшается.
У тел в твердом состоянии по сравнению с жидкими веществами межмолекулярные взаимодействия больше, соответственно они имеют большую удельную поверхностную энергию.
Рассмотрим пример сравнения значений для различных веществ.
Вещество |
·103 Дж/м2 |
H2O |
71,95 |
Hg |
473,5 |
Pb(ж) |
442 |
Cu(ж) |
1270 |
Поверхностное натяжение меньше у неполярных жидкостей, чем у полярных, имеющих более сильные межмолекулярные связи.
Существует значительное число методов измерения поверхностного натяжения легкоподвижных поверхностей раздела фаз жидкость – газ и жидкость – жидкость. Отметим два из них.
Метод отрыва кольца (метод де Нуи) является одним из наиболее распространенных методов определения поверхностного натяжения жидкостей. Связь поверхностного натяжения с силой F, необходимой для отрыва от поверхности жидкости тонкого кольца радиуса R, хорошо смачиваемого жидкостью, описывается уравнением:

где величина k зависит от соотношения радиуса кольца и толщины проволоки, из которой оно сделано, а также от поверхностного натяжения жидкости; однако последняя зависимость достаточно слаба, что позволяет с удовлетворительной надежностью использовать этот метод как относительный.

где величины Э и FЭ относятся к эталонной жидкости.
Метод максимального давления пузырька основан на измерении максимального значения капиллярного давления

возникающего при образовании на срезе капилляра пузырька сферической формы. Это максимальное давление определяется радиусом капилляра ro. Метод чаще всего используется как относительный, и поверхностное натяжение исследуемой жидкости определяется из отношения значений максимальных давлений исследуемой Р и эталонной Рэ жидкостей или из соотношения соответствующих высот поднятия манометрической жидкости h и hэ:
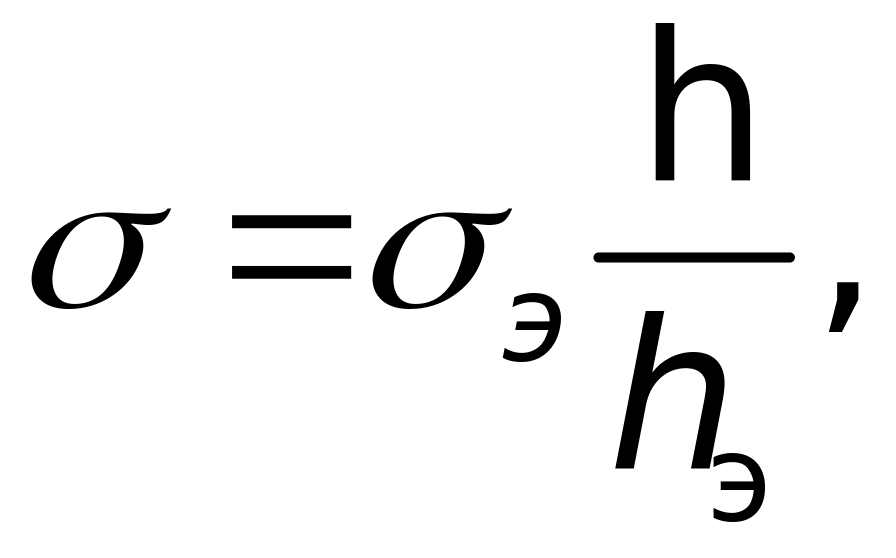
где э – поверхностное натяжение эталонной жидкости.
Любая гетерогенная система характеризуется определенным запасом поверхностной энергии. В изобарно-изотермических условиях
Gпов = ·S.
Условием самопроизвольного течения процессов при р и Т = const служит условие Gmax < 0. Следовательно, для рассматриваемых поверхностных процессов ·s 0, т.е. поверхностная энергия стремится самопроизвольно уменьшиться за счет уменьшения межфазной поверхности (S < 0) или поверхностного натяжения ( < 0).
Для системы жидкость – газ уменьшение поверхностной энергии возможно за счет обоих факторов. Так, поверхность жидкости может самопроизвольно уменьшаться при изменении формы тела (шарообразная форма капли). Поверхностное натяжение может также уменьшаться за счет увеличения концентрации растворенного вещества в поверхностном слое по сравнению с концентрацией в объемной фазе.
Мелкораздробленные твердые вещества, стремясь уменьшить поверхность, самопроизвольно агрегируют (слипаются). Твердые тела, как правило, уменьшают свою поверхностную энергию за счет снижения поверхностного натяжения благодаря адсорбции на поверхности веществ из газовой или жидкой фазы.
Процесс самопроизвольного изменения концентрации какого-либо вещества у поверхности раздела двух фаз называется адсорбцией.
Адсорбентом называется вещество, на поверхности которого происходит изменение концентрации другого вещества – адсорбата.
