
- •Часть 2
- •3. Металлургия магния Свойства и области приминения магния.
- •Удельная теплоемкость жидкого магния, Дж/моль:
- •Применение
- •Минералы магния
- •Обезвоживание хлорида магния (бишофита)
- •Обезвоживание карналлита
- •Поэтому процесс ведут в две стадии
- •Хлорирование окиси магния
- •Технологические схемы Карналитовая схема
- •Магнезитовая схема
- •Смешанная схема
- •Печь кс
- •Печь скн (Рис 19, 20.)
- •Хлоратор
- •Сравнение скн и хлоратора
- •3.1.Основы электрометаллургии магния Физико-химические свойства электролитов
- •Состав используемых электролитов
- •Показатели электролиза
- •Электродные процессы. Катодные процессы.
- •Анодные процессы
- •Процессы в объеме электролита
- •Влияние различных факторов на выход по току.
- •Конструкции магниевых электролизеров. Общие сведения.
- •Диафрагменные электролизеры
- •Диафрагменный электролизер с верхним вводом анодов.
- •Диафрагменный электролизер с боковым вводом анодов
- •Диафрагменный электролизер с нижним вводом анода
- •Общие плюсы диафрагменных (относительно бездиафрагменных)
- •Общие минусы
- •Бездиафрагменный электролизер
- •Технология электролиза Питание электролизера
- •Извлечение шлама
- •Извлечение магния
- •Регулировка температуры
- •Отсос газа из электролизера
- •Поточная технология электролиза карналлита
- •3.2. Рафинирование магния
- •3.3. Производство магния термическими способами
ФГАОУ ВПО «Уральский федеральный университет имени первого
Президента России Б.Н.Ельцина»
Кафедра Металлургии легких металлов
Основы электрометаллургии алюминия и магния
Часть 2
Конспект лекций для студентов всех форм обучения
направления 150400 – Металлургия
направления «Металлургия легких и тугоплавких металлов»
Екатеринбург
2011 г.
3. Металлургия магния Свойства и области приминения магния.
Впервые магний в составе амальгамы магния получил Х.Деви в 1808 году.
В 1829 г. А. Бюсси получил чистый металл восстановлением хлорида магния парами натрия.
MgCl2 + 2Na = 2NaCl + Mg
Электролизом расплавленного хлорида магния впервые магний получил М.Фарадей в 1830 году.
1852 г. Матиссен вместо MgCl2 подверг электролизу карналлит KCl - MgCl2, что улучшило показатели процесса.
1883 г. Гретцель предложил электролит NaCl - KCl - MgCl2 каждый компонент, которого придает особые свойства.
Сейчас используют, как правило, 4-х компонентные электролиты.
Магний – химический элемент второй группы периодической системы Менделеева; порядковый номер 12, атомная масса 24,305. Во всех устойчивых соединениях степень окисления магния +2.
Магний – металл серебристо белого цвета, обладающий гексагональной решеткой с плотной упаковкой.
а=0,320 нм

а с=0,520 нм
с/а=1,62
с b=0,319 нм
b
Рис. 3.1. Строение элементарной ячейки магния
Плотность, г/см3 при 20 0С…………………………...…1,738
То же при 650 0С……………………………………...….1,590
Температура плавления 0С……………………..………..650
Температура кипения 0С………………………….……..1107
Теплота плавления, кДж/моль………………………..…8,96
Теплота испарения, кДж/моль…………………….……133,98
Теплопроводность, 200с Вт/(моль·К)……………………157
Удельное электр. сопротивление при 200С, мкОм/см…4,45
Электрохимический эквивалент, г/(А·ч)………………..0,454
Удельная теплоемкость твердого магния до температуры плавления, Дж/моль:
Сртв = 22,32 + 0,01026 Т – 0,43·105 Т-2
Удельная теплоемкость жидкого магния, Дж/моль:
Срж = 33,15 + 0,83
Линейный коэффициент термического расширения 25·10-6 м/ 0С.
По удельной прочности Mg превосходит все металлы.
Магниевые сплавы немагнитны и не дают искры при ударах и трении и хорошо воспринимают ударные нагрузки.
На воздухе медленно окисляется, покрывась тонкой пленкой оксида.
2Mg + O2 = MgO
(Мольн. отн. MgO/Mg=0,79 окись не защищает от окисления)
Температура воспламенения на воздухе 623С.
С повышением температуры скорость окисления увеличивается и особенно быстро свыше 350 0С. Заметное влияние на скорость окисления оказывает влага, содержащаяся в воздухе.
С кипящей водой взаимодействует с выделением водорода и с образованием студенистого осадка гидроксида.
Mg + H2O = MgO + H2 (при температуре свыше 380 0С резко ускоряется)
MgO + H2O = Mg(OH)2 ( в природе брусит)
В слитках или изделиях магний не огнеопасен, но легко загорается в расплавленном или порошкообразном состоянии.
Интенсивно растворяется во всех минеральных кислотах, кроме плавиковой (образуется труднорастворимый MgF2)
Mg + HCl = MgCl2 + H2
В растворах едких щелочей магний химически стоек вплоть до температуры кипения.
C водородом: Mg + H2 500C MgH2 600C Mg + H2
Водород хорошо растворим в Mg: 30 см3 в 100 г (ж)
10 см3 в 100 г (тв)
На коррозионную стойкость магния сильное влияние оказывают примеси, в особенности железо, никель, медь, а также хлориды.
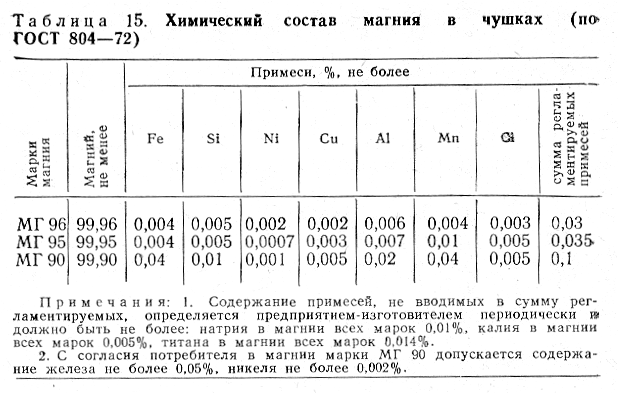
Таблица 3.1. Химический состав магния в чушках
Магний долгое время оставался стратегическим металлом, использовался в основном в военной технике. Во время 1-ой Великой Отечественной в мире производилось сотни тонн, перед 2-ой Мировой – 22 тыс. тонн (60% Германия, 15% Япония). К концу 2-ой Мировой – 230 тыс. тонн. После войны производство упало до 8 тыс. тонн. 1970- 160 тыс. тонн, 1999 – 400 тыс. тонн.
Таблица 3.2. Мировой объем производства магния в 2000 г.
Страна |
Общий объем, тыс.т |
Объем терм, тыс.т |
Китай |
193 |
190 |
США |
74 |
36 |
Канада |
55 |
7 |
Норвегия |
50 |
0 |
Россия |
40 |
0 |
Франция |
17 |
17 |
Казахстан |
10 |
0 |
Бразилия |
9 |
9 |
Украина |
2 |
0 |
