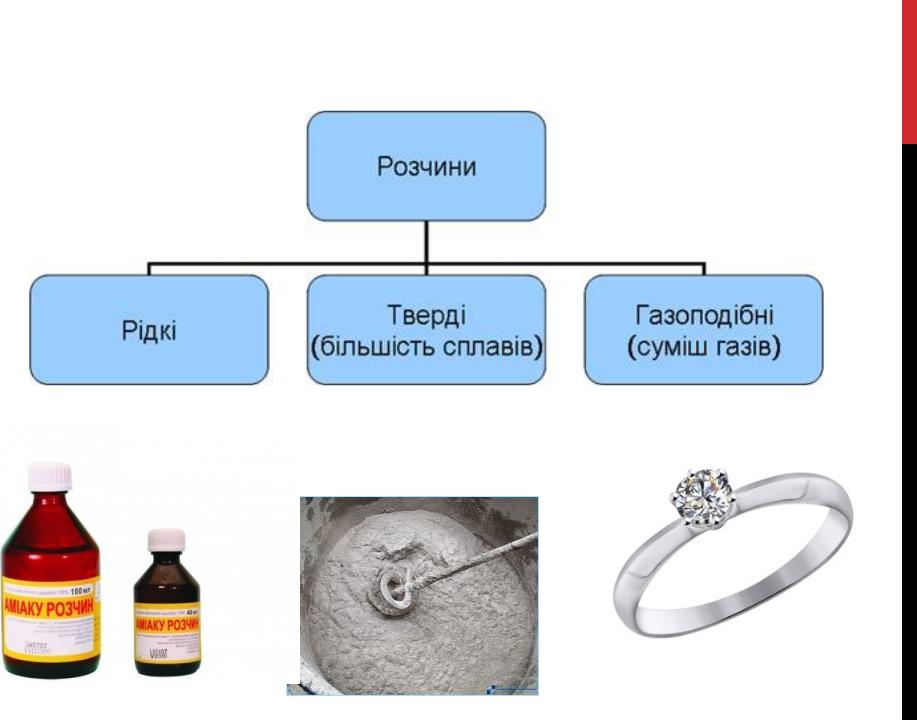
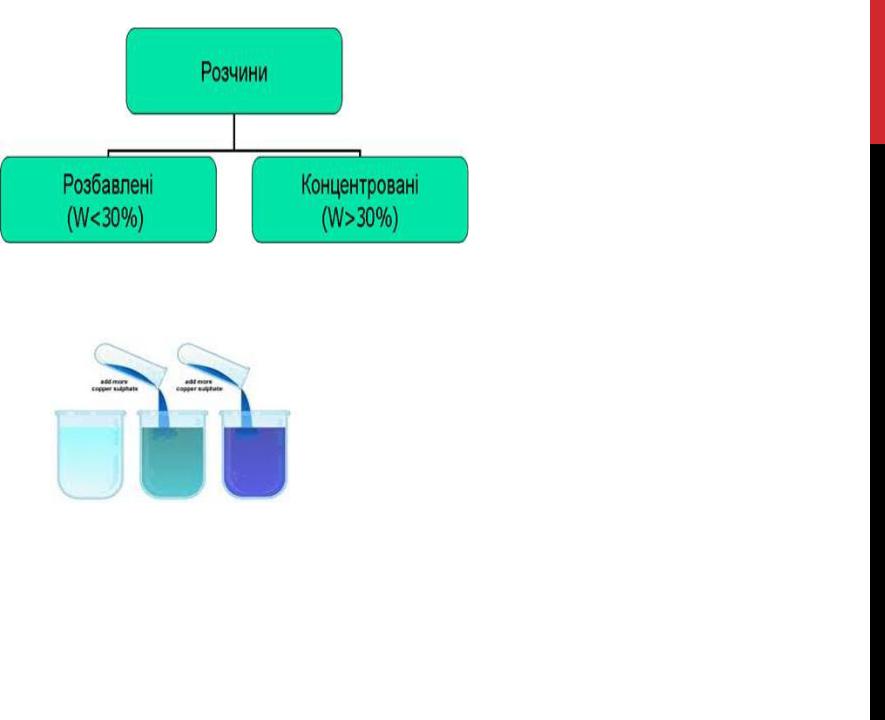
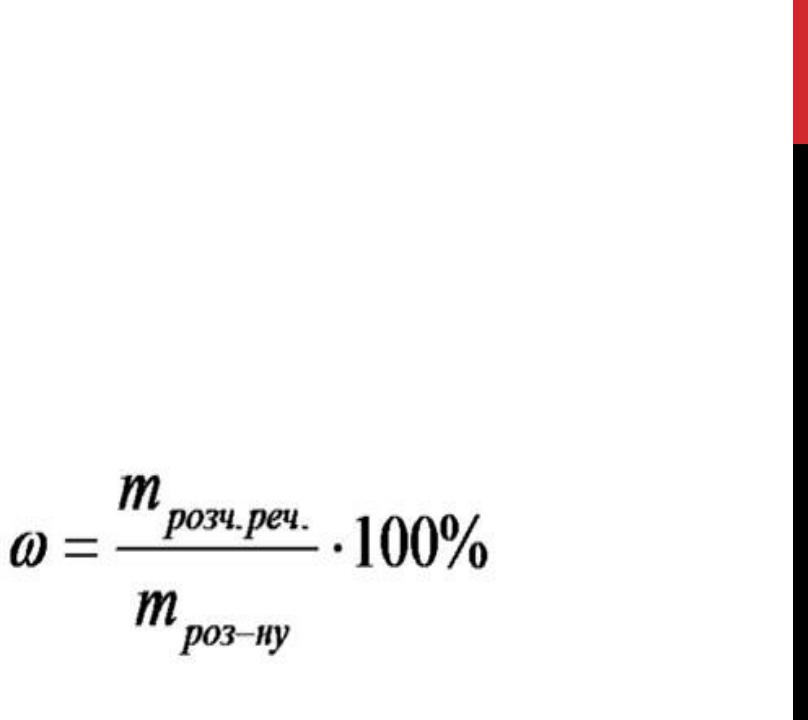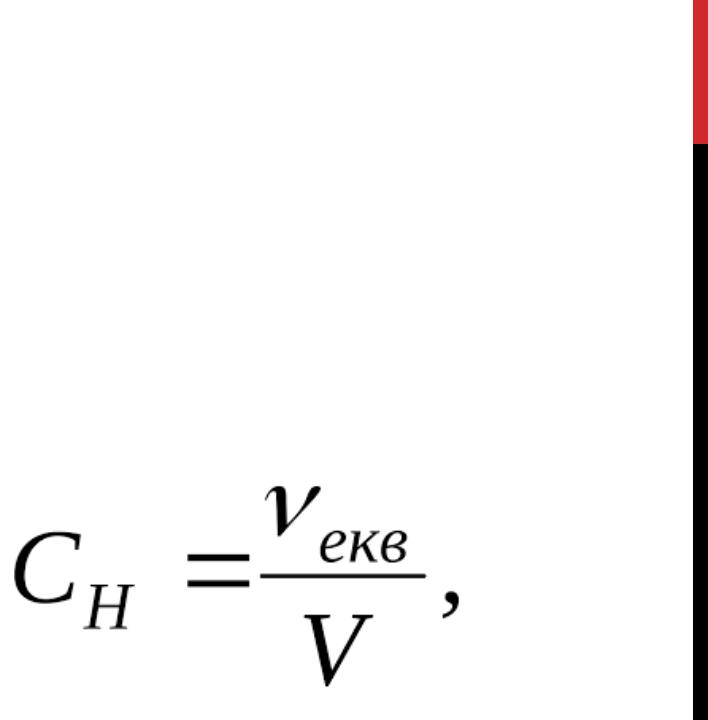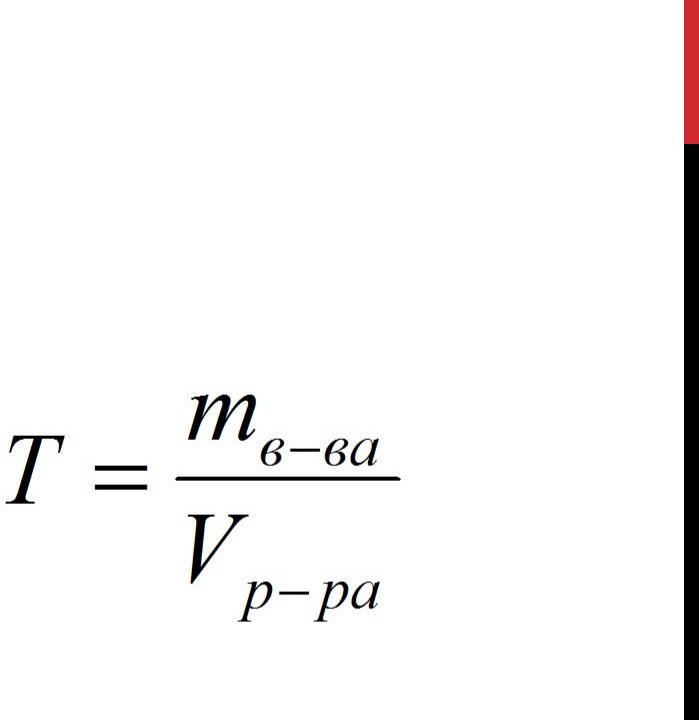Розчином
називається рідка або тверда гомогенна система, що складається з двох або більше компонентів.
Розчин складається з:
1.Розчинник
2.Розчинена речовина
СПОСОБИ ВИРАЖЕННЯ КІЛЬКІСНОГО СКЛАДУ РОЗЧИНІВ.
1.МАСОВА ЧАСТКА
2.МОЛЯРНА КОНЦЕНТРАЦІЯ
3.ЕКВІВАЛЕНТНА КОНЦЕНТРАЦІЯ АБО НОРМАЛЬНІСТЬ.
МАСОВА ЧАСТКА – ЦЕ ВІДНОШЕННЯ МАСИ РОЗЧИНЕНОЇ РЕЧОВИНИ ДО МАСИ РОЗЧИНУ.
МАСОВА ЧАСТКА ВИМІРЮЄТЬСЯ У % АБО ЧАСТКАХ ОДИНИЦІ.
100%=1; 50%=0,5; 5%=0,05.
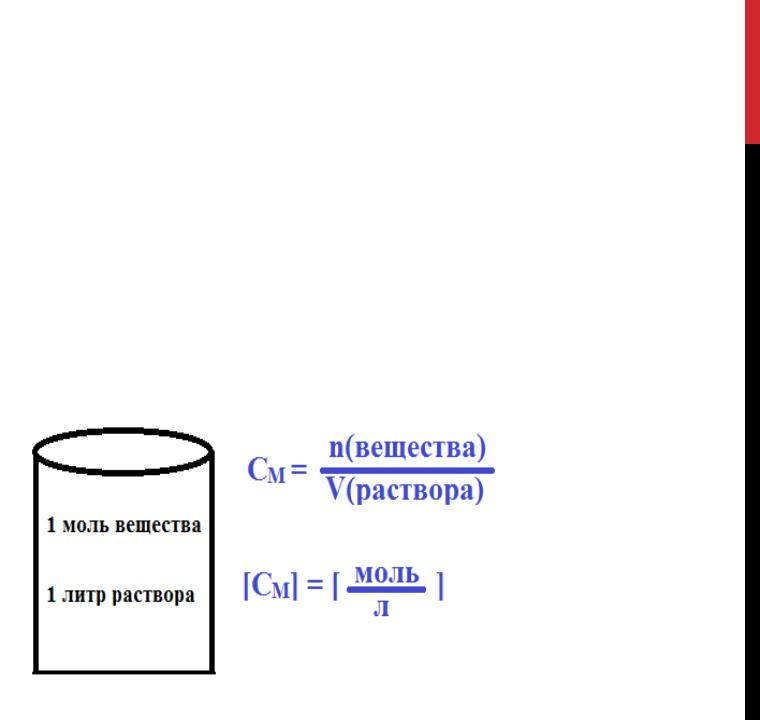
МОЛЯРНА КОНЦЕНТРАЦІЯ -
ЦЕ КІЛЬКІСТЬ МОЛЕЙ РОЗЧИНЕНОЇ РЕЧОВИНИ В 1Л РОЗЧИНУ. (МОЛЬ/Л),
ЇЇ ПОЗНАЧАЮТЬ ЛІТЕРОЮ М.
ЕКВІВАЛЕНТНА КОНЦЕНТРАЦІЯ АБО НОРМАЛЬНІСТЬ – ЦЕ КІЛЬКІСТЬ
ЕКВІВАЛЕНТІВ РОЗЧИНЕНОЇ РЕЧОВИНИ В 1Л РОЗЧИНУ.