
- •Тема 1. Молекулярно-кінетична теорія ідеального газу.
- •Тема2.Основи термодинаміки.
- •Ізохорний процес .
- •Ізобарний процес .
- •Ізотермічний процес .
- •Тема 3.Електростатика.
- •Паралельне з’єднання конденсаторів.
- •Послідовне з’єднання конденсаторів.
- •Тема 4.Постійний струм.
- •. Енергетичні зони в кристалах
- •Розподіл електронів по енергетичних зонах. Валентна зона і зона провідності. Метали, діелектрики і напівпровідники
- •Власна провідність напівпровідників
- •§142. Домішкова провідність напівпровідників
- •Тема 5.Магнітостатика.
- •1. Магнітне поле прямолінійного провідника зі струмом.
- •2. Магнітне поле колового струму.
- •Тема 6.Електромагнітна індукція. Магнітні властивості речовини.
- •Тема 7.Основи теорії Максвела для електромагнітного поля.
- •Тема 8.Механічні і електромагнітні коливання.
- •Тема 9.Хвилі. Елементи хвильової оптики.
- •Смуги однакового нахилу
- •§2.1.4. Смуги однакової товщини
- •Кільця Ньютона
- •Дифракція Фраунгофера на одній щілині
- •Дифракція світла на дифракційній гратці
- •Тема 10. Основи квантової оптики.
- •Тема 11.Будова атома за Резерфордом-Бором.
- •Тема 12. Основи квантової механіки.
- •Тема 13.Елементи фізики атомного ядра.
Тема 11.Будова атома за Резерфордом-Бором.
1.Досліди Резерфорда і ядерна модель атома.
Перша спроба
створення моделі атома на основі
нагромаджених експериментальних даних
належить Дж. Томсону
(1903р.). Згідно з цією моделлю атом є
рівномірно зарядженою кулею радіусом
~![]() ,
всередині якої біля своїх положень
рівноваги коливаються електрони;
сумарний від’ємний заряд електронів
дорівнює додатному заряду кулі.
Модель Томсона виявилась неправильною.
,
всередині якої біля своїх положень
рівноваги коливаються електрони;
сумарний від’ємний заряд електронів
дорівнює додатному заряду кулі.
Модель Томсона виявилась неправильною.
Велику роль у розвитку уявлень про будову атома відіграли досліди Е. Резерфорда із вивчення розсіяння a- частинок в речовині.
a-частинки утворюються під час природного радіоактивного розпаду деяких важких елементів і є позитивно зарядженими частинками з зарядом 2е і масою, яка приблизно в чотири рази більша за масу атома водню.
Спрощена схема досліду Резерфорда зображена на рис. 281.
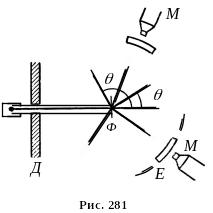
Джерело a-
частинок поміщене всередині свинцевої
порожнини з вузьким каналом. Усі
a-частинки,
крім тих, що рухаються всередині вузького
каналу, поглинаються свинцем. Потік
a-частинок,
пройшовши через вузьку діафрагму Д,
потрапляє на тонку золоту фольгу Ф
завтовшки
![]() ,
що складається з декількох атомних
шарів. При проходженні через фольгу
a-частинки
відхиляються на різні кути
,
що складається з декількох атомних
шарів. При проходженні через фольгу
a-частинки
відхиляються на різні кути
![]() і потрапляють на екран Е,
який можна поміщати в різних положеннях
відносно фольги. Екран покритий
флюоресцентною речовиною. За допомогою
мікроскопа М
можна спостерігати місця
потрапляння a-частинок
за свіченням екрану. Поведінку a-частинок
після проходження через фольгу вивчали
в камері Вільсона.
і потрапляють на екран Е,
який можна поміщати в різних положеннях
відносно фольги. Екран покритий
флюоресцентною речовиною. За допомогою
мікроскопа М
можна спостерігати місця
потрапляння a-частинок
за свіченням екрану. Поведінку a-частинок
після проходження через фольгу вивчали
в камері Вільсона.
Резерфорд з’ясував, що потік a-частинок, пройшовши крізь фольгу, майже не відхиляється від прямолінійного напрямку і лише деякі частинки змінють напрямок руху, відхиляючись на дуже великі кути, близько 135 – 150°(рис. 282).
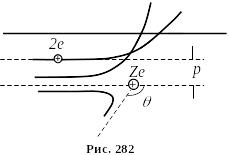
На підставі досліду Резерфорд зробив такі висновки.
Оскільки переважна більшість a-частинок проходить через атоми, не змінюючи свого напрямку, то атом прозорий і частинки, на яких відбувається розсіювання, займають об’єм значно менший за об’єм атома.
Тому що при розсіюванні спостерігаються кути відхилення a-частинок близько 150°, то взаємодіють одноіменно заряджені частинки, тобто розсіювання відбувається на позитивно заряджених частинках.
Після проходження a-частинкою фольги в камері Вільсона спостерігалися треки однакової довжини, які належать лише a-частинці. Отже, маса частинки, на якій відбувається розсіювання, значно більша від маси a-частинки і через це вона не отримує прискорення.
Резерфорд приблизно розрахував розмір частинки, на якій відбувається розсіювання. Розглянемо центральний удар a-частинки, який відповідає куту розсіяння
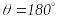 .
Із закону збереження енергії випливає,
що в момент найбільшого зближення
a-частинки
з невідомою частинкою її кінетична
енергія
.
Із закону збереження енергії випливає,
що в момент найбільшого зближення
a-частинки
з невідомою частинкою її кінетична
енергія
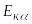 цілком перейде в потенціальну енергію
їх взаємодії:
цілком перейде в потенціальну енергію
їх взаємодії:
![]() .
.
Оцінимо величину
R
для золота
![]() .
Якщо
припустити, що швидкість a-частинки
.
Якщо
припустити, що швидкість a-частинки
![]() ,
її маса
,
її маса
![]() ,
заряд електрона
,
заряд електрона
![]() ,
то
,
то
![]() .
.
В той же час, радіус
атома
![]() .
.
Таким чином, частинка на якій відбувається розсіювання a-частинок займає в атомі об’єм, який значно менший від об’єму атома.
Резерфорд теоретично розглянув задачу про розсіювання a-частинок у кулонівському електричному полі частинки, що має заряд Q. Кут відхилення a- частинок тим більший, чим менша віддаль p від ядра до початкового напрямку руху a-частинки (рис. 282). Віддаль p називається „параметром удару”.
Закони динаміки
дозволяють розрахувати залежність кута
відхилення
від параметра удару р,
а методами теорії ймовірностей можна
знайти ймовірність пролітання a-частинки
на даній відстані р
від частинки і тим самим ймовірність
її відхилення на кут
.
Розрахунок показує, що із загального
числа розсіяних N
a-частинок
в тілесному куті
![]() ,
що міститься між двома конічними
поверхнями, твірні які утворюють кути
і
,
що міститься між двома конічними
поверхнями, твірні які утворюють кути
і
![]() з початковим напрямком руху a-частинок,
розсіюється така їх кількість:
з початковим напрямком руху a-частинок,
розсіюється така їх кількість:
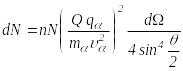 ,
,
де n – кількість a-частинок, які налітають на частинку через одиницю площі поперечного перерізу пучка за одиницю часу.
Для певної розсіюючої
речовини при певній енергії a-частинок
і заданій
густині їх потоку добуток
![]() повинен бути сталим, що було експериментально
підтверджено в дослідах Гейгера і
Марсдена.
повинен бути сталим, що було експериментально
підтверджено в дослідах Гейгера і
Марсдена.
Наведена формула
дозволяє за виміряним числом частинок,
які розсіяні під певним кутом
,
визначити величину позитивного заряду
![]() ,
тому, що всі інші величини, що входять
у цю формулу, доступні вимірюванню.
Оскільки атоми в нормальному стані
нейтральні, то позитивний заряд
повинен бути цілим кратним від значення
заряду електрона:
,
тому, що всі інші величини, що входять
у цю формулу, доступні вимірюванню.
Оскільки атоми в нормальному стані
нейтральні, то позитивний заряд
повинен бути цілим кратним від значення
заряду електрона:
![]() ,
,
де Z
– ціле число. На основі вимірювань
Резерфорда виникла гіпотеза, що величина
Z
дорівнює порядковому номеру елементу
в таблиці Менделєєва. Пізніше ця гіпотеза
підтвердилася.Знаючи заряд частинки
![]() ,
можна знайти, який „параметр удару”
відповідає різним кутам удару
.
,
можна знайти, який „параметр удару”
відповідає різним кутам удару
.
На підставі результатів дослідів з розсіянням a-частинок тонкими фольгами Резерфорд запропонував ядерну модель атома.
Згідно з цією
моделлю в центрі атома знаходиться
ядро, в якому зосереджено позитивний
заряд Ze
і практично
вся маса атома. Лінійні розміри ядра
~![]() .
.
Навколо ядра в області з лінійними розмірами ~ по замкнених орбітах рухаються Z електронів, утворюючи електронну оболонку атома.
Ядерна модель Резерфорда зовні дуже нагадує Сонячну систему: у центрі – ядро, навколо нього по орбітах рухаються електрони. Тому цю модель називають планетарною. Орбіти електронів в атомі стаціонарні, атому властива виняткова стійкість.
Стійкість атома
не можна погодити з класичним поясненням
ядерної моделі. Електрон по коловій
орбіті рухається з доцентровим
прискоренням
![]() ,
а згідно із законами електродинаміки
він повинен випромінювати електромагнітні
хвилі і внаслідок цього неперервно
втрачати енергію. За класичними
уявленнями це випромінювання повинно
відбуватися безперервно. Тому електрон
не зможе триматись на коловій орбіті –
він повинен по спіралі наближатись до
ядра, і частота його обертання навколо
ядра повинна безперервно змінюватись.
Електромагнітне випромінювання атома
тому повинно мати неперервний, а не
лінійчастий спектр.
,
а згідно із законами електродинаміки
він повинен випромінювати електромагнітні
хвилі і внаслідок цього неперервно
втрачати енергію. За класичними
уявленнями це випромінювання повинно
відбуватися безперервно. Тому електрон
не зможе триматись на коловій орбіті –
він повинен по спіралі наближатись до
ядра, і частота його обертання навколо
ядра повинна безперервно змінюватись.
Електромагнітне випромінювання атома
тому повинно мати неперервний, а не
лінійчастий спектр.
Отже, застосування класичної електродинаміки до ядерної моделі атома привело до суперечності з експериментальними фактами.
2.Постулати Бора та їх дослідне підтвердження.
Перша спроба побудови якісно нової теорії атома була зроблена в 1913 р. Н.Бором. Він поставив перед собою мету зв’язати в єдине ціле емпіричні закономірності лінійчастих спектрів, ядерну модель атома Резерфорда і квантовий характер випромінювання та поглинання світла.
В основу своєї теорії Бор поклав три постулати.
Перший постулат
Бора (постулат стаціонарних станів):
існують деякі стаціонарні стани атома
з відповідними значеннями енергії
![]() перебуваючи в яких, він не випромінює
енергії.
перебуваючи в яких, він не випромінює
енергії.
Цим стаціонарним станам відповідають цілком визначені (стаціонарні) орбіти, по яких рухаються електрони, які, незважаючи на наявність у них прискорення, електромагнітних хвиль не випромінюють.
Другий постулат Бора (правило квантування орбіт): в стаціонарному стані атома електрон, рухаючись по коловій орбіті, повинен мати квантові значення моменту імпульсу, які задовольняють умову
![]() ,
,
![]() ,
,
![]() ,
,
де m
– маса електрона,
![]() – його швидкість,
– його швидкість,
![]() – радіус орбіти електрона.
– радіус орбіти електрона.
Третій постулат
Бора (правило частот): при переході атома
з одного стаціонарного стану в інший
випромінюється або поглинається один
фотон з
енергією
![]() ,
яка дорівнює різниці енергій відповідних
стаціонарних станів.
,
яка дорівнює різниці енергій відповідних
стаціонарних станів.
Випромінювання
фотона відбувається при переході атома
зі стану з більшою енергією
![]() у стан з меншою енергією
у стан з меншою енергією
![]() ,
тобто при переході електрона з орбіти
більш віддаленої від ядра на ближчу до
ядра орбіту. Поглинання енергії
супроводжується переходом атома у стан
з більшою енергією, і електрон
переходить на віддаленішу від ядра
орбіту. Набір можливих частот
,
тобто при переході електрона з орбіти
більш віддаленої від ядра на ближчу до
ядра орбіту. Поглинання енергії
супроводжується переходом атома у стан
з більшою енергією, і електрон
переходить на віддаленішу від ядра
орбіту. Набір можливих частот
![]() квантових переходів і визначає лінійчастий
спектр атома.
квантових переходів і визначає лінійчастий
спектр атома.
Постулати, висунуті Бором, дозволили розрахувати спектр атома водню і воднеподібних систем, а також теоретично розрахувати сталу Рідберга.
