
- •4 Структура и свойства биологических мембран
- •4.1 Состав и функции биологических мембран
- •5.Генерация и проведение биопотенциалов.
- •4.2 Строение биологических мембран
- •4.3 Физическое состояние и фазовые переходы липидов в мембранах
- •4.4 Особенности межмолекулярных взаимодействий в мембранах
- •4.5 Модельные липидные мембраны
5.Генерация и проведение биопотенциалов.
6.Рецепторная (механическая, акустическая, обонятельная, зрительная, химическая, терморецепция).
4.2 Строение биологических мембран
Совокупность результатов, полученных физическими и химическими методами исследования, дала возможность предложить жидкостно-мозаичную модель строения биологических мембран (Сингер и Никольсон, 1972 г.). Согласно авторам, структурную основу биологической мембраны образует двойной слой фосфолипидов, инкрустированный белками (рис.4.1).
Липиды находятся при физиологических условиях в жидком агрегатном состоянии. Это позволяет сравнить мембрану с фосфолипидным морем, по которому «плавают» белковые молекулы. Одним из подтверждений жидкостно-мозаичной модели является то, что в разных мембранах соотношение между содержанием белков и фосфолипидов сильно отличается. В миелиновой мембране белков в 2,5 раза меньше, а в эритроцитах белков в 2,5 раза больше, чем липидов.
Большинство, хотя и не все липиды в мембране, расположены по принципу двойного слоя (бислоя).

Рис.4.1.Жидкостно-мозаичная модель плазматической мембраны.
Молекула фосфолипида лецитина содержит полярную голову (соединение – производное фосфорной кислоты) и длинный неполярный хвост (остатки жирных кислот). В голове фосфолипидной молекулы имеются две заряженные группы, расположенные на некотором расстоянии друг от друга. Два разноименных заряда, равные по абсолютной величине, образуют электрический диполь.

Рис. 4.2. Схематичное изображение «двухвостовой» фосфолипидной молекулы (а) и схема образования бислойной мембраны из таких молекул (б).
Полярные головы молекул фосфолипидов гидрофильные, а неполярные хвосты - гидрофобные. В смеси фосфолипидов с водой термодинамически выгодно, чтобы полярные головы были погружены в состоящую из полярных молекул воду, а их неполярные хвосты были бы расположены далеко от воды. Такое расположение амфифильных (имеющих гидрофильную и гидрофобную части) молекул соответствует наименьшему значению энергии Гиббса по сравнению с другими возможными расположениями.
Очень существенным является то обстоятельство, что молекулы фосфолипидов имеют два хвоста. Такая молекула в пространстве имеет форму, близкую к цилиндру (рис.4.2). Из молекул фосфолипидов в водной среде происходит самосборка бислойной мембраны. Присутствие молекул с одним хвостом (лизолецитин), имеющих в пространстве форму, близкую к конусу, разрушает клеточные мембраны (рис. 4.3). Фосфолипидные молекулы, лишенные одного хвоста, образуют поры в мембране. При этом нарушается их барьерная функция.

Рис.4.3. Схематичное изображение «однохвостовой» фосфолипидной молекулы (а) и схема образования поры в мембране из «однохвостовых» молекул (б).
4.3 Физическое состояние и фазовые переходы липидов в мембранах
Твердое тело может быть как кристаллическим, так и аморфным. В первом случае имеется дальний порядок в расположении частиц на расстояниях, много превышающих межмолекулярные расстояния (кристаллическая решетка). Во втором – нет дальнего порядка в расположении атомов и молекул.
Различие между аморфным телом и жидкостью состоит не в наличии или отсутствии дальнего порядка, а в характере движения частиц. Молекулы жидкости и твердого тела совершают колебательные (иногда вращательные) движения около положения равновесия. Через некоторое среднее время («время оседлой жизни») происходит перескок молекул в другое положение равновесия. Различие заключается в том, что «время оседлой жизни» в жидкости намного меньше, чем в твердом состоянии.
Липидные двухслойные мембраны при физиологических условиях – жидкие, «время оседлой жизни» фосфолипидной молекулы в мембране составляет 10−7- 10−8 с.
Молекулы в мембране расположены не беспорядочно, в их расположении наблюдается дальний порядок. Фосфолипидные молекулы находятся в двойном слое, а их гидрофобные хвосты примерно параллельны друг другу. Есть порядок и в ориентации полярных гидрофильных голов.
Физиологическое состояние, при котором есть дальний порядок во взаимной ориентации и расположении молекул, но агрегатное состояние жидкое, называется жидкокристаллическим состоянием. Жидкие кристаллы могут образовываться не во всех веществах, а в веществах из «длинных молекул» (поперечные размеры которых меньше продольных). Могут существовать различные жидкокристаллические структуры (рис.4.4, б, в, г): нематическая (нитевидная), когда длинные молекулы ориентированы параллельно друг другу; смектическая – молекулы параллельны друг другу и располагаются слоями; холестическая – молекулы располагаются параллельно друг другу в одной плоскости, но в разных плоскостях ориентации молекул разные.

Рис.4.4. Расположение молекул в аморфном (а), и жидкокристаллическом состоянии (б, в, г).
Двуслойная липидная фаза мембран соответствует смектическому жидкокристаллическому состоянию.
Жидкокристаллические структуры очень чувствительны к изменению температуры, давления, химического состава, электрического поля. Например, при понижении температуры в фосфолипидной мембране происходит переход из жидкокристаллического в гель-состояние (рис.4.5). В гель-состоянии молекулы расположены еще более упорядоченно, чем в жидкокристаллическом. Все углеводородные гидрофобные хвосты фосфолипидных молекул в гель-фазе полностью вытянуты строго параллельно друг другу (имеют полностью транс-конформацию). В жидком кристалле за счет теплового движения возможны транс-гош-переходы, хвосты молекул изгибаются, их параллельность в отдельных местах нарушается и особенно сильно в середине мембраны.
Толщина мембраны в гель-фазе больше, чем в жидком кристалле. Однако при переходе из твердого в жидкокристаллическое состояние объем несколько увеличивается, потому что возрастает площадь мембраны (в расчете на одну молекулу площадь возрастет с 0,48 до 0,58 нм2). Так как в твердокристаллическом состоянии упорядоченность в строении выше, чем в жидком кристалле, ему соответствует меньшая энтропия.
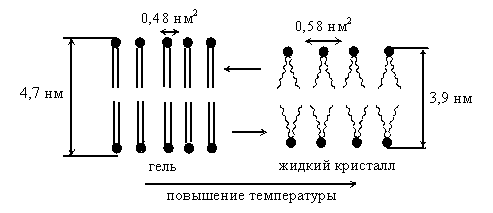
Рис.4.5.Изменение структуры мембраны при переходе из жидкокристаллического состояния в гель-состояние и обратно при изменении температуры.
Для нормального функционирования мембрана должна быть в жидкокристаллическом состоянии. Поэтому в живых системах при продолжительном понижении температуры окружающей среды наблюдается адаптационное изменение химического состава мембран в результате обмена веществ. Это обеспечивает понижение температуры фазового перехода. Температура фазового перехода понижается при увеличении числа ненасыщенных связей в составе жирных кислот в фосфолипидах. Температура фазового перехода гель – жидкий кристалл может изменяться от – 20 ºС (для мембран из ненасыщенных липидов) до + 60 ºС (для насыщенных липидов). Увеличение числа ненасыщенных липидов в мембране при понижении температуры среды обитания наблюдается у всех организмов.
Гипотеза петли (кинка). Плавление жирнокислотных цепей при фазовом переходе обусловлено вращательной изомерией. Наименьшей энергией обладает транс-, а наибольшей - цис-конформация. Гош-конформации [гош (+) и гош (−) - это поворот на ±120° относительно транс – конформации]. Синоним гош-конформации – скошенная конформация. Он сравнительно мало превышают по энергии транс-конформацию (на 2-3 кДж/моль), но эти состояния разделяет энергетический барьер высотой ~ 12-17 кДж/моль. Если углеводородные цепи, находящиеся полностью в транс-конформации представляют собой линейные структуры, то появление одиночной гош-конформации в цепи приводит к искривлению пространственной конфигурации цепи на угол ~ 120°. В плотно упакованных мембранных системах с полностью транс-конформацией углеводородных цепей это искривление порождает серьезные стереохимические затруднения, делающие невозможным появление одиночных гош-конформаций.
Уменьшение стереохимических затруднений при плавлении углеводородных цепей в мембранах достигается при синхронном появлении в цепи сразу двух гош-конформаций [гош (+) и гош (−)], разделенных одиночной С − С-связью в транс-конформации. Хотя энергия такого состояния вдвое выше одиночной гош-конформации, возникает ротационное состояние цепи. Оно не вызывает сильного расширения решетки, так как при последовательном повороте цепи на +120 и −120° пространственная конфигурация цепи в целом сохраняется прямолинейной (рис.4.6, А). Участок цепи, находящийся в гош (+)-транс-гош (−)-конформации, формирует уступ или петлю в углеводородной цепи, которую часто называют кинком (от английского kink —петля).

Рис.4.6. А: 1 - углеводородные цепи полностью в транс-конформации, 2 - в гош-транс-гош-конформации, 3 – в цис-транс-гош-конформации; Б: кинк-блоки в углеводородных цепях мембран: 1 - в одном монослое мембраны; 2 – в двух монослоях липидного бислоя.
Образование кинка сопровождается уменьшением эффективной длины цепи на ~ 0,127 нм. При этом часть цепи отодвигается на ~ 0,15 нм, образуя свободный объем, а занимаемый молекулой липида общий объем увеличивается на 0,025-0,050 нм3. Хотя появления одного кинка в углеводородной цепи недостаточно для ее плавления, однако одиночные кинки облегчают возникновение кинков в соседних углеводородных цепях, формируя чередующиеся кинк-блоки (рис. 4.6, Б). Такие блоки могут возникать либо в одном монослое мембраны, либо в двух противоположно расположенных углеводородных слоях (в бислое). При увеличении числа кинков в углеводородных цепях неупорядоченность углеводородной зоны мембран резко нарастает.
Двойные (цис-) связи в жирнокислотных ненасыщенных цепях мембран могут играть роль зародышей образования кинков в соседних насыщенных цепях. В этом случае для образования кинка в ненасыщенной цепи необходимо появление лишь одной гош-конформации при искривлении цепи на 80°. При этом устраняются стереохимические затруднения, возникающие при размещении ненасыщенной цепи в углеводородной зоне мембран из насыщенных липидов. Это хорошо согласуется с экспериментально наблюдаемым резким снижением температуры фазового перехода мембран из насыщенных липидов при добавлении к ним небольших количеств ненасыщенных жирнокислотных цепей – мембрана становится более рыхлой. Поворот вокруг С − С-связи с образованием транс-конформации практически исключен.
