
- •Решебник
- •Ростов-на-Дону
- •Кандидат физико-математических наук
- •Внутреннее строение вещества
- •Введение в теорию идеального газа
- •Основы термодинамики
- •Статистические закономерности в термодинамике
- •Реальные газы
- •Явления переноса
- •Развернутое изложение методов решения физических задач по молекулярной физике
- •Внутреннее строение вещества
- •Классификация кристаллов
- •Физические типы кристаллических решеток
- •Введение в теорию идеального газа
- •Статистические закономерности
- •Решение.
- •Поток теплоты на единицу длины цилиндров
- •Основы термодинамики
- •Поток тепла, проходящий через него, в силу закона Фурье равен
- •Реальные газы
Решение.
Подставив в уравнение Менделеева – Клапейрона P=b/Vn, получим:
![]()
Выразим температуру из последнего уравнения:
![]()
Отсюда ясно, что если n<1, то при расширении газа температура увеличивается, если же n>1, температура уменьшается.
2.12. Давление воздуха внутри бутылки, закрытой пробкой, равно 0,1 МПа при температуре 70С. На сколько градусов нужно нагреть воздух в бутылке, чтобы пробка вылетела? Без нагревания пробку можно вынуть, прикладывая к ней силу 30 Н. Сечение пробки 2 см2.
Решение.
Чтобы
пробка вылетела из бутылки, необходимо,
чтобы давление воздуха в бутылке
равнялось:
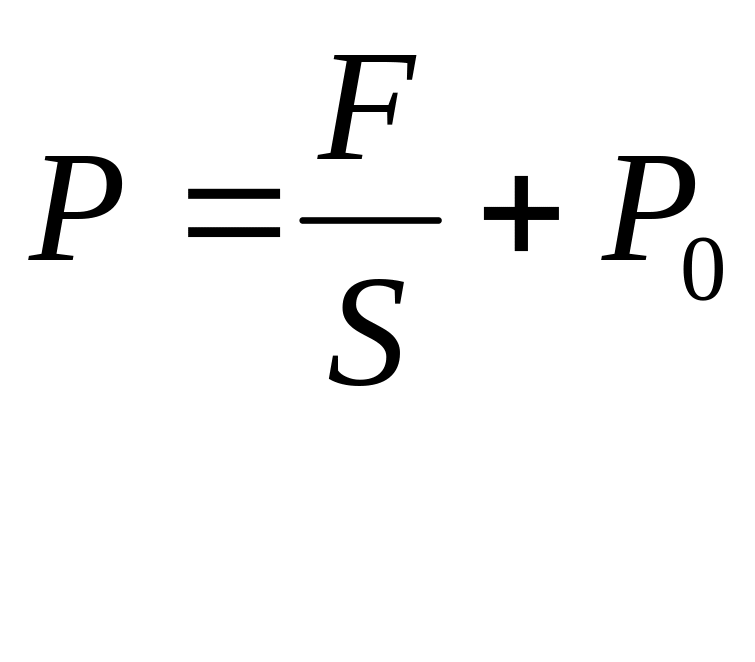
При нагревании объем не изменяется. По закону Шарля:
![]()
откуда:
![]()
Следовательно:
![]() =
420К.
=
420К.
2.13. В баллоне емкостью 110 л помещено 0,8 кг водорода, и 1,6 г кислорода. Определить давление смеси на стенки сосуда, если температура окружающей среды 270С.
Решение.
Согласно закону Дальтона, давление смеси равно сумме парциальных давлений: Р=Р1 +Р2.
Здесь:
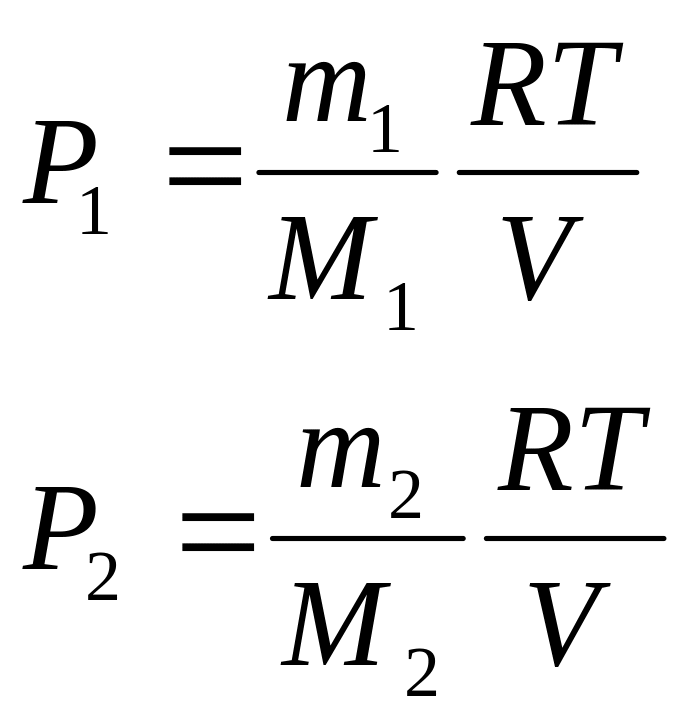
Тогда
имеем:
![]() .
.
2.14. Сколько молекул ртути содержится в 1 см3 воздуха в помещении, зараженном ртутью, при температуре 20° С, если давление пара ртути при этой температуре равно 0,645 Па? Число Авогадро NA = 6,023■ 1023 молек/г-моль.
Решение.
Из условия задачи вытекает, что давление и температура воздуха близки к нормальным, т. е. в этом случае воздух с хорошим приближением можно рассматривать как смесь идеальных газов, для которых справедлив закон Дальтона.
Пусть
в объеме V
содержится
N
молекул
ртути, имеющих суммарную массу m.
Тогда
![]()
и, следовательно, число молекул ртути в единице объема
![]() .
.
2.15. Определить давление и молекулярный вес смеси газов, состоящей из 10 г кислорода и 10 г азота, которые занимают объем 20 л при температуре 150° С.
Решение.
По
закону Дальтона
![]() .
.
Придав
правой части вид, совпадающий с уравнением
состояния идеального газа,
![]()
где
по смыслу
![]() ,
находим для молекулярного веса смеси
,
находим для молекулярного веса смеси
![]() .
.
2.16.
Пространство
между двумя достаточно длинными
цилиндрами с радиусами R1
и R2
заполнено
идеальным газом, коэффициент
теплопроводности которого равен
![]() .
Тмепература внешнего цилиндра Т2
,
внутреннего – Т1
(Т1
> Т2).
Считая,
конвекция газа отсутствует, а длина
свободного пробега молекул газ меньше
расстояния между цилиндрами, найти
тепловой поток ql,
приходящийся на единицу длины цилиндров.
.
Тмепература внешнего цилиндра Т2
,
внутреннего – Т1
(Т1
> Т2).
Считая,
конвекция газа отсутствует, а длина
свободного пробега молекул газ меньше
расстояния между цилиндрами, найти
тепловой поток ql,
приходящийся на единицу длины цилиндров.
Решение.
Температуры внешнего и внутреннего цилиндров постоянны, поэтому в пространстве между ними устанавливается постоянное распределение температур Т(г), где г — расстояние до оси цилиндров. Поток тепла не будет зависеть от времени, т. е. процесс стационарный.
Выделим мысленно цилиндр радиусом, коаксиальный с данными цилиндрами, все точки которого имеют одинаковую температуру Т (r).Тепловой поток, проходящий через этот цилиндр,
![]() ,
,
где
— коэффициент теплопроводности; S
=
![]() —
площадь
поверхности цилиндра длиной / и радиусом
г .
—
площадь
поверхности цилиндра длиной / и радиусом
г .
Необходимым
условием стационарности процесса
является независимость потока теплоты
от радиуса цилиндра, т. е. q=const.
Учитывая это, разделим переменные и
проинтегрируем уравнение (1). Получим:
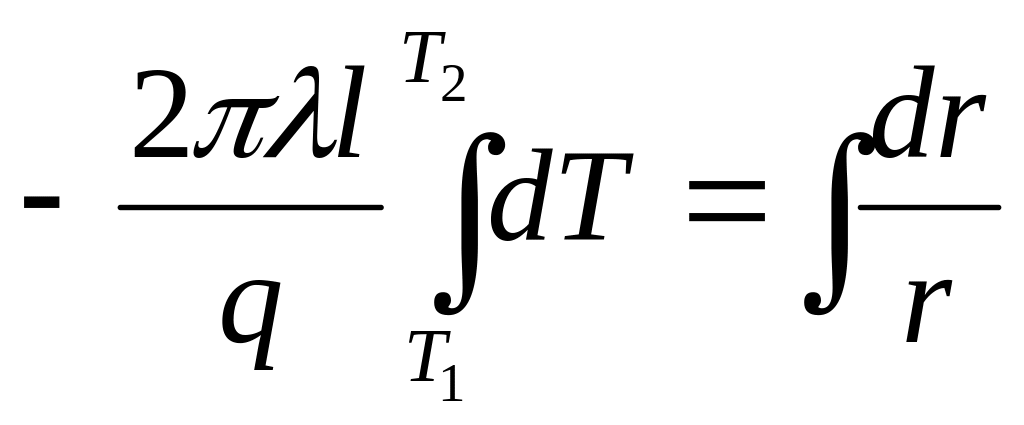 .
.
откуда
![]() .
.
