
- •Решебник
- •Ростов-на-Дону
- •Кандидат физико-математических наук
- •Внутреннее строение вещества
- •Введение в теорию идеального газа
- •Основы термодинамики
- •Статистические закономерности в термодинамике
- •Реальные газы
- •Явления переноса
- •Развернутое изложение методов решения физических задач по молекулярной физике
- •Внутреннее строение вещества
- •Классификация кристаллов
- •Физические типы кристаллических решеток
- •Введение в теорию идеального газа
- •Статистические закономерности
- •Решение.
- •Поток теплоты на единицу длины цилиндров
- •Основы термодинамики
- •Поток тепла, проходящий через него, в силу закона Фурье равен
- •Реальные газы
Введение в теорию идеального газа
Какую максимальную концентрацию молекул углекислого газа, газокинетический диаметр которых равен d=3,2• 10-10 м, можно образовать в сферическом сосуде диаметра D=1 м, чтобы средний свободный пробег превосходил величину диаметра? Решение.
Из основной формулы имеем п0 <
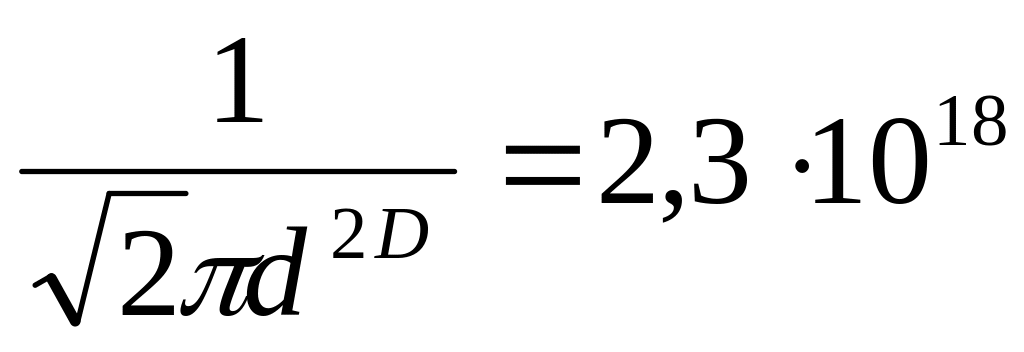 м-3.
м-3.
2.2. Сколько молекул кислорода находится в объеме 1 л при температуре
0° С и давлении 133,3 Па?
Решение.
При решении используется основная формула кинетической теории р = п0кТ, (1)
где п0 — число молекул в единице объема.
Поскольку
1
м3=103
л,
то искомое число молекул N
связано
с п0
соотношением
![]() = п0.
= п0.
Следовательно, из (1) следует, что
N
=
![]() ~
3,5-1019,
~
3,5-1019,
где величины р, к, Т необходимо выразить в системе СИ.
2.3. Каково давление в смеси газов емкостью 2 л, если в ней находится 1015 молекул кислорода и 10-7 г азота, а температура смеси 50° С?
Решение.
По закону Дальтона
р = [п0(О.2)+п0(N2)]кТ, (1)
причем n0(02) = 1015-0,5-103 = 0,5-1018 м-3, а
п0(N2)
= 0,5-103
(![]() )N0~
1,1
• 10-2
м3,
)N0~
1,1
• 10-2
м3,
где учтено, что число Авогадро N0 = 6-1023.
Отсюда следует, что
Р = (n0 (Оа) + n0 (N2)) kT = 0,72 • 102 Па.
2.4. Давление газа равно 104 Па, а средняя квадратичная скорость равна 500 м/с. Найти плотность этого газа.
Решение.
Основное
уравнение кинетической теории может
быть представлено следующим образом:
р
=n0кТ=
—
![]() .
.
Следовательно,
![]() =
Зр/<V2>
=0,12 кг/м3.
=
Зр/<V2>
=0,12 кг/м3.
2.5. Чему равна энергия вращательного движения двухатомного газа, находящегося под давлением р=105 Па в сосуде объемом 1 л? Считать, что вращательные степени свободы полностью возбуждены.
Решение.
Из основного кинетического уравнения для плотности кинетической энергии Е молекул имеем
![]()
Эта плотность энергии получается за счет трех поступательных степеней свободы каждой из молекул. Вращательных степеней свободы две. Следовательно, плотность вращательной энергии равна
Евр = 2Е/3 = р.
Отсюда энергия вращательного движения в одном литре
Евр
=![]() =10 Дж.
=10 Дж.
2.6. На упругой нити с модулем кручения D=10-15 Н-м подвешено зеркальце. Вследствие беспорядочных ударов молекул оно совершает колебания. Определить средний квадрат амплитуды этих колебаний. Температура воздуха 20° С.
Решение.
Уравнение
движения нити есть
![]()
где / — момент инерции зеркальца относительно оси кручения.
Отсюда следует закон сохранения энергии
1/2![]() + 1/2
D
+ 1/2
D
![]() 2
= сопst.
2
= сопst.
Следовательно, имеем
![]() .
.
где использована теорема о равнораспределении энергии по степеням свободы.
Следовательно,
![]() .
.
Статистические закономерности
2.7. Выразить поток молекул N, падающих стенку сосуда, через плотность молекул п0 и среднюю скорость <V>. Функцию распределения
f(V) по скорости считать изотропной.
Решение.
Условие нормировки функции распределения имеет вид:
![]()
где
![]() — элемент телесного угла.
— элемент телесного угла.
По определению средней скорости имеем
<V>=![]()
C другой стороны, отсчитывая углы 0 от нормали стенке, получаем
![]()
2.8. Определить отношение числа частиц N1энергия которых меньше, чем Е1 к числу частиц N2, энергия которых больше этой величины.
Решение.
Используем
распределение Максвелла, которое с
учетом того, что
![]() может быть записано в виде
может быть записано в виде
dN=
А
ехр
(— Е/кТ)
![]() dE,
dE,
А — нормировочная постоянная.
Отсюда
получаем:
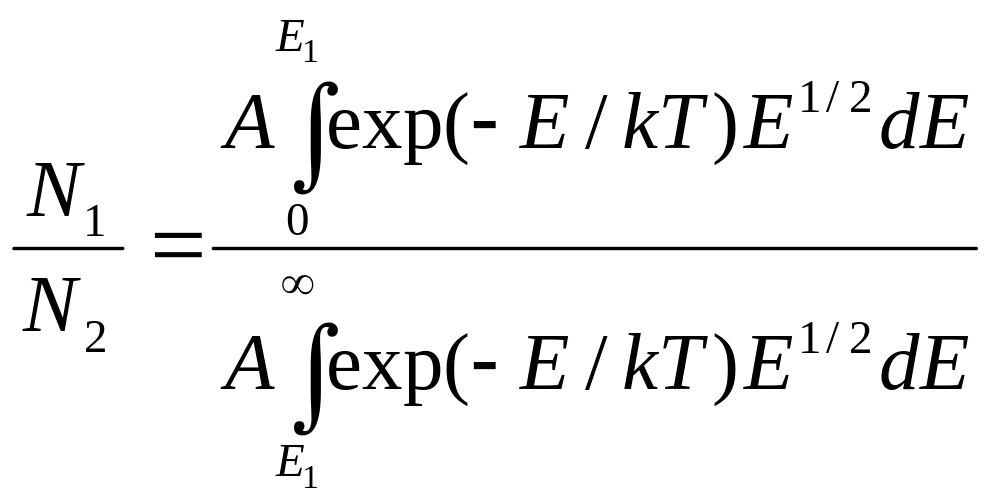
Эти интегралы подстановкой у = t2 и интегрированием по частям легко сводятся к табулированным интегралам ошибок.
2.9.
Идеальный газ, имеющий температуру Т,
вращается
вместе с цилиндром высоты l
и радиуса R
вокруг
своей оси с угловой скоростью
![]() .
Найти давление газа на боковую стенку
цилиндра, если общее число молекул
в цилиндре N0.
.
Найти давление газа на боковую стенку
цилиндра, если общее число молекул
в цилиндре N0.
Решение.
В
системе координат, связанной с вращающимся
цилиндром, на молекулы идеального
газа действуют силы инерции т
2г,
направленные
от
оси вращения. Следовательно, можно
считать, что газ находится в эффективном
потенциальном поле (—]/2![]() 2г2)
и
поэтому распределение Больцмана имеет
вид
2г2)
и
поэтому распределение Больцмана имеет
вид
dN
= А ехр
(
2
г2/2кТ)
2![]() dгdz, (1)
dгdz, (1)
где А есть нормировочная постоянная, которая находится из условия
![]()
где N0 — общее число частиц в цилиндре, V— объем цилиндра.
Имеем:
![]()
Отсюда
для плотности распределения частиц по
радиусу цилиндра получаем
формулу
![]()
где
учтено, что объем цилиндра
![]() .
Давление на боковую стенку:
.
Давление на боковую стенку:
P(R) =n0(R)kT.
2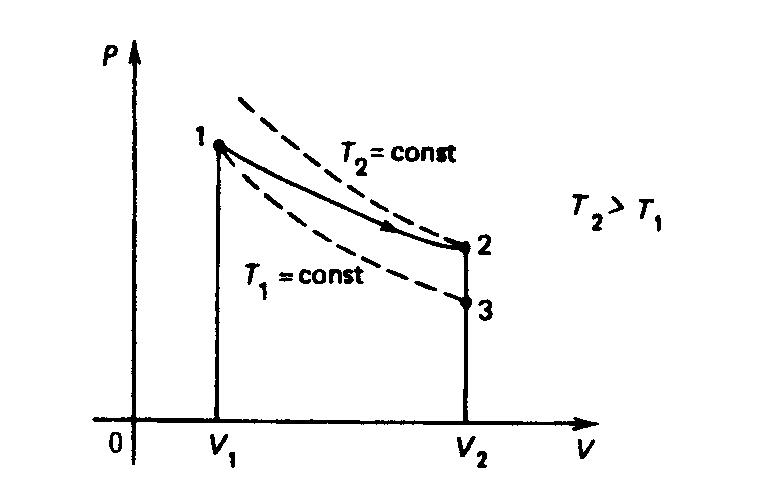 .10.
Нагревается или охлаждается газ при
переходе из состояния 1 в состояние 2?
m=const.
.10.
Нагревается или охлаждается газ при
переходе из состояния 1 в состояние 2?
m=const.
Решение.
Изобразим на диаграмме P – V графики зависимости P(V) при изотермическом расширении газа. Изотерма, проходящая через точку 2, определяющую состояние 2, выше изотермы, проходящей через точку 1, определяющую состояние 1, следовательно, Т2 > Т1. Газ нагревается.
2.11. Нагревается или охлаждается газ, если процесс его расширения происходит по закону PVn=const? Масса газа постоянна. Рассмотреть два случая: 1) n<1, 2) n>1.
