
- •Пакет комплексних контрольних робіт
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •1 Електрична потужність , яку генерує хімічне джерело струму
- •2 Гальвані-потенціал електрода «х» – це
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •1 Який параметр можна підрахувати за наведеною формулою
- •2 Рівноважний потенціал електрода – це
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •1 Електрична потужність , яку споживає електролізер
- •2 Потенціал електрода «х» – це
- •3 Який фізичний зміст має цей параметр:
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •1 Вказати правильний запис закона Фарадея
- •2 Стаціонарний потенціал електрода «х» – це
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Критерії оцінки
- •Рецензія
Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
Напрям підготовки – 6.051301 «Хімічна технологія» за професійним спрямуванням на спеціальність "Технічна електрохімія"
Кафедра технічної електрохімії
Білет № 17
________________________________________________________________________________
1 Вимоги до електродних матеріалів
А) йонна провідність
Б) електронна провідність
В) ізоляційні властивості
_____________________ ______________________________________________________________
2 Вільна енергія G електрохімічної реакції – це
А) запас хімічної енергії, яку має система хімічних речовин (реагентів самовільної реакції)
Б) частина хімічної енергії системи речовин, яка здатна в самовільній електрохімічній реакції перетворитись у тепло
В) частина хімічної енергії системи речовин, яка здатна в самовільній електрохімічній реакції перетворитись у електричну роботу
_________________________ __________________________________________________
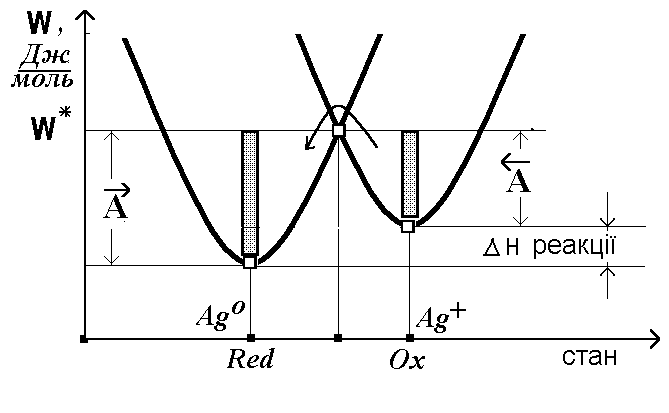 3
Вказати значення енергії активації
реакції окиснення срібла Ag
Ag+
+ e–
3
Вказати значення енергії активації
реакції окиснення срібла Ag
Ag+
+ e–
А) (А )
Б) (А )
В) [(А )+(А )]/2
_ _______________________________________________
4. Підрахувати іонну силу водного розчину, що містить 0.01 моль/л КОН і 0.5 моль/л Na2SO4.
Затверджено на засіданні кафедри ТЕ.
Протокол № 8 від “08” лютого 2012 р.
Завідувач кафедри ТЕ, професор В.Г. Нефедов
Викладач, професор М.Д.Кошель
МІНІСТЕРСТВО ОСВІТИ І НАУКИ, МОЛОДІ ТА СПОРТУ УКРАЇНИ
ДЕРЖАВНИЙ ВИЩИЙ НАВЧАЛЬНИЙ ЗАКЛАД
«УКРАЇНСЬКИЙ ДЕРЖАВНИЙ ХІМІКО-ТЕХНОЛОГІЧНИЙ
УНІВЕРСИТЕТ»
Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
Напрям підготовки – 6.051301 «Хімічна технологія» за професійним спрямуванням на спеціальність "Технічна електрохімія"
Кафедра технічної електрохімії
Білет № 18
____________________________________________________________________________
1 Питома електропровідність електролітів
А) зростає з підвищенням температури
Б) зменшується з підвищенням температури
В) не залежить від температури
_________________________ __________________________________________________
2 Вимоги до електроліту
А) великий питомий опір
Б) малий питомий опір
В) електронна провідність
_________________________ __________________________________________________
3 Термодинамічний потенціал електрода «х» – це
А) е.р.с., виміряна в парі (електрод «х»–електрод порівняння)
Б) невимірний стрибок потенціалу між електродом «х» і електролітом
В) потенціал, підрахований за термодинамічними даними (рівняння Нернста, G)
4. Іонний добуток води дорівнює 1∙10-14. Підрахувати ступінь дисоціації води.
_________________________ __________________________________________________
Затверджено на засіданні кафедри ТЕ.
Протокол № 8 від “08” лютого 2012 р.
Завідувач кафедри ТЕ, професор В.Г. Нефедов
Викладач, професор М.Д.Кошель
МІНІСТЕРСТВО ОСВІТИ І НАУКИ, МОЛОДІ ТА СПОРТУ УКРАЇНИ
ДЕРЖАВНИЙ ВИЩИЙ НАВЧАЛЬНИЙ ЗАКЛАД
«УКРАЇНСЬКИЙ ДЕРЖАВНИЙ ХІМІКО-ТЕХНОЛОГІЧНИЙ
УНІВЕРСИТЕТ»
