
- •Пакет комплексних контрольних робіт
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •1 Електрична потужність , яку генерує хімічне джерело струму
- •2 Гальвані-потенціал електрода «х» – це
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •1 Який параметр можна підрахувати за наведеною формулою
- •2 Рівноважний потенціал електрода – це
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •1 Електрична потужність , яку споживає електролізер
- •2 Потенціал електрода «х» – це
- •3 Який фізичний зміст має цей параметр:
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •1 Вказати правильний запис закона Фарадея
- •2 Стаціонарний потенціал електрода «х» – це
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
- •Критерії оцінки
- •Рецензія
Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
Напрям підготовки – 6.051301 «Хімічна технологія» за професійним спрямуванням на спеціальність "Технічна електрохімія"
Кафедра технічної електрохімії
Білет № 25
_______________________________________________________________________
1 Електрохімічний еквівлент речовини в реакції це
А) маса одного грам-еквівалента речовини
Б) кількість речовини, яка витрачена або утворена в електрохімічної реакції при проходженні одиниці кількості електрики (Г/Агод, г/Кл)
В) кількість електрики, яка витрачена на утворення одиниці маси речовини в реакції (Агод/г, Кл/г)
_________________________ __________________________________________________
2 Вказати правильний запис рівняння Нернста для іонно-металевого електрода
Ag+|Ag0 (E0 = +0.81 B); Ag++e– Ag0;
А)
![]() Б)
Б)![]()
В)
![]()
_________________________ __________________________________________________
3 Вказати вираз для визначення стандартної густини струму обміну електрохімічної реакції
А)
![]() Б)
Б)
![]()
_________________________ __________________________________________________
4. Розрахувати теоретичну питому енергію Дж/кг реакції в свинцево-кислотному акумуляторі
Pb+PbO2 + 2H 2SO4 2e 2PbSO4 + 2 H2O.
Затверджено на засіданні кафедри ТЕ.
Протокол № 8 від “08” лютого 2012 р.
Завідувач кафедри ТЕ, професор В.Г. Нефедов
Викладач, професор М.Д.Кошель
МІНІСТЕРСТВО ОСВІТИ І НАУКИ, МОЛОДІ ТА СПОРТУ УКРАЇНИ
ДЕРЖАВНИЙ ВИЩИЙ НАВЧАЛЬНИЙ ЗАКЛАД
«УКРАЇНСЬКИЙ ДЕРЖАВНИЙ ХІМІКО-ТЕХНОЛОГІЧНИЙ
УНІВЕРСИТЕТ»
Комплексна контрольна робота з дисципліни “ теоретична електрохімія ”
Напрям підготовки – 6.051301 «Хімічна технологія» за професійним спрямуванням на спеціальність "Технічна електрохімія"
Кафедра технічної електрохімії
Б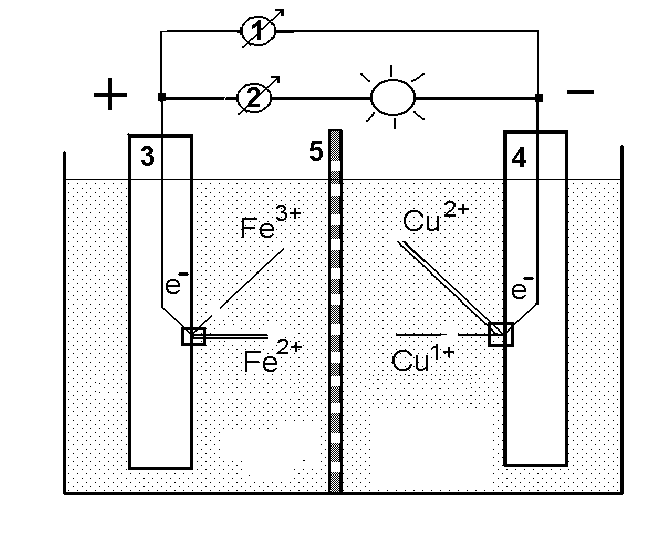 ілет
№ 26
ілет
№ 26
___________________________________________________
1 Розгляньте схему хімічного джерела струму із мідним та залізним електродом і вкажіть
Який процес відбувається на лівому електроді ХДС (рис)
А) окислення Fe3+ Fe2+ Б) відновлення Fe3+ Fe2+
В) окислення Fe2+Fe3+ Г) відновлення Fe2+Fe3+
_________________________________________
2 Підрахувати рівноважний потенціал мідного електрода в розчині CuSO4 , з активністю електроліту а= 0.5 М (стандартний потенціал Е0=-+ 0.34 В) за рівнянням Нернста
А) Еcu2+/Cu0 = +0.34 + 0.059Log(1) = +0.34 В
Б) Еcu2+/Cu0 = +0.34 + 0.059Log(0.5) = ….. В
В) Еcu2+/Cu0 = +0.34 + ((0.059)/2)Log(0.5) = ….. В
_________________________ __________________________________________________
3 Вказати вираз для визначення константи швидкості електрохімічної реакції
А) Б)
_________________________ __________________________________________________
4. Розрахувати електрохімічний еквівалент H 2SO4 в реакції
PbO2 + H 2SO4 + 2e PbSO4 + 2 H2O.
Затверджено на засіданні кафедри ТЕ.
Протокол № 8 від “08” лютого 2012 р.
Завідувач кафедри ТЕ, професор В.Г. Нефедов
Викладач, професор М.Д.Кошель
МІНІСТЕРСТВО ОСВІТИ І НАУКИ, МОЛОДІ ТА СПОРТУ УКРАЇНИ
ДЕРЖАВНИЙ ВИЩИЙ НАВЧАЛЬНИЙ ЗАКЛАД
«УКРАЇНСЬКИЙ ДЕРЖАВНИЙ ХІМІКО-ТЕХНОЛОГІЧНИЙ
УНІВЕРСИТЕТ»
