
- •1. Качественные особенности живой материи. Уровни организации живого
- •2. Клеточная мембрана. Поверхностный аппарат клетки, её основные части, их назначение
- •3. Химический состав клетки (белки, их структура и функции)
- •5. Мейоз
- •6. Формы биологических связей в природе. Симбиоз, его виды. Паразитизм как биологический феномен. Примеры
- •7. Плоские черви. Морфология, систематика, основные представители. Циклы развития. Пути заражения. Профилактика
- •8. Генотип. Геном. Фенотип. Факторы, определяющие развитие фенотипа. Доминантность и рецессивность. Взаимодействие генов в детерминации признаков: доминирование, промежуточное проявление
- •9. Экологические факторы, их взаимодействие
3. Химический состав клетки (белки, их структура и функции)
Все клетки животных и растительных организмов, а также микроорганизмов сходны по химическому составу. В клетке содержится несколько тысяч веществ, которые участвуют в разнообразных химических реакциях. Сходство в строении и химическом составе разных клеток свидетельствует о единстве их происхождения.
Одни элементы содержатся в клетках в относительно большом количестве, другие - в малом. Особенно велико содержание в клетке четырех элементов - кислорода, углерода, азота и водорода (до 98%). Сера, фосфор, хлор, калий, магний, натрий, кальций, железо составляют вместе 1,9%. Все остальные элементы содержатся в клетке в исключительно малых количествах (таблица 2). В живых телах наряду с веществами, распространенными в неживой природе, содержится много веществ, характерных только для живых организмов.
Таблица 2. Содержание химических элементов в клетке
-
Элементы
Количество (в%)
Элементы
Количество (в%)
Кислород
Углерод
Водород
Азот
Фосфор
Калий
Сера
Хлор
65 - 70
15 - 18
8 - 10
1,5 - 3,0
0,20 - 1,00
0,15 - 0,4
0,15 - 0,2
0,05 - 0,10
Кальций
Магний
Натрий
Железо
Цинк
Медь
Йод
Фтор
0,04 - 2,00
0,02 - 0,03
0,02 - 0,03
0,01 - 0,015
0,0003
0,0002
0,0001
0,0001
Вода составляет почти 80% массы клетки. Она определяет физические свойства клетки - ее объем, форму, упругость. Вода участвует в образовании структурных молекул органических веществ, в частности структуры белков. Большинство реакций, протекающих в клетке, могут идти только в водном растворе; многие вещества поступают в клетку из внешней среды в водном растворе и в водном же растворе отработанные продукты выводятся из клетки. Вода является непосредственным участником многих химических реакций (расщепление белков, углеводов, жиров и др.).
Биологическая роль воды определяется особенностью ее молекулярной структуры, полярностью молекул воды. Частица воды - диполь: в области атомов водорода (протона) преобладает положительный заряд, а в области атомов кислорода - отрицательный. Этим объясняется способность воды к ориентированию в электрическом поле и присоединению к различным молекулам и участкам молекул, несущим заряд, с образованием гидратов. Много веществ способно растворяться в воде: соли, кислоты, щелочи, а из органических веществ - многие спирты, амины, углеводы, белки и др. Вещества, хорошо растворимые в воде, называются гидрофильными веществами. Жиры, клетчатка и другие вещества плохо или вовсе не растворяются в воде, их называют гидрофобными. Гидрофильные вещества - это соли, углеводы, белки, низкомолекулярные органические соединения. Гидрофобные вещества входят в состав клеточных мембран, обусловливая их полупроницаемость.
Для процессов жизнедеятельности клетки наиболее важны такие катионы, как K+, Na+, Ca2+, Mg2+, из анионов - HPO42-, Cl-, HCO3-. Концентрация анионов и катионов в клетке и среде ее обитания, как правило, резко различна. К примеру, внутри клетки всегда довольно высокая концентрация ионов калия и очень малая - ионов натрия, а в окружающей среде (плазме крови, морской воде) мало ионов калия и много ионов натрия. Пока клетка жива, это соотношение ионов строго поддерживается, а после смерти клетки содержание ионов в среде и клетке выравнивается. Ионы клетки способствуют поддержанию постоянного осмотического давления внутри клетки и рН. В норме реакция клеток слабощелочная, обеспечиваемая содержащимися в клетке анионами слабых кислот (НСО3-, НРО4-) и слабыми кислотами (Н2СО3), которые связывают и отдают ионы водорода, в результате чего реакция внутренней среды клетки практически не изменяется. Некоторые неорганические вещества содержатся в клетке не только в растворенном, но и в твердом состоянии. Так, прочность и твердость костной ткани обеспечивается фосфатом кальция, а раковин моллюсков - карбонатом кальция. Не все вещества, содержащиеся в клетке, специфичны для живой природы. Вода и соли распространены и вне живого. Но в организмах и продуктах их жизнедеятельности обнаружено большое количество углеродсодержащих соединений, характерных только для живых клеток и организмов, получивших название органических веществ.
Из органических веществ клетки на первом месте по количеству и значению стоят белки, состоящие из крупных молекул (макромолекул). В состав всех белков входят атомы водорода, кислорода, азота; во многие белки входят еще атомы серы, а в некоторые - атомы металлов железа, цинка, меди. Белки составляют 10-20% от сырой массы и 50-80% от сухой массы клетки. Белки обладают большой молекулярной массой: молекулярная масса альбумина - одного из белков яйца - 36 000, гемоглобина - 152 000, миозина (одного из белков мышц) - 500 000. Тогда как молекулярная масса спирта - 46, уксусной кислоты - 60, бензола - 78. Среди органических веществ белки самые сложные, они составлены из повторяющихся сходных по структуре низкомолекулярных соединений, ковалентно связанных между собой, которые называются мономерами. Поэтому белки (как углеводы и жиры) являются полимерами. Если обозначить мономер буквой А, то структуру полимера можно изобразить так: А-А-А-А-А. Большинство природных и искусственных (полиэтилен, лавсан, капрон и др.) полимеров построены из одинаковых мономеров. Белки же состоят из сходных, но не вполне одинаковых мономеров. Мономерами белков являются аминокислоты. Аминокислота имеет следующую формулу:
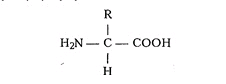
В состав аминокислот входят: NH2 – аминокислотная группа, сдающая основными свойствами; СООН – карбоксильная группа, имеет кислотные свойства.
Имеется много разных аминокислот, но мономерами любых природных белков - животных, растительных, микробных, вирусных - являются только 20 аминокислот (таблица 3). Соединение аминокислот происходит через общие для них группировки: аминогруппа одной аминокислоты соединяется с карбоксильной группой другой с отщеплением молекулы воды. Между аминокислотами образуется прочная ковалентная связь -NH-CO2-, которая называется пептидной связью. Образовавшееся соединение аминокислот называется пептидом. Пептид из двух аминокислот называется дипептидом, из трех - трипептидом, из многих аминокислот - полипептидом. Все белки представляют собой полипептиды, т.е. цепи из многих десятков и даже сотен аминокислотных звеньев.
Структура белков:
1. Каждый живой организм содержит большое число разнообразных белков, причем каждому виду присущи свойственные только ему белки. Белки различаются по составу аминокислот, числу аминокислотных звеньев, порядку следования в цепи. Поэтому число структурных вариантов достигает астрономических цифр. Последовательность аминокислотных остатков в молекуле белка определяет его первичную структуру, прочность которой определяется ковалентными связями. Схема конденсации аминокислот (образование первичной структуры белка):
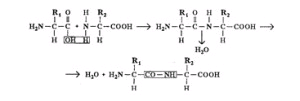
2. Следующий уровень структуры белка определяется степенью закручивания белковой нити в спираль. Между группами -СООН, находящимися на одном витке спирали, и группами -NH2 - на другом витке образуются водородные связи, которые слабее ковалентных, но их большое число обеспечивает образование достаточно прочной структуры.
3. Дальнейшая укладка полипептидной спирали заключается в свертывании полипептидной нити в клубок. Образуется третичная структура белка, специфичная для каждого белка. Третичную структуру поддерживают гидрофобные связи, возникающие между радикалами гидрофобных аминокислот. Эти связи слабее водородных: в водной среде клетки гидрофобные радикалы отталкиваются от воды и слипаются друг с другом. Кроме гидрофобных сил, в третичной структуре существенную роль играют электростатические связи между электроотрицательными и электроположительными радикалами аминокислотных остатков. Третичная структура поддерживается также небольшим числом ковалентных дисульфидных -S-S- связей, возникающих между атомами серы серосодержащих аминокислот. В живой клетке образуются и другие, более сложные формы структуры белка, например, четвертичные, которые обеспечивают полноценную работу белков.
4. Четвертичная структура формируется при соединении нескольких молекул белков. Пептидные цепи, уложенные в виде клубка, называются глобулярными, а в виде нитей - фибриллярными белками (рисунок 3).
Под влиянием внешних факторов (изменение температуры, солевого состава среды, рН, радиация и иные факторы) слабые связи рвутся и структура белка, а следовательно, и его свойства изменяются. Этот процесс называется денатурацией. Такие изменения структуры белка обычно легко обратимы. Разрыв большого числа слабых связей ведет к необратимой денатурации белка: например, свертывание яичного белка при кипячении. При обратимой денатурации нарушаются слабые связи, которые не затрагивают первичную структуру белка. При денатурации изменяются и свойства белка: он утрачивает растворимость, становится доступным действию ферментов, теряет присущие ему функции. Гормоны также могут оказывать денатурирующее действие. Все особенности белка определяются его первичной структурой, т.е. порядком чередования аминокислот в полипептидной цепи. Способность белков к обратимому изменению структуры в ответ на действие физических и химических факторов лежит в основе важнейшего свойства всех живых систем - раздражимости.
Функции белков:
1. Прежде всего, они выполняют строительную функцию, участвуя в образовании всех клеточных мембран и органоидов клетки, а также внеклеточных структур.
2. Большое значение имеет каталитическая функция белков. Быстрое расщепление и синтез органических веществ в клетке обеспечивают катализаторы (ускоритель реакции) - ферменты, по химической структуре являющиеся белками. Каталитическая активность ферментов исключительно велика: они ускоряют протекание реакций в десятки, сотни миллионов раз. В большинстве случаев ферменты катализируют превращение веществ, размеры молекул которых по сравнению с размерами макромолекулы фермента очень малы. Например, фермент каталаза имеет молекулярную массу 250 000, а пероксида водорода (Н2О2), распад которого катализирует каталаза, всего 34. Это указывает на то, что каталитическая активность фермента определяется не всей молекулой, а только небольшим ее участком - активным центром фермента. Возможность сближения фермента и вещества происходит благодаря геометрическому соответствию структур активного центра фермента и молекулы вещества (они подходят друг к другу, как “ключ к замку”). При денатурации фермента его каталитическая активность исчезает, так как нарушается структура активного центра. Почти каждая химическая реакция катализируется особым ферментом. Число различных реакций в клетке достигает нескольких тысяч, соответственно в клетке обнаружено к настоящему времени более 2 тыс. ферментов. Каждый фермент обеспечивает одну или несколько реакций, которые они катализируют (трансферазы, оксиредуктазы и др.). Многие гормоны являются белками (например, гормон роста, производимый клетками гипофиза - АКТГ и др., инсулин, глюкагон и т.п.). Белковые и небелковые гормоны способны изменять активность многих ферментов, усиливая или подавляя действие ферментов и тем самым регулируя протекание физиологических процессов в организме.
3. Весьма важна для жизни клетки сигнальная функция белков. В поверхностную мембрану клетки встроены молекулы белков, способных изменять свою третичную структуру в ответ на действие факторов внешней среды. Так происходит прием сигналов из внешней среды и передача команд в клетку.
4. Двигательная функция белков проявляется в осуществлении различных видов движений (мерцание ресничек простейших, движение жгутиков, сокращение мышц). Движения обусловлены наличием особых сократительных белков. В крови, наружных клеточных мембранах, в цитоплазме и ядрах клеток есть различные транспортные белки, способные присоединять различные вещества и переносить их из одного места клетки в другое. Белок крови гемоглобин присоединяет кислород и транспортирует его ко всем тканям и органам тела. Белки-транспортеры клеточных мембран обеспечивают активный и строго избирательный транспорт внутрь и наружу клетки сахаров, различных веществ и ионов.
5. Большое значение имеет защитная функция белков. При введении чужеродных белков или клеток в организм в нем происходит выработка особых белков, которые связывают и обезвреживают чужеродные клетки и вещества. В лимфоидных тканях организма человека (вилочковая железа, лимфатические железы, селезенка) производятся лимфоциты - клетки, способные синтезировать огромное разнообразие защитных белков - антител, носящих название иммуноглобулинов. Антигены, попадающие в организм, вызывают в лимфоцитах синтез антител определенного типа. Практически лимфоциты способны синтезировать антитела на любой антиген, с которым клетка и организм никогда не встречались. Такая защита обеспечивается генами клетки, ответственными за синтез иммуноглобулинов. Защитные белки синтезируются и растениями (флавоноиды, терпены, алкалоиды).
6. Белки служат одним из источников энергии в клетке (энергетическая функция). При распаде 1 г белка до конечных продуктов выделяется 17,6 кДж (или 4,2 ккал). Белки в клетке распадаются сначала до аминокислот, а затем до конечных продуктов - образуется вода, СО2 и азотистые продукты (аммиак, мочевина и др.) с выделением энергии, используемой клеткой для синтеза новых веществ или на другие нужды. Однако белки используются в качестве источника энергии тогда, когда истощаются другие ее источники (как углеводы и жиры). Часть аминокислот не расщепляется до конечных продуктов, а используется для синтеза новых белков.
К биополимерам, помимо белков, относятся углеводы. В состав углеводов входят атомы углерода, кислорода, водорода. Различают простые и сложные углеводы. Простые - моносахариды. Сложные - полимеры, мономерами которых являются моносахариды (олигосахариды и полисахариды). С увеличением числа мономерных звеньев растворимость полисахаридов уменьшается, сладкий вкус исчезает.
Моносахариды - это твердые бесцветные кристаллические вещества, которые хорошо растворяются в воде и очень плохо (или совсем не) растворяются в органических растворителях. Среди моносахаридов различают триозы, тетрозы, пентозы и гексозы. Среди олигосахаридов наиболее распространенными являются дисахариды (мальтоза, лактоза, сахароза). Полисахариды наиболее часто встречаются в природе (целлюлоза, крахмал, хитин, гликоген). Их мономерами являются молекулы глюкозы. В воде растворяются частично, набухая образуют коллоидные растворы.
Липиды - нерастворимые в воде жиры и жироподобные вещества, состоящие из глицерина и высокомолекулярных жирных кислот. Жиры - сложные эфиры трехатомного спирта глицерина и высших жирных кислот. Животные жиры содержатся в молоке, мясе, подкожной клетчатке. У растений - в семенах, плодах. Кроме жиров в клетках присутствуют и их производные - стероиды (холестерин, гормоны и жирорастворимые витамины А, D, К, Е, F).
Липиды являются:
-структурными элементами мембран клеток и клеточных органелл;
-энергетическим материалом (1г жира, окисляясь, выделяет 39 кДж энергии);
-запасными веществами;
-выполняют защитную функцию (у морских и полярных животных);
-влияют на функционирование нервной системы;
-источник воды для организма (1кг, окисляясь, дает 1,1кг воды).
Нуклеиновые кислоты. Название "нуклеиновые кислоты" происходит от латинского слова "нуклеус", т.е. ядро: они впервые были обнаружены в клеточных ядрах. Биологическое значение нуклеиновых кислот очень велико. Они играют центральную роль в хранении и передаче наследственных свойств клетки, поэтому их часто называют веществами наследственности. Нуклеиновые кислоты обеспечивают в клетке синтез белков, точно таких же, как в материнской клетке и передачу наследственной информации. Существует два вида нуклеиновых кислот - дезоксирибонуклеиновая кислота (ДНК) и рибонуклеиновая кислота (РНК).
Молекула ДНК состоит из двух спирально закрученных цепей. ДНК - полимер, мономерами которого являются нуклеотиды. Нуклеотиды - соединения, состоящие из молекулы фосфорной кислоты, углевода дезоксирибозы и азотистого основания. У ДНК четыре типа азотистых оснований: аденин (А), гуанин (Г), цитозин (Ц), тимин (Т). Каждая цепь ДНК - полинуклеотид, состоящий из нескольких десятков тысяч нуклеотидов. Удвоение ДНК - редупликация - обеспечивает передачу наследственной информации от материнской клетки к дочерним.
РНК - полимер, по структуре сходный с одной цепочкой ДНК, но меньших размеров. Мономеры РНК - нуклеотиды, состоящие из фосфорной кислоты, углевода рибозы и азотистого основания. Вместо тимина в РНК присутствует урацил. Известны три вида РНК: информационная (и-РНК) - передает информацию о структуре белка с молекулы ДНК; транспортная (т-РНК) - транспортирует аминокислоты к месту синтеза белка; рибосомная (р-РНК) - содержится в рибосомах, участвует в поддержании структуры рибосомы.
Очень важную роль в биоэнергетике клетки играет адениловый нуклеотид, к которому присоединены два остатка фосфорной кислоты. Такое вещество называют аденозинтрифосфорной кислотой (АТФ). АТФ - универсальный биологический аккумулятор энергии: световая энергия солнца и энергия, заключенная в потребляемой пище, запасается в молекулах АТФ. АТФ - неустойчивая структура, при переходе АТФ в АДФ (аденозиндифосфат) выделяется 40 кДж энергии. АТФ образуется в митохондриях клеток животных и при фотосинтезе в хлоропластах растений. Энергия АТФ используется для совершения химической (синтез белков, жиров, углеводов, нуклеиновых кислот), механической (движение, работа мышц) работ, трансформации в электрическую или световую (разряды электрических скатов, угрей, свечение насекомых) энергии
4. ОБМЕН ВЕЩЕСТВ И ПРЕВРАЩЕНИЕ ЭНЕРГИИ В КЛЕТКЕ. ФОТОСИНТЕЗ. ХЕМОСИНТЕЗ
Все живые организмы, существующие на Земле, представляют собой открытые системы, характеризующиеся способностью активно обмениваться
с окружающей средой веществами и энергией. Живые существа могут использовать два вида энергии - световую (энергию солнечного излучения), такие организмы называются фототрофами, и химическую (энергию связей химических соединений) - это хемотрофы. Для синтеза компонентов организма необходимо потребление химических элементов извне. Главным структурным элементом органических молекул является углерод. В зависимости от источников углерода живые организмы делят на автотрофы, использующие неорганический источник углерода, и гетеротрофы, использующие органические источники углерода. Большинство организмов относится к фотоавто- трофам или хемогетеротрофам.
Процесс потребления энергии и веществ называется питанием. Пищевые вещества, попавшие в клетку или многоклеточный организм, вовлекаются в процессы метаболизма. Метаболизм представляет собой совокупность взаимосвязанных, сбалансированных и координированных в пространстве и времени процессов, включающих разнообразные химические превращения веществ в организме. Метаболизм состоит из анаболизма – реакций синтеза веществ с потреблением энергии (пластический обмен или ассимиляция) и катаболизма, представленного реакциями расщепления веществ с высвобождением энергии, которая может запасаться в виде АТФ и/или рассеиваться в виде тепла (энергетический обмен или диссимиляция). Процессы энергетического и пластического обменов неразрывно связаны между собой.
Энергетический обмен в клетке. Синтез АТФ
АТФ – аденозинтрифосфорная кислота, является универсальным источником энергии у всех живых организмов. По своей химической природе
АТФ является мононуклеотидом и состоит из азотистого основания аденина,
углевода рибозы и трех остатков фосфорной кислоты, соединенных между собой макроэргическими связями (рисунок 4).
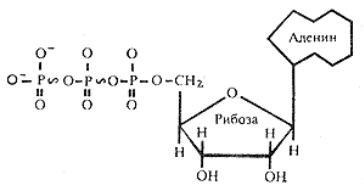
Рисунок 4 - Строение молекулы АТФ
Молекула АТФ в клетке может гидролизоваться до АДФ (аденозиндифосфата) и АМФ (аденозинмонофосфата), при этом при распаде АТФ до АДФ и АМФ высвобождается порядка 30,6 кДж энергии. Энергия, высвобождаемая при гидролизе АТФ, используется клеткой на все виды деятельности, и большая часть энергии тратится на синтетические процессы.
Запас энергии в клетке ограничен и пополняется благодаря процессу фосфорилирования (присоединения неорганического фосфата к АДФ). Энергия для синтеза АДФ образуется в ходе энергетического обмена. Энергетический обмен состоит из трех этапов:
1-й этап – подготовительный (мобилизация субстратов) – заключается в ферментативном расщеплении высокомолекулярных органических веществ до низкомолекулярных, простых. Он протекает в пищеварительном тракте, а на уровне клетки – в лизосомах. Вся энергия подготовительного этапа рассеивается в виде тепла. Реакции подготовительного этапа:
белки + вод ⟶ аминокислоты,
углеводы + вода ⟶ глюкоза,
жиры + вода ⟶ глицерин + высшие жирные кислоты.
2-й этап - неполное окисление (бескислородный) — протекает непосредственно в цитоплазме, где находятся ферменты для дальнейшего расщепления органических молекул. Главным источником энергии в клетке является глюкоза. Бескислородное, неполное расщепление глюкозы называется гликолизом. Процесс гликолиза протекает в цитоплазме, где располагаются ферменты превращения шестиуглеродной глюкозы до двух трехуглеродных молекул пировиноградной кислоты (пирувата, ПВК). В ходе гликолиза образуется по две молекулы ПВК, АТФ и воды, а также атомы водорода, которые запасаются в окисленной форме НАД+ (никотинамидадениндинуклеотид) с образованием НАДН + Н+. В ходе гликолиза выделяется 200 кДж/моль энергии. Часть этой энергии (60%) рассеивается в виде тепла, остальная (40%) используется на синтез АТФ. Суммарная формула гликолиза имеет следующий вид:
С2Н12О6+2АДФ++2Фн+2НАД+ ⟶2С3Н6О3+2АТФ+2Н2О+2НАДН+Н+.
Дальнейшая судьба ПВК и НАД Н + Н+ складывается по разному. При
недостатке кислорода в дрожжах происходит спиртовое брожение – ПВК восстанавливается до этилового спирта:
СН3СОСООН ⟶ СН3СОН + СО2
СН3СОН + НАДН+Н+ ⟶ С2Н5ОН + НАД+.
В клетках животных в бескислородной среде пируват восстанавливается за счет НАДН+Н+ до молочной кислоты (лактата), происходит молочнокислое брожение:
СН3СОСООН + НАДН +Н+⟶ С3Н6О3 + НАД+.
Если же процесс идет в присутствии кислорода (аэробные условия), то ПВК и НАДН +Н вступают в реакции биологического окисления.
3-й этап - кислородный (дыхание). Биологическое окисление протекает в митохондриях и представляет собой цепь реакций, контролируемых ферментами внутренней мембраны и матрикса митохондрий. Попав в митохондрию, пируват подвергается окислению и декарбоксирированию, при этом отщепившийся диоксид углерода выводится из клетки, ПВК переходит в ацетилкофермент А (ацетил-КоА), который вовлекается в цикл трикарбоновых кислот (цикл Кребса), а атомы водорода в виде восстановленных коферментов НАД направляются к внутренней мембране митохондрий.
В цикле Кребса, состоящего из последовательных ферментативных реакций, из ацетил-КоА образуются две молекулы СО2, молекула АТФ и четыре пары атомов водорода, передаваемые на НАД и ФАД (флавинадениндинуклеотид). Суммарную реакцию гликолиза и цикла Кребса можно представить в следующем виде:
C6H2O6 + 6H2O ⟶ 6CO2 + 4АТФ +12(НАДН + Н+ + ФАДН2).
Восстановленные НАДН + Н+ и ФАДН2 транспортируют атомы водорода к внутренней мембране митохондрий, где передают их по цепи встроенных в мембрану белков. Транспорт частиц по цепи осуществляется так, что протоны остаются на внешней стороне внутренней мембраны митохондрий и накапливаются в межмембранном пространстве, а электроны передаются на внутреннюю поверхность внутренней мембраны митохондрий, где взаимодействуют с их конечным акцептором – кислородом:
О2 + ē ⟶ О2-.
В результате работы ферментов цепи переноса электронов внутренняя мембрана митохондрии изнутри заряжается отрицательно, а снаружи – поло- жительно, что приводит к образованию разности потенциалов. Когда разность потенциалов на мембране достигнет критического уровня (200 мВ), положительные заряженные частицы Н+ силой электрического поля начинают проталкиваться через канал встроенного в мембрану АТФазного комплекса и, оказавшись на внутренней поверхности мембраны, взаимодействуя с кислородом, образуют воду:
1/2О2 + 2Н+ ⟶ Н2О.
При этом энергия транспортирующихся ионов водорода используется для фосфорилирования АДФ в АТФ:
АДФ +Фн ⟶ АТФ.
Суммарные реакции клеточного дыхания:
1)C6H2O6 + 6H2O ⟶ 6CO2 + 12H2 + 4АТФ (гликолиз, цикл Кребса);
2) 12H2 + 6O2 ⟶ 12H2O +34АТФ;
3) C6H12O 6 + 6O2 ⟶ 6CO2 + 6H2O + 38АТФ.
Пластический обмен
Пластический обмен – совокупность реакций биологического синтеза,
в результате которого из простых низкомолекулярных веществ, поступающих в клетку извне, образуются сложные вещества, подобные содержимому клетки. Гетеротрофная ассимиляция сводится к перестройке органических веществ, поступающих с пищей. Автотрофные организмы способны самостоятельно и полностью синтезировать органические молекулы из неорганических веществ, поступающих в клетку их внешней среды. В процессе автотрофной ассимиляции реакции фото– и хемосинтеза обеспечивают образование простых органических соединений, из которых в дальнейшем синтезируются макромолекулы.
Фотосинтез
Фотосинтез – образование органических соединений из неорганических, при использовании энергии солнечного света. Фотосинтез протекает в клетках растений и некоторых бактериях, содержащих фотосинтезирующие пигменты, обладающие уникальным свойством – улавливать свет и трансформировать его энергию в энергию химических связей. Главным фотосинтезирующим пигментом растений является хлорофилл, который встроен во внутреннюю мембрану тилакоидов хлоропластов.
Процесс фотосинтеза состоит из двух последовательных фаз: световой и темновой. Световые реакции фотосинтеза протекают только на свету в гранах тилакоидов при участии хлорофилла, белков-переносчиков и АТФазы.
Кванты видимого света (фотоны) взаимодействуют с молекулами хлорофилла, переводя их в возбужденное состояние, связанное с потерей ими электронов:
хл +hv ⟶ хл +e-.
Эти электроны передаются переносчиками на наружную (обращенную к матриксу) поверхность мембраны тилакоида, где накапливаются. Одновременно внутри полостей тилакоидов происходит фотолиз воды под действием энергии света:
H2O + hv ⟶ H++OH-.
Ионы гидроксила отдают свои электроны, превращаясь в реакционноспособные радикалы ОН:
OH- - e- ⟶ OH.
Образовавшиеся электроны передаются переносчиками к молекулам хлорофилла, восстанавливая его, а радикалы ОН объединяясь, образуя воду
и свободный кислород:
4OH ⟶ 2H2O + O2.
Протоны водорода, образовавшиеся при фотолизе воды, не могут проникнуть через мембрану граны и накапливаются внутри ее. В результате внутренняя поверхность мембраны граны заряжается положительно, а наружная – отрицательно. На мембране создается разность потенциалов, которая возрастает и, достигнув критической величины, начинает проталкивать протоны через канал АТФ-синтетазы. На выходе из протонного канала накапливается высокий уровень энергии, достаточный для синтеза АТФ из АДФ:
АДФ +Фн ⟶ АТФ.
Ионы водорода, оказавшись на наружной поверхности мембраны тилокоида, встречаясь там с электронами, образуют атомарный водород, который идет на восстановление специфического переносчика НАДФ (никотинамидадениндинуклеотид). Таким образом, во время световой фазы фотосинтеза происходит образование кислорода, диффундирующего в атмосферу, НАДФН2 и АТФ, транспортирующихся в матрикс пластид и участвующих в процессах темновой фазы.
2H+ +4e- +НАДФ+ ⟶ НАДФН2.
Темновая фаза фотосинтеза протекает в матриксе хлоропласта как на свету, так и в темноте и представляет собой ряд последовательных преобразований СО, поступающего из воздуха за счет АТФ и НАДФН+Н, и использования имеющихся в пластидах пятиуглеродных сахаров, одним из которых является рибулозодифосфат – акцептор СО. В результате образуются соединения, которые последовательно восстанавливаются до шестиуглеродной молекулы глюкозы. Суммарная реакция фотосинтеза:
6CO2 + 6H2O ⟶ С6H12O6 + 6O2.
В процессе фотосинтеза кроме глюкозы, которая превращается в крахмал и запасается растениями, синтезируются мономеры других органических молекул - аминокислоты, глицерин и жирные кислоты (рисунок 5). Благодаря фотосинтезу хлорофиллсодержащие клетки обеспечивают себя и все живое на Земле необходимыми органическими веществами и кислородом.
Хемосинтез
В природе органическое вещество создают не только зеленые растения, но и бактерии, не содержащие хлорофилла. Этот автотрофный процесс называется хемосинтезом. Осуществляется он благодаря энергии, выделяющейся при химических реакциях окисления различных неорганических соединений: водорода, сероводорода, аммиака, оксида железа (II) и др. Энергия, получаемая при окислении, запасается в организме в форме АТФ. В водоемах, вода которых содержит сероводород, живут бесцветные серобактерии. Энергию, необходимую для синтеза органических соединений из углекислого газа они получают, окисляя сероводород.
Хемосинтез - тип питания, свойственный некоторым микроорганизмам и способный создавать органические вещества из неорганических ( угольной кислоты и воды) за счет энергии, получаемой при окислении ими других неорганических веществ (например, аммиака, сероводорода).
2H2S + О2 ⟶ 2H2О + 2S + 272 кДж
Выделяющаяся в результате свободная сера накапливается в их клетках в виде множества крупинок. При недостатке сероводорода бесцветные серобактерии производят дальнейшее окисление находящейся в них свободной серы до серной кислоты. Образовавшаяся в результате энергия также используется на синтез органического вещества из углекислого газа.
2S+3О2+2H2О =2H2SО4 + 636 кДж
Чрезвычайно широко распространены в почве и в различных водоемах нитрифицирующие бактерии. Они добывают энергию путем окисления аммиака и азотистой кислоты, поэтому играют очень важную роль в круговороте азота в природе. Аммиак, образующийся при гниении белков в почве или в водоемах, окисляется нитрифицирующими бактериями, которые С.Н. Виноградский назвал нитросомонас (Nitrosomonas):
2NH3 + 3О2 ⟶ 2HNО2 + 2H2О + 662 кДж
Энергия, выделяющаяся при этом, также используется для синтеза органических соединений вследствие восстановления углекислого газа. Дальнейшее окисление образовавшейся азотистой кислоты до азотной кислоты осуществляется другой группой нитрифицирующих микроорганизмов - нитробактером (Nitrobacter):
2HNО2+ О2 = 2HNО3+ 101 кДж
Процесс нитрификации происходит в почве в огромных масштабах и служит источником нитратов. Жизнедеятельность бактерий представляет собой один из важнейших факторов плодородия почв.
Широко распространены в почве также бактерии, окисляющие водород. Водородные бактерии окисляют водород, постоянно образующийся при анаэробном (бескислородном) разложении различных органических остатков микроорганизмами почвы:
2Н2+ О2=2Н2О+ 235 кДж
Существуют бактерии, окисляющие соединения железа и марганца, они чрезвычайно широко распространены как в пресных, так и в морских водоемах. Благодаря их жизнедеятельности на дне болот и морей образуется огромное количество отложенных руд железа и руд марганца.
