
- •Термодинамика и теплопередача
- •Введение
- •Основные понятия и определения. Состояние газа Метод термодинамики. Термодинамическая система. Рабочее тело
- •Основные параметры состояния, их измерение
- •Законы идеального газа
- •Смеси идеальных газов
- •Понятие теплоемкости газов
- •Первый закон термодинамики. Газовые процессы Виды энергии, внутренняя энергия, внешняя работа
- •Уравнение первого закона термодинамики. Энтальпия газа
- •Энтропия. Свойства т, s-диаграммы
- •Термодинамические процессы, их исследование
- •Процессы сжатия в компрессоре
- •Второй закон термодинамики. Газовые циклы Цикл, его термический кпд. Понятие обратного цикла
- •Цикл Карно. Формулировки второго закона термодинамики
- •Энтропия необратимых процессов
- •Циклы двигателей внутреннего сгорания
- •Циклы газотурбинных установок
- •Водяной пар Свойства воды и водяного пара. Диаграммы состояния р, V; t, s; h, s
- •Истечение и дросселирование газов и паров
- •Цикл Ренкина. Пути повышения кпд паросиловых установок
- •Цикл холодильной установки
- •Влажный воздух
- •Основы теплообмена
- •Теплопроводность
- •Теплопроводность однослойной стенки
- •Теплопроводность многослойной плоской стенки
- •Теплопроводность цилиндрической стенки
- •Конвективный теплообмен
- •Теплопередача
- •Теплообмен излучением
- •Теплообменные аппараты
- •Библиографический список
- •Приложение
- •Термодинамика и теплопередача
- •644046, Г. Омск, пр. Маркса, 35
Энтропия необратимых процессов
Введенное в подразд. 2.3 понятие энтропии как функции состояния имеет в дифференциальной форме следующее выражение:
ds = dq / T. (3.110)
П
Рис. 3.32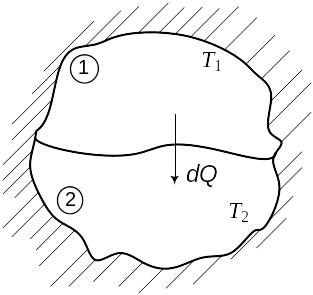
Рассмотрим изменение энтропии термодинамических систем, в которых происходят необратимые процессы.
Пусть изолированная система состоит из двух тел, имеющих различную температуру, причем T1 > T2 (рис. 3.7). Процесс теплообмена будет происходить при конечной разности температур, следовательно, он будет необратимым. Тепло будет передаваться от тела с большей температурой Т1 к телу с меньшей температурой Т2. Энтропия первого тела при передаче тепла dQ уменьшится в соответствии с формулой (3.10) на величину
ds1 = – dQ / T1, (3.111)
а энтропия второго тела возрастет на
ds2 = – dQ / T2. (3.112)
Изменение же энтропии всей рассматриваемой системы
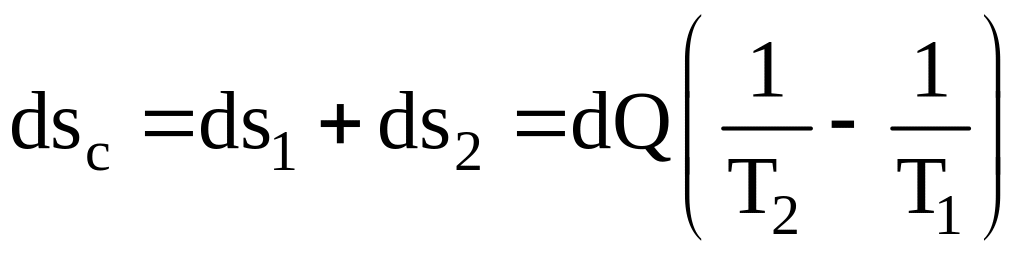 . (3.113)
. (3.113)
Так как по условию T1 > T2, то
dsc > 0. (3.114)
Следовательно, в результате необратимого процесса теплообмена между телами замкнутой изолированной системы энтропия последней возрастает.
Необратимый перенос тепла от горячего тела к холодному может быть осуществлен также посредством совершения необратимого цикла. Для этого термодинамическая система кроме источников тепла (или тел с различной температурой) должна включать в себя рабочее тело. Однако введение рабочего тела не должно повлиять на изменение энтропии системы, так как за цикл рабочее тело возвращается в исходное состояние и изменения его энтропии не происходит: Δsр.т = 0.
Поэтому не только при непосредственном теплообмене между телами, но и в случае совершения изолированной системой необратимого цикла энтропия ее возрастает.
Изменение энтропии изолированных систем, в которых протекают обратимые процессы, равно нулю (из соотношения ds = dQ / T при dsc = 0), тогда в общем случае для любых процессов
dsc 0. (3.115)
Таким образом, какие бы процессы ни протекали в изолированной системе, ее энтропия не может уменьшаться. Другими словами, энтропия изолированных систем стремится к максимуму. Достижение максимума энтропии соответствует полному тепловому равновесию элементов системы. Самопроизвольные процессы становятся невозможными, система становится неспособной к самопроизвольному изменению состояния.
С этих позиций можно дать следующее определение энтропии. Энтропия есть физическая величина, характеризующая обесценивание, рассеяние, деградацию энергии. Энтропия – мера работоспособности системы.
С принципом возрастания энтропии в замкнутых системах связана теория «тепловой смерти Вселенной», выдвинутая Клаузиусом. «Энтропия мира стремится к максимуму, – заявил Клаузиус, – что достигается при наступлении полного равновесия за счет односторонне протекающих в природе процессов, после чего прекращаются всякие тепловые процессы и наступает «тепловая смерть».
Ошибочность его концепций состояла в том, что он принимал Вселенную в качестве конечной изолированной системы, в то время как она бесконечна.
