
Лекция 2
.pdf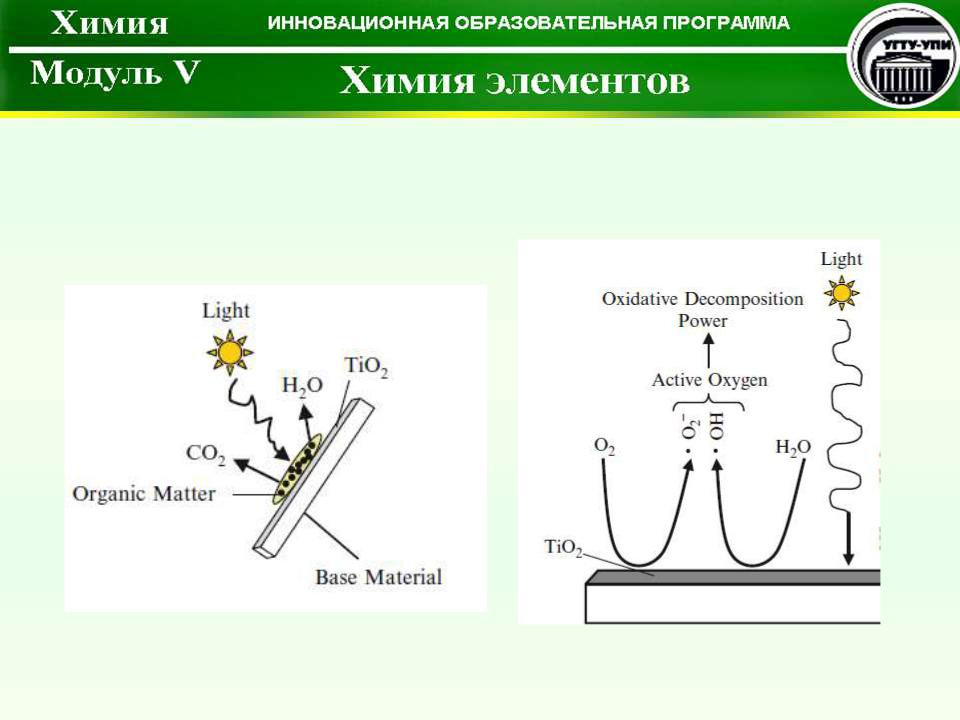
vk.com/club152685050 | vk.com/id446425943
TiO2 как фотокатализатор
vk.com/club152685050 | vk.com/id446425943
TiO2 как фотокатализатор

vk.com/club152685050 | vk.com/id446425943
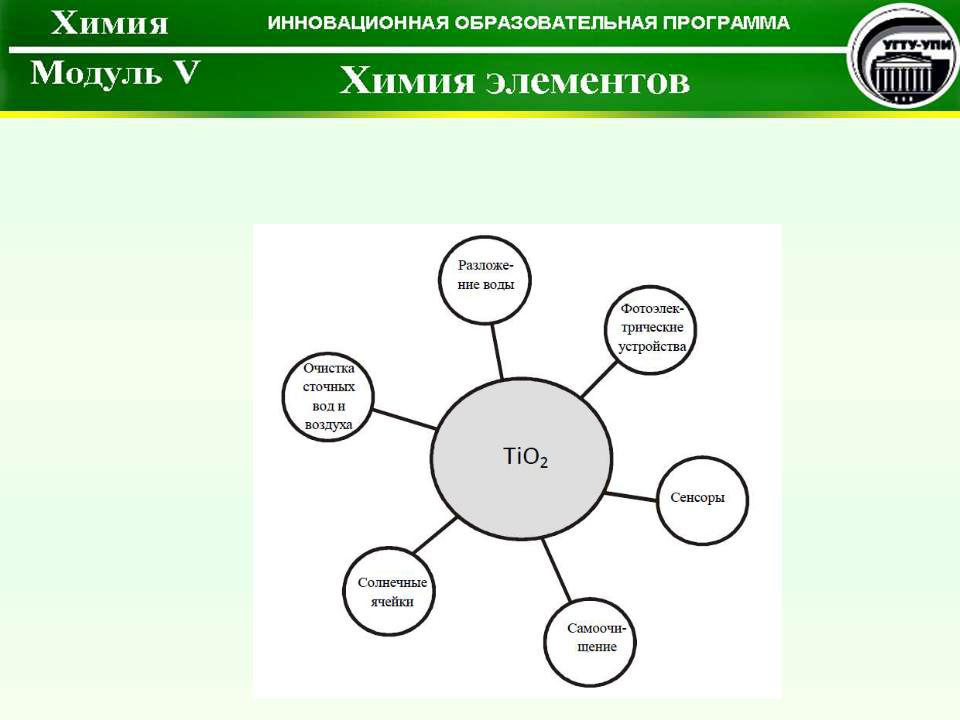
Объекты с фотокатализатором
vk.com/club152685050 | vk.com/id446425943
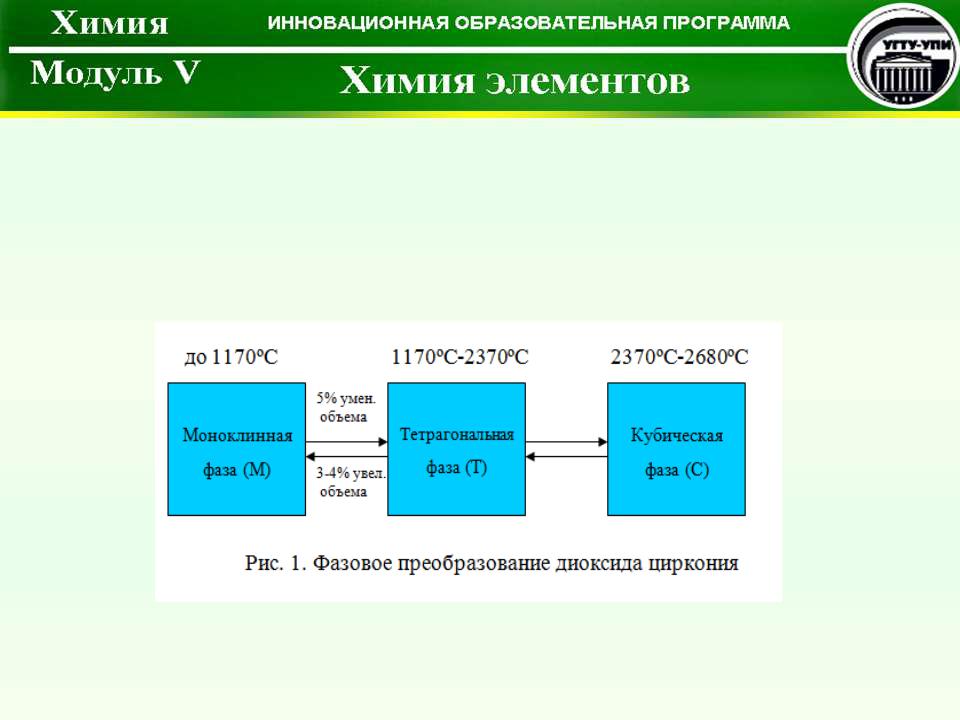
Керамика из диоксида циркония
Частично стабилизированный диоксид циркония. Образуется при добавлении в ZrO2 оксидов 2-3% моль иттрия (Y2O3).

vk.com/club152685050 | vk.com/id446425943
Керамика из диоксида циркония
vk.com/club152685050 | vk.com/id446425943
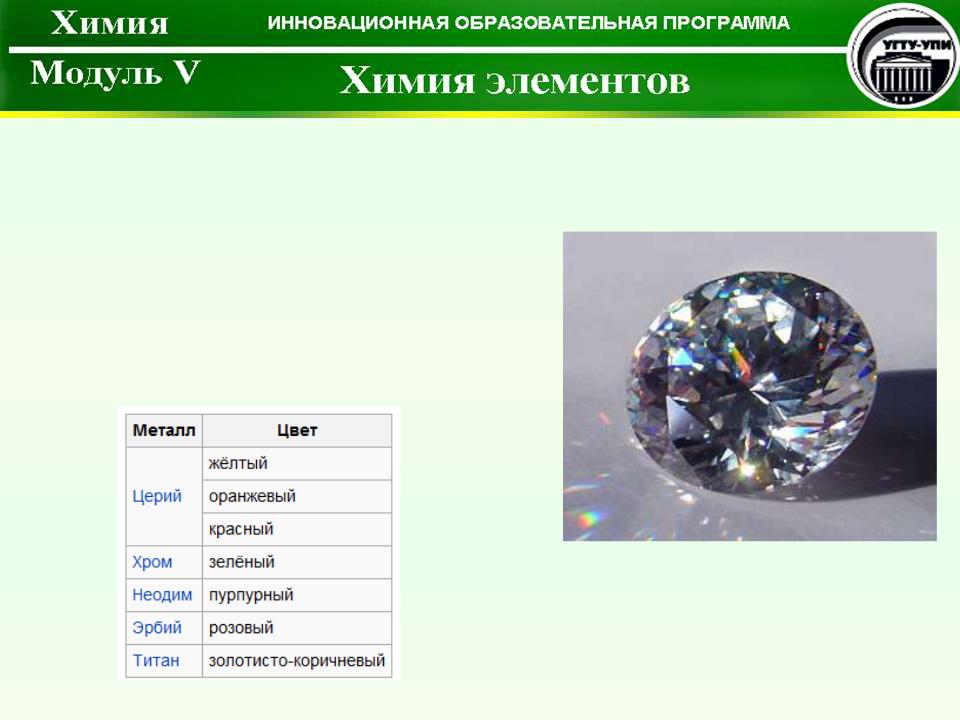
Фианиты из диоксида циркония
Для окрашивания бесцветного диоксида циркония в различные цвета добавляются переходные и редкоземельные элементы.
Название фианит получил в честь Физического института Академии наук
СССР (ФИАН)

vk.com/club152685050 | vk.com/id446425943
Галогениды
•Известны галогениды типа MeГ2, MeГ3, MeГ4.
•Тетрагалогениды – это ковалентные соединения. При растворении в воде они гидролизуются в очень большой степени.
•Галогениды используются для получении Ti, Zr, Hf.
•Выделенный из титановой руды оксид TiO2 нагревают с углем в присутствии Cl2 и получают летучий хлорид TiCl4.
TiO2 + 2С + 2Cl2= TiCl4 +2СО
•TiCl4 затем восстанавливают жидким магнием.
TiCl4 +2Mg = 2MgCl2 +Ti
•Получение и термическое разложение MeI4 лежит в основе рафинирования металлов. TiI4 2I2 + Ti
vk.com/club152685050 | vk.com/id446425943
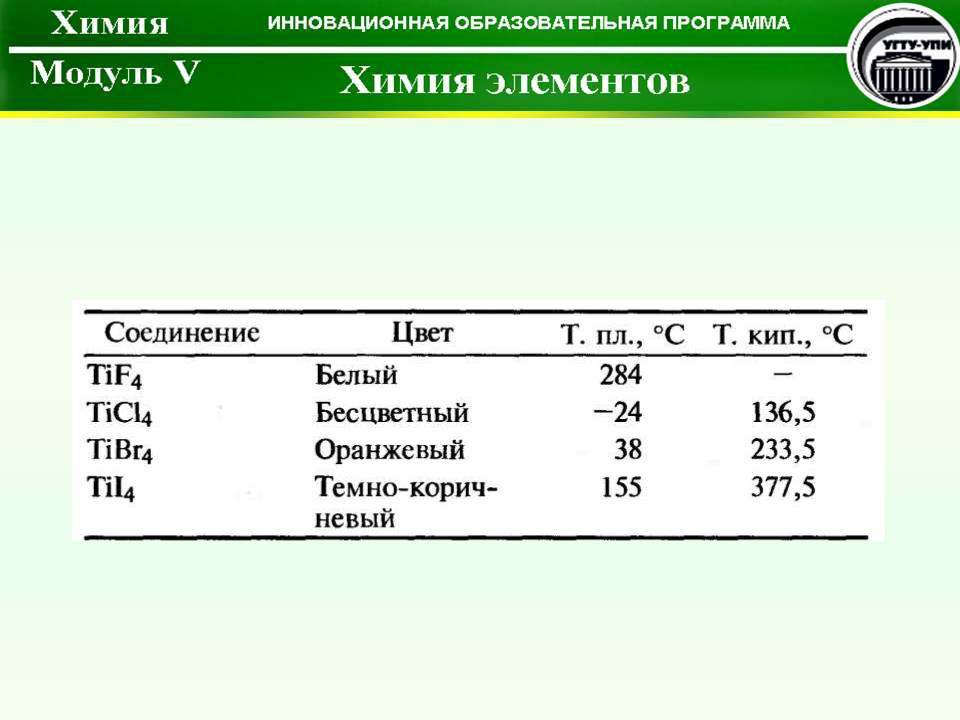
Галогениды титана

vk.com/club152685050 | vk.com/id446425943
Химия водных растворов
•В водных растворах более устойчивы соединения Me(+4).
•Галогениды, сульфаты растворимы в воде, но в растворе в
заметной степени гидролизуются.
•При обычной температуре продукты гидролиза растворимы и представляют собой аквагидроксокомплексы, в том числе полимерные, описываются условной формулой MeO2+.
•При нагревании гидролиз усиливается и полимерные аквагидроксокомплексы выпадают в осадок.
•Гидролиз условно описывают уравнениями:
• 1стадия: |
TiCl |
4 |
+ H |
O = TiO2+ + 2H++ 4Cl–; |
|
|
2 |
|
• 2 стадия (при нагревании): TiO2+ + H2O TiO(OH)2+ 2H+

vk.com/club152685050 | vk.com/id446425943
Химия водных растворов
•При добавлении щелочи к растворам соединений Me(+4)образуется бесцветные гелеобразные осадки гидратированных диоксидов с условной формулой MeO(OH)2.
•Свежеполученные осадки растворяются под действием кислот и очень концентрированной щелочи.
MeO(OH)2 + 2H+ = MeO2+ + 2H2O MeO(OH)2 + 2OH– + H2O= [Me(OH)6]2–
