
Лекция 2
.pdf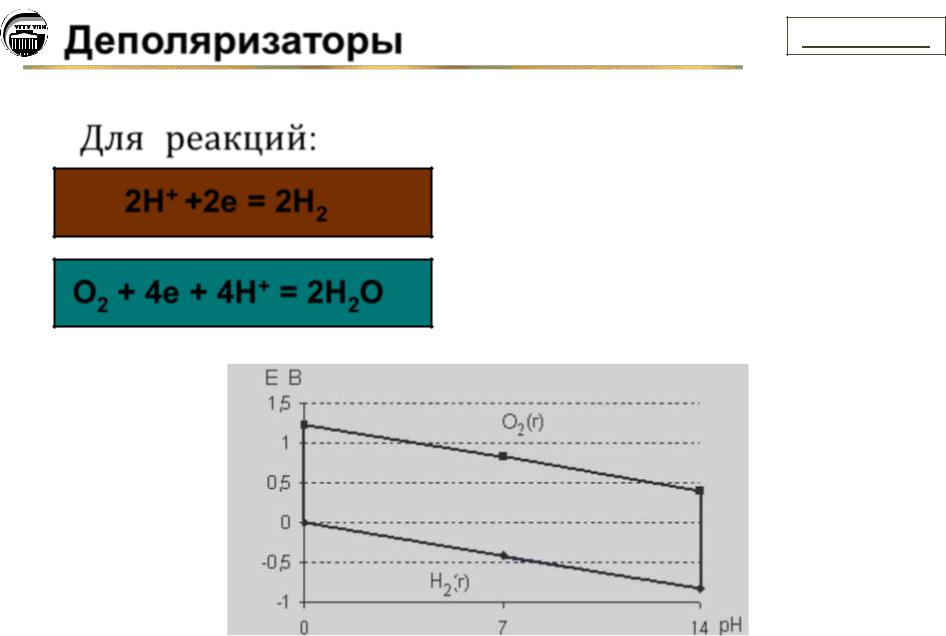
vk.com/club152685050 | vk.com/id446425943 |
|
Деполяризаторы |
содержание |
|
Для реакций:
2H+ +2e = 2H2
O2 + 4e + 4H+ = 2H2O
E |
|
|
|
|
E |
o |
|
|
0,059pH |
2H |
|
/H |
|
2H |
|
/H |
|||
|
2 |
|
2 |
||||||
|
|
|
|
||||||
|
|
|
|
|
|
|
|
E0O2 /2H 2O 1,23 0,059pH.
vk.com/club152685050 | vk.com/id446425943 |
|
Катодный процесс |
содержание |
|
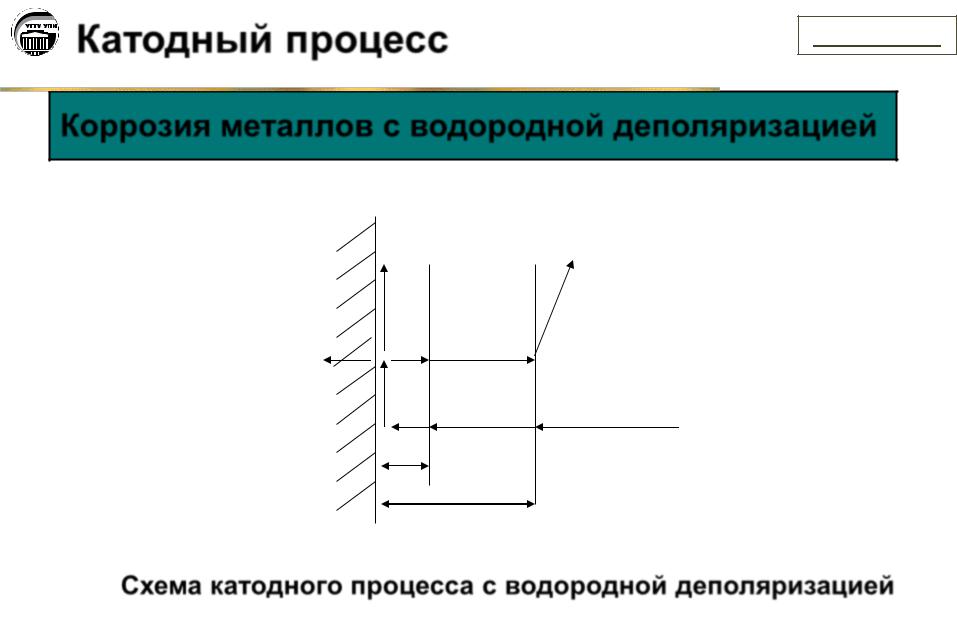
Коррозия металлов с водородной деполяризацией
Металл |
|
|
Н2 |
|
|
|
|
|
6 |
|
|
|
Раствор |
|
|
5 |
7 |
8 |
9 |
К |
3 |
2 |
1 H+ |
δ
П
Схема катодного процесса с водородной деполяризацией

vk.com/club152685050 | vk.com/id446425943 |
|
Катодный процесс |
содержание |
|
Коррозия металлов с водородной деполяризацией
E |
0 |
|
|
|
2H |
/H |
|||
|
|
|||
|
|
|
2 |
Для кислой среды
= - 0,059рН
E02H /H2 0В
Для нейтральной среды
0 |
|
|
|
E |
|
O/H |
|
2H |
2 |
2 |
|
|
|
0,414 B.
Для щелочной среды
0 |
|
|
|
E |
|
O/H |
|
2H |
2 |
2 |
|
|
|
0,827B.
Коррозия с водородной деполяризацией возможна, если:
E02H /H2 E0Me2 /Me

vk.com/club152685050 | vk.com/id446425943 |
|
Катодный процесс |
содержание |
|
Коррозия металлов с водородной деполяризацией протекает в следующих условиях:
для большинства металлов в растворах кислот
для активных металлов в нейтральных растворах
для амфотерных металлов в растворах щелочей
vk.com/club152685050 | vk.com/id446425943 |
|
Катодный процесс |
содержание |
|
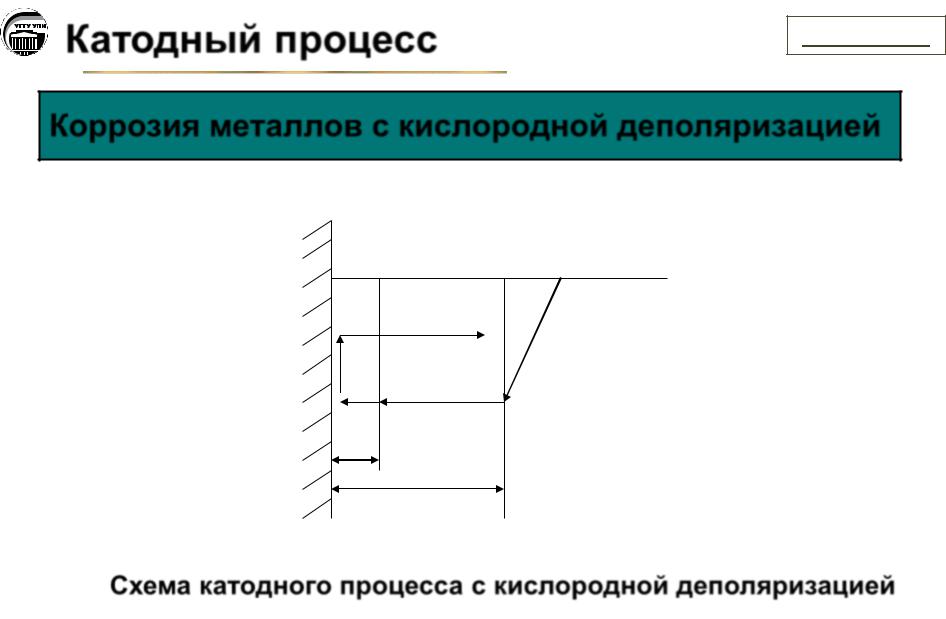
Коррозия металлов с кислородной деполяризацией
Металл
6
|
5 |
O |
2 |
|
|
||
|
|
|
|
К |
|
4 |
|
δ
 O2
O2
2
2H |
|
O 4e 4OH |
|
2 |
|
||
|
|
|
|
|
|
3 |
|
П
Схема катодного процесса с кислородной деполяризацией

vk.com/club152685050 | vk.com/id446425943 |
|
Катодный процесс |
содержание |
|
Коррозия металлов с кислородной деполяризацией
O |
|
2H |
|
O 4e 4OH |
|
2 |
2 |
|
|||
|
|
|
|
E |
0 |
|
|
|
1,23 0,059pH. |
|
O |
/2H |
2 |
O |
|||
|
|
|||||
|
2 |
|
|
|
Для кислой среды
Для нейтральной среды
E |
0 |
|
|
|
|
|
1,22B. |
|
O |
/2H |
2 |
O |
|||||
|
|
2 |
|
|
|
|
|
|
E |
0 |
|
|
|
|
|
0,81B. |
|
O |
|
/4OH |
|
|||||
|
|
|
|
|
||||
|
|
2 |
|
|
|
|
|
|
Для щелочной среды |
EO0 |
2 |
/4OH 0,40B. |
|
|
|
Коррозия с кислородной деполяризацией возможна, если:
E0O2/4OH E0Men /Me

vk.com/club152685050 | vk.com/id446425943 |
содержание |
|
Поляризация электродных процессов |
||
|
||
|
Изменение потенциала электрода при прохождении тока называется поляризацией:
Е = Еi – EР
где Е – поляризация;
Еi - потенциал электрода под током; ЕР – равновесный потенциал
vk.com/club152685050 | vk.com/id446425943 |
содержание |
|
Поляризация электродных процессов |
||
|
||
|
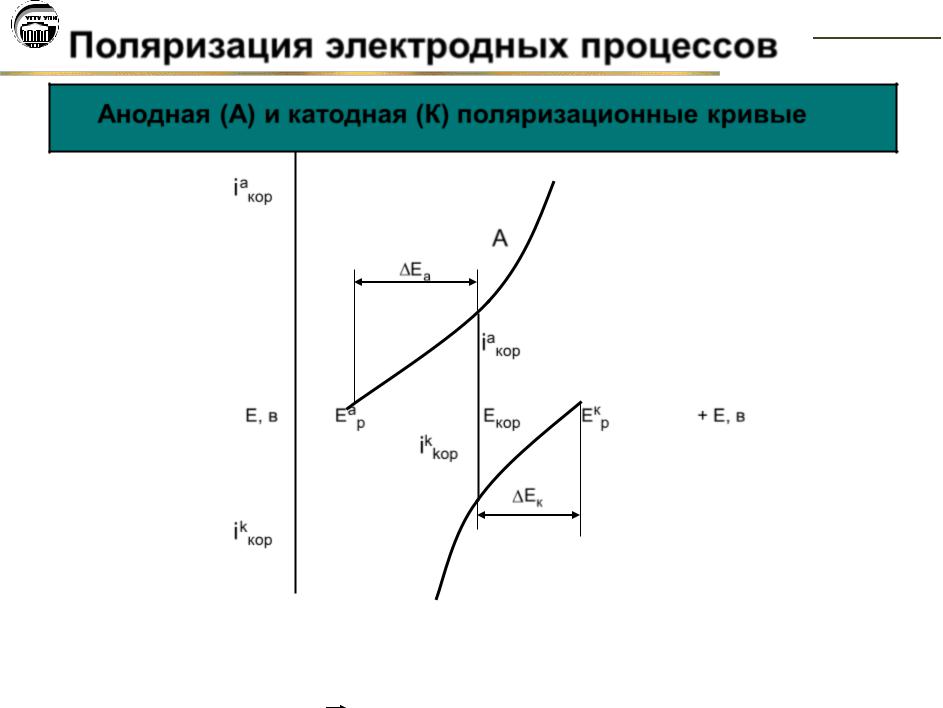
Анодная (А) и катодная (К) поляризационные кривые
iaкор
A
Еа
iaкор
|
|
|
|
|
|
|
- Е, в |
Еар |
Екор |
Екр |
+ Е, в |
||
ikkop
Ек
i |
k |
кор |
K |
|
|||
|
|
К
vk.com/club152685050 | vk.com/id446425943 |
|
Пассивация |
содержание |
|
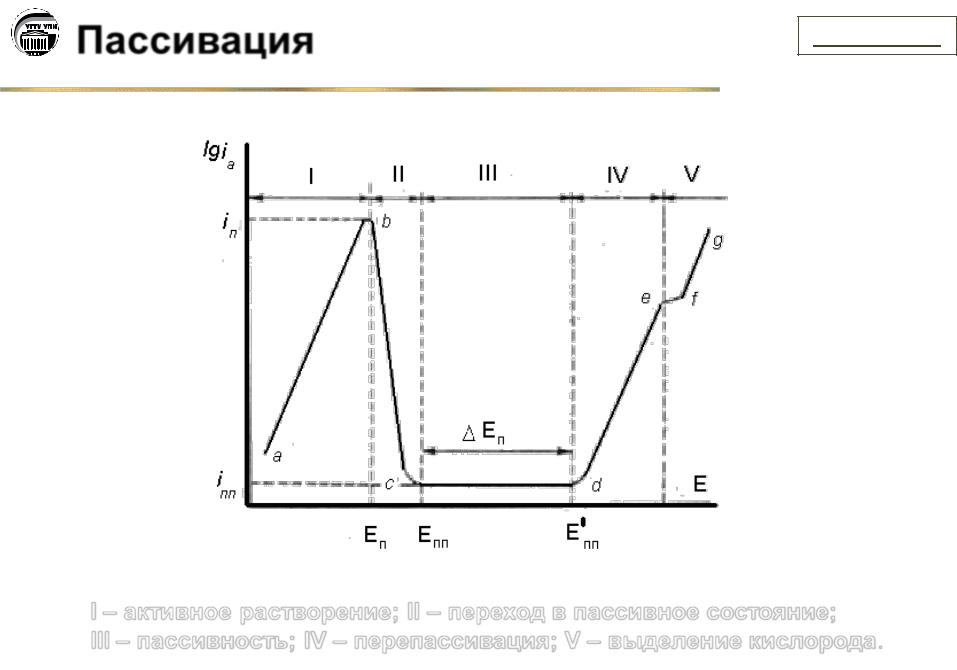
I – активное растворение; II – переход в пассивное состояние;
III – пассивность; IV – перепассивация; V – выделение кислорода.

vk.com/club152685050 | vk.com/id446425943 |
содержание |
|
Выводы и заключения |
||
|
||
|
Электрохимическая коррозия протекает через сопряженные процессы анодного растворения металла и катодного восстановления окислителя.
