
Лекция 2
.pdf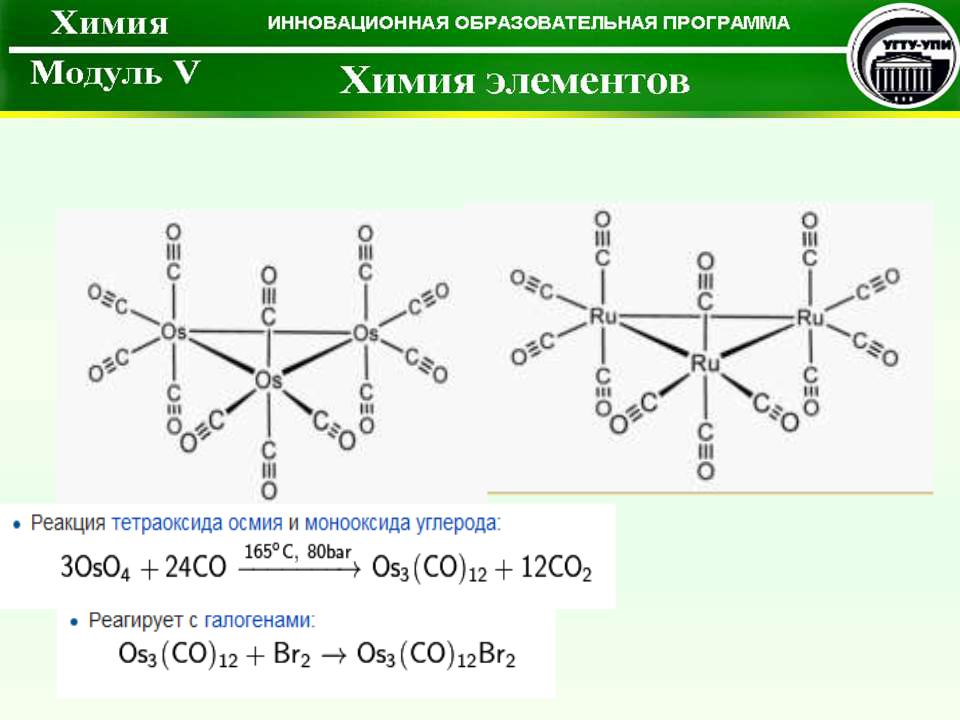
vk.com/club152685050 | vk.com/id446425943
Додекакарбонилтриосмий |
Додекакарбонилрутений |
vk.com/club152685050 | vk.com/id446425943

vk.com/club152685050 | vk.com/id446425943
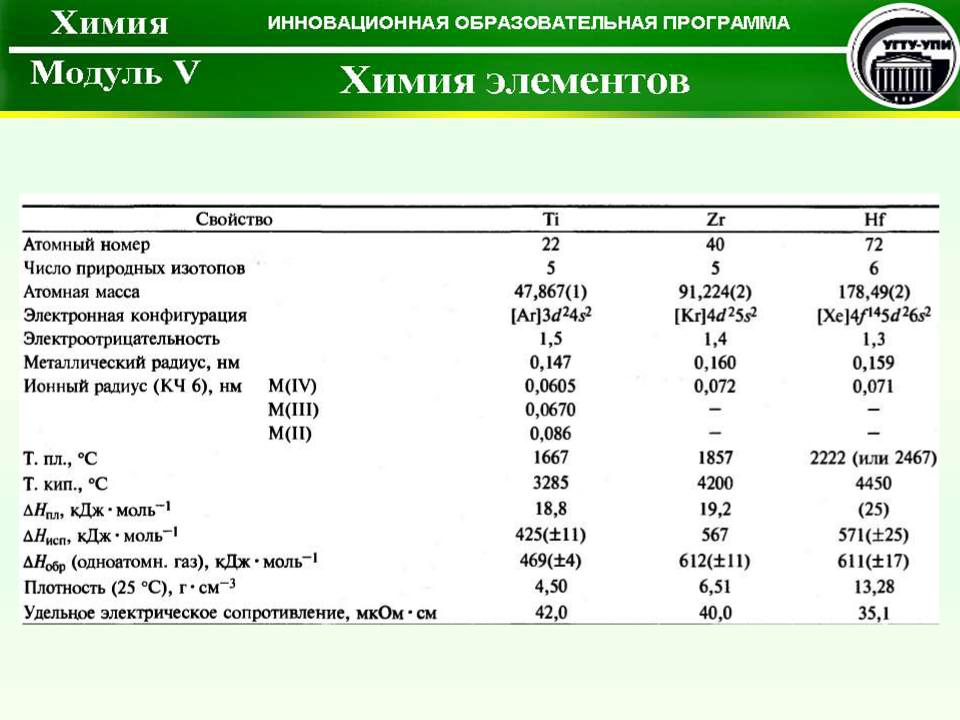
Металлы IVБ-подгруппы

vk.com/club152685050 | vk.com/id446425943
Металлы IVБ-подгруппы
Основные вопросы, рассматриваемые в лекции
Общая характеристика металлов IVБ-подгруппы. Электронное строение, наиболее характерные степени окисления.
Природные соединения
Свойства простых веществ
Соединения
Оксиды
Галогениды
Химия водных растворов

vk.com/club152685050 | vk.com/id446425943
|
|
IV |
|
|
|
|
|
|
4 |
22 |
Ti |
|
титан |
||
|
|
||
IV |
|
47,88 |
|
|
5 |
Ge |
32 |
|
72,59 |
|
|
|
|
|
|
|
|
|
|
|
6 |
40 |
Zr |
|
цирконий |
||
V |
|
||
|
91,224 |
||
|
7 |
Sn |
50 |
|
118,71 |
||
|
|
||
|
8 |
72 |
Hf |
|
гафний |
||
VI |
|
178,49 |
|
|
9 |
Pb |
82 |
|
207,2 |
||
|
|
||
VII |
10 |
104 |
Rf |
|
|
[261] |
|
|
|
|
|
Общая характеристика
•IVБ-подгруппу образуют
d-элементы: Ti, Zr, Hf, Rf.
•Валентные электроны: (n–1)d2ns2
•Самой устойчивой у всех этих элементов является высшая степень окисления +4.
•У титана есть также степени окисления: +3 и
+2.
•Соединения Ti в этих степенях окисления проявляют восстановительные свойства
•Цирконий и гафний очень похожи между собой.
•Наибольшее практическое значение имеет титан.

vk.com/club152685050 | vk.com/id446425943
|
|
IV |
|
|
|
|
|
|
4 |
22 |
Ti |
|
титан |
||
|
|
||
IV |
|
47,88 |
|
|
5 |
Ge |
32 |
|
72,59 |
|
|
|
|
|
|
|
|
|
|
|
6 |
40 |
Zr |
|
цирконий |
||
V |
|
||
|
91,224 |
||
|
7 |
Sn |
50 |
|
118,71 |
||
|
|
||
|
8 |
72 |
Hf |
|
гафний |
||
VI |
|
178,49 |
|
|
9 |
Pb |
82 |
|
207,2 |
||
|
|
||
VII |
10 |
104 |
Rf |
[261] |
|
||
|
|
|
|
|
|
|
|
Общая характеристика
•Высшие оксиды и гидроксиды всех металлов имеют амфотерный характер, основные свойства заметно усиливаются при переходе от Ti к Hf.
•К амфотерным относят оксид и гидроксид Ti(+3), но у него преобладает основной характер. Оксид Ti(+2) – основной.
•Соединения Me(+4) являются не ионными, а ковалентными соединениями, которые в водных растворах в сильной степени гидролизуются.

vk.com/club152685050 | vk.com/id446425943
Природные соединения
•Содержание Ti в Земной коре – около 0,5 масс.%, т.е. Ti – распространенный элемент.
• Содержание Zr – 2 .10–2 масс. % ; Hf – 4.10–4 %.
•Все металлы в природных соединениях находятся в степени окисления (+4).
•Основные минералы Ti:
•рутил – TiO2;
•ильменит – FeO . TiO2 ( FeTiO3); перовскит CaO . TiO2 ( CaTiO3);
•титаномагнетит – [(FeO . TiO2) . (FeO . Fe2O3)n].
•Наиболее важные минералы Zr:
• |
циркон – ZrSiO4, бадделит ZrO2; |
Минерал ильменит |
• |
Hf сопутствует Zr. |
|
vk.com/club152685050 | vk.com/id446425943

vk.com/club152685050 | vk.com/id446425943
Нейтронной прозрачности (крайне низкое сечение поглощения нейтронов), прочность и высокая коррозионная стойкость циркония

vk.com/club152685050 | vk.com/id446425943
Простые вещества
•Простые вещества элементов IVБ-группы – серебристо-серые металлы, с высокими температурами плавления, повышающимися при переходе от Ti к Hf.
•Титан относится к легким , Zr и Hf – к тяжелым металлам.
•Все металлы отличаются высокой коррозионной стойкостью.
•Причиной стойкости являются поверхностные тонкие пленки инертных оксидов типа МеО2.
•При температуре больше 600оС компактные металлы сгорают в кислороде с образованием оксидов МО2.
Me + О2 = MeO2
