
Уравнение Клапейрона – Клаузиуса
Рассмотрим цикл Карно для системы, состоящей из двух фаз единичной массы, находящихся в равновесии (например, жидкость и газ). Будем считать, что температуры нагревателя и холодильника отличаются на очень малую величину dТ.
Процесс перехода из 1 в 2 изотермический. Для осуществления фазового перехода нужно отобрать у вещества количество тепла (для единицы массы вещества = q). Это количество теплоты соответствует теплу, получаемому за цикл от нагревателя Q1
![]()
 .
.
1 и 2 – однофазное состояние;
промежутки между 1 и 2 – двухфазное.
П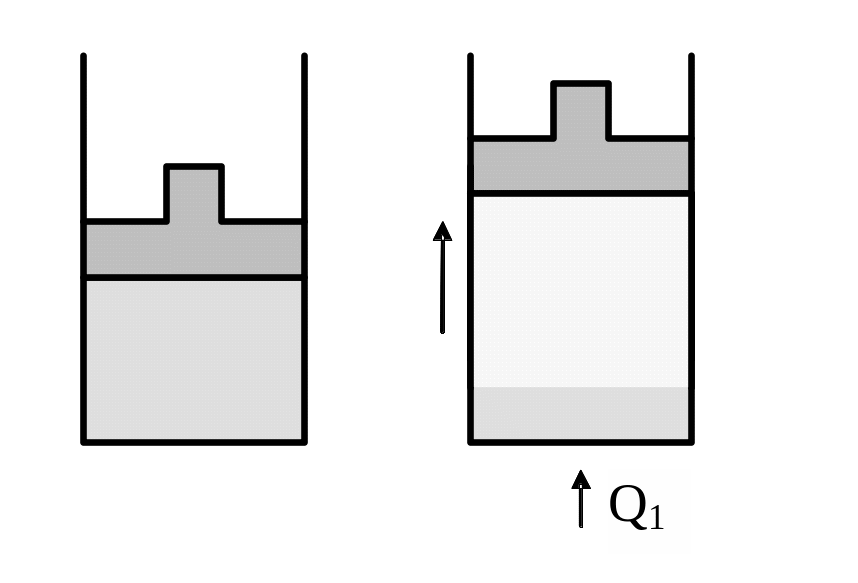 ри
сообщении системе тепла Q1
жидкость
будет испаряться, и совершать работу,
например, поднимая поршень. Когда
испариться единица массы жидкости,
уберем тепловой контакт и заставим
систему расширяться по короткой адиабате
2-3 до тех пор, пока температура системы
не будет равна температуре холодильника.
Из состояния 3 вернем систему по изотерме
3-4 и адиабате 4-1 в исходное состояние 1,
т.е. совершим цикл Карно.
ри
сообщении системе тепла Q1
жидкость
будет испаряться, и совершать работу,
например, поднимая поршень. Когда
испариться единица массы жидкости,
уберем тепловой контакт и заставим
систему расширяться по короткой адиабате
2-3 до тех пор, пока температура системы
не будет равна температуре холодильника.
Из состояния 3 вернем систему по изотерме
3-4 и адиабате 4-1 в исходное состояние 1,
т.е. совершим цикл Карно.
Работа, совершаемая за цикл, будет равна площади заштрихованной фигуры
![]()
![]() .
.
По определению
К.П.Д. цикла Карно
![]() .
.
Откуда
![]() - уравнение
Клапейрона-Клаузиуса.
- уравнение
Клапейрона-Клаузиуса.
Это уравнение связывает производную от равновесного давления по температуре с теплотой перехода, температурой и разностью удельных объемов фаз, находящихся в равновесии. Уравнение Клапейрона-Клаузиуса справедливо не только для испарения, но и для других фазовых превращений, связанных с выделением или поглощением теплоты.
В случае плавления, например, можно записать
![]() ,
,
где q23 – удельная теплота плавления;
V2 и V3 – удельные объемы жидкой и твердой фазы;
Т – температура плавления.
Если V2
> V3
, то
![]() .
С повышением давления точка плавления
возрастает.
.
С повышением давления точка плавления
возрастает.
Если V2
< V3
, то
![]() .
С повышением давления температура
плавления понижается.
.
С повышением давления температура
плавления понижается.
Так для воды V3 -V2 = 9,1*10-2 см3 /г; Т= 273°К; q=80 кал/г; dP/dT=134атм/К. Значит, что с увеличением давления на одну атмосферу Тпл льда понижается на 0,0075градуса.
Диаграмма фазовых переходов
А)
Р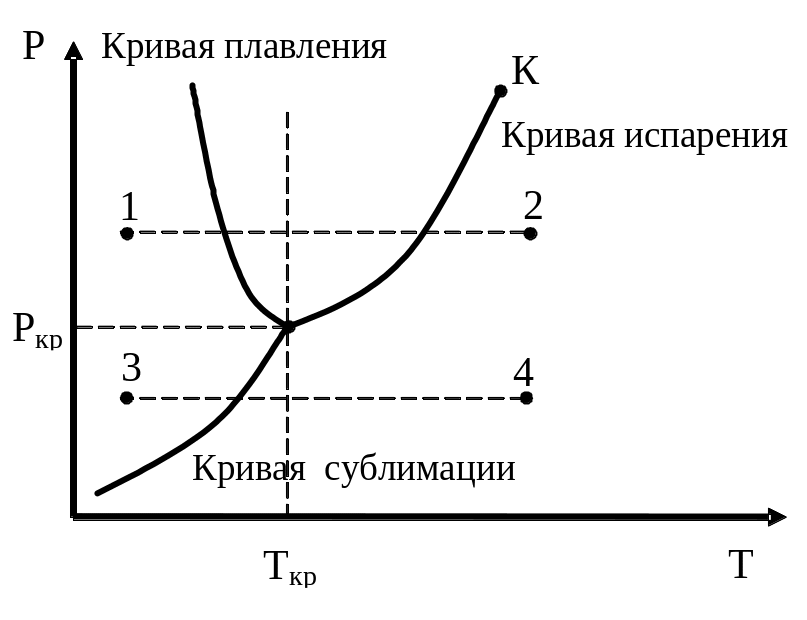 ассмотрим
состояние сис-темы, в которой число фаз,
находящихся в равновесии друг с другом,
равно трем. Примером такой системы может
служить система твердое тело → жидкость
→ пар.
ассмотрим
состояние сис-темы, в которой число фаз,
находящихся в равновесии друг с другом,
равно трем. Примером такой системы может
служить система твердое тело → жидкость
→ пар.
Возьмем сначала систему жидкость → пар, и будем от-нимать у нее тепло (охлаждать).
Точка, изображающая сос-тояние системы, будет пере-мещаться вниз по кривой испарения, пока не достигнет значения Ткр . Здесь будет кристаллизация. Эта температура и соответствующее ей значение Ркр будут единственной точкой, где существуют одновременно три состояния вещества: жидкое, твердое и газообразное. Она называется тройной точкой.
Б)
Е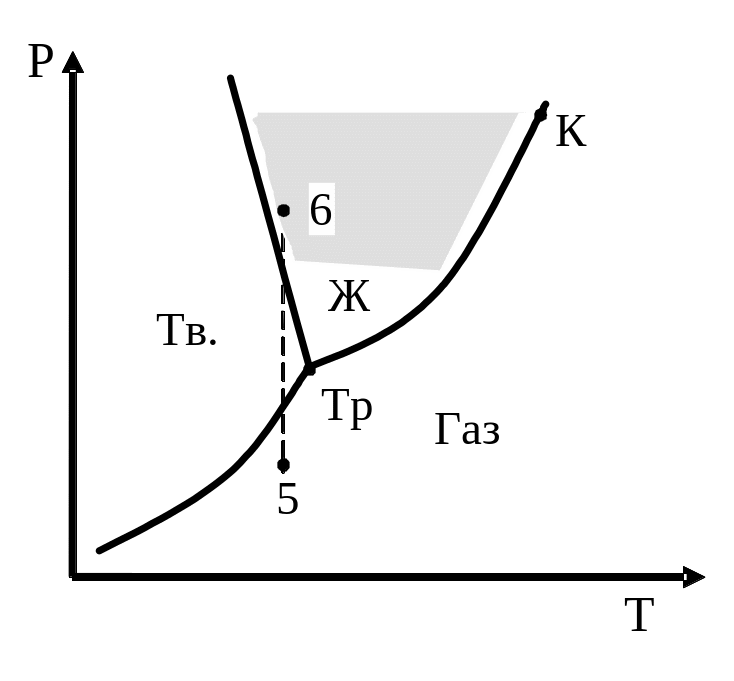 сли
продолжать отнимать тепло (охлаждать
тело), то точка, изображающая состояние
системы, переместится вниз по кривой
сублимации.
сли
продолжать отнимать тепло (охлаждать
тело), то точка, изображающая состояние
системы, переместится вниз по кривой
сублимации.
В зависимости от соотношений между удельными объемами твердой и жидкой фаз кривая плавления будет иметь либо вид , показанный на предыдущем рисунке, либо будет выглядеть так :
Все три кривые разбивают координатную плоскость на три области жидкость – газ - твердое тело.
Каждая точка такой области соответствует определенному равновесному состоянию вещества, поэтому ее называют диаграммой состояния.
Для веществ с несколькими кристаллическими модификациями диаграмма состояния имеет более сложный вид.
В)
З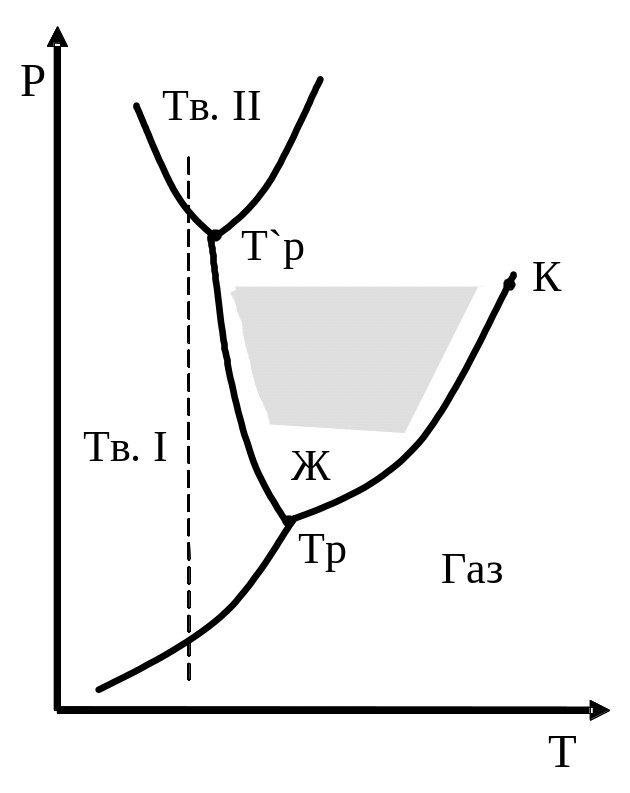 десь
число кристаллических состояний равно
двум (имеем две тройные точки Тр
и
Тр'.
десь
число кристаллических состояний равно
двум (имеем две тройные точки Тр
и
Тр'.
Зная диаграмму состояния можно предсказать, в каком состоянии будет вещество при различных условиях, а также, какие превращения оно будет претерпевать при различных процессах.
Пример
Переход 1-2: изобарическое нагревание кристалл→жидкость→газ;
Переход 3-4: изобарическое нагревание кристалл→газ.
У большинства веществ тройная точка лежит ниже атмосферного давления. Поэтому переход из твердого состояния в газообразное осуществляется через промежуточную – жидкую – фазу. Но могут быть и другие переходы.
Для углекислоты давление тройной точки Р=5,11 атм. Поэтому при атмосферном давлении она может существовать только в твердом (точка 3) и газообразном (точка 4) состоянии.
Если удельный объем кристаллов превосходит удельный объем жидкой фазы, то, пользуясь диаграммой (б), переход из 5 в 6 будет проходить через состояния газ→ кристалл→ жидкое состояние. Отметим еще одну особенность диаграммы состояния: кривая испарения заканчивается в критической точке К. Поэтому возможен переход из жидкого состояния в газообразное в обход критической точки без пересечения кривой испарения. Этот переход совершается непрерывно через последовательность однофазных состояний, у которых отсутствует анизотропия.
Анизотропия изменяется только скачком (либо она есть, либо ее нет). Поэтому кривая плавления уходит в бесконечность, а кривая сублимации – в точку Р=0, Т=0
