
- •Оксидиметрия.Перманганатометрия
- •1.Сколько граммов кристаллогидрата щавелевой кислоты нужно взять для приготовления 250 мл раствора с молярной концентрацией эквивалента 0,01 моль/дм3?
- •2.Рассчитать молярную концентрацию эквивалента раствора щавелевой кислоты, если для его приготовления навеску 3,2576 г h2c2o4*2h2o растворили в воде в мерной колбе объёмом 500 мл?
- •1.Рассчитать навеску перманганата калия, которая потребуется для приготовления 500 мл раствора с молярной концентрацией эквивалента 0,01 моль/дм3 для титрования в кислой среде?
- •2.Рассчитать молярную концентрацию эквивалента раствора перманганата калия, если для его приготовления навеску 1,67 г перманганата калия растворили в мерной колбе объёмом 500 мл (среда кислая)?
- •3.Рассчитать объём раствора kMnO4 с молярной концентрацией эквивалента 0,1 моль/дм3, который потребуется для приготовления 500 мл раствора с молярной концентрацией эквивалента 0,05 моль/дм3?
Оксидиметрия.Перманганатометрия
Теоретическая часть.
|
Перманганатометрия - титриметрический метод, в котором в качестве рабочего раствора применяется перманганат калия KMnO4. |
||
Окислительные свойства перманганата калия. |
|||
Среда |
Уравнение реакции |
f |
|
Кислая |
MnO4- +5e- +8H+ = Mn2+ +4H2O |
1/5 |
|
Нейтральная |
MnO4- + 2H2O + 3e- = MnO2↓+ 4OH- |
1/3 |
|
Щелочная |
MnO4- + e- = MnO42- |
1 |
|
Исходные растворы:
|
Рабочий раствор: Перманганат калия – KMnO4 |
||
Способ приготовления: |
|||
|
|
||
Уравнение метода 2KMnO4+3H2SO4+5H2C2O4=2MnSO4+K2SO4+10CO2+8H2O MnO4-+8H++5e-→ Mn2++4H2O C2O42- + 2e-→ 2CO2 |
|||
Перманганат калия: f = 1/5 М = 158,03 г/моль Mf = 31,61г/моль |
Щавелевая кислота- H2 C2 O4 * 2H2 O f = 1/2 М = 126,06 г/моль Mf = 63,03 г/моль |
||
*Если в условиях задачи не указана среда, это означает, что анализ проводится в кислой среде. |
|||
1.Приготовление исходных растворов. |
Обучающие задачи |
1.Сколько граммов кристаллогидрата щавелевой кислоты нужно взять для приготовления 250 мл раствора с молярной концентрацией эквивалента 0,01 моль/дм3?
-
Дано:
Решение:
V=250 мл=0,25 л
Сf=0,01 моль/дм3
M=?
1.Рассчитать молярную массу H2C2O4*2H2O:
М = (1,01•2+12,01•2+16•4)+18,01•2=126,06 г/моль
2. Рассчитать молярную массу эквивалента H2C2O4*2H2O:
f=1/2

3.Рассчитать навеску щавелевой кислоты:
m= Сf •Mf •V
mкислоты=0,01 моль/дм3 • 63.03 г/моль• 0,25 л=0,1576 г.
Ответ: Для приготовления 250 мл раствора щавелевой кислоты с Сf=0,01 моль/дм3 потребуется 0,1576 г кристаллогидрата.
2.Рассчитать молярную концентрацию эквивалента раствора щавелевой кислоты, если для его приготовления навеску 3,2576 г h2c2o4*2h2o растворили в воде в мерной колбе объёмом 500 мл?
-
Дано:
Решение:
m=3,2576 г
V=500 мл
Сf=?
1.Рассчитать титр щавелевой кислоты:


2.Записать молярную массу эквивалента H2C2O4*2H2O:
М = 126.06 г/моль
f = 1/2
Mf = 63.03 г/моль
3.Рассчитать молярную концентрацию эквивалента щавелевой кислоты:
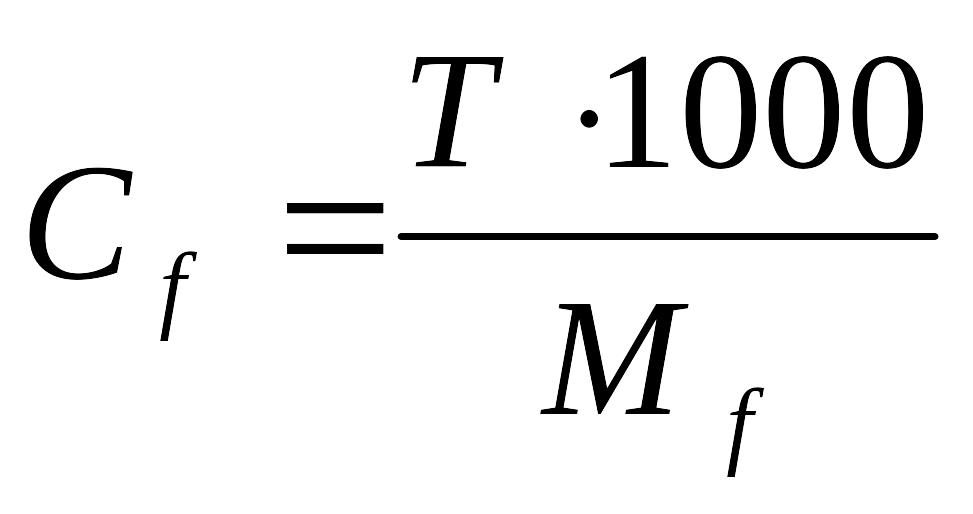

Ответ: Молярная концентрация эквивалента раствора щавелевой кислоты равна 0,1034 моль/л.
3.Рассчитать навеску, необходимую для приготовления 250 мл раствора кристаллогидрата щавелевой кислоты с Т=0,01254 г/мл?
-
Дано:
Решение:
V=250 мл
Т=0,01254 г/мл
m=?
1.Рассчитать навеску H2C2O4*2H2O, необходимую для приготовления раствора:
m=T ∙ V
mкислоты=0,01254 г/мл ∙ 250 мл = 3,1350 г.
Ответ: Для приготовления 250 мл раствора щавелевой кислоты с Т=0,01254 г/мл потребуется 3,1350 г кристаллогидрата.
Задачи для самостоятельного решения.
1.Сколько граммов H2C2O4*2H2O нужно взять для приготовления 5 л раствора с молярной концентрацией эквивалента 0,1 моль/дм3?
( Ответ: m=31,5150 г )
2.Рассчитать молярную концентрацию эквивалента раствора щавелевой кислоты, если для его приготовления навеску 1,5563 г H2C2O4*2H2O растворили в воде в мерной колбе объёмом 500 мл? Написать алгоритм приготовления раствора.
( Ответ: Сf= 0,04939 моль/л )
3.Сколько граммов кристаллогидрата оксалата аммония нужно взять для приготовления 500 мл раствора с Т =0,003459 г/мл?
(Ответ: m=1,7295 г )
4.Сколько граммов оксалата натрия нужно взять для приготовления 500 мл раствора с молярной концентрацией эквивалента 0,05 моль/дм3?
( Ответ: m=1,6750 г )
5.Рассчитать молярную концентрацию эквивалента раствора, если для его приготовления лаборант взвесил навеску 1,4506 г кристаллогидрата оксалата аммония, перенёс её количественно в мерную колбу объёмом 200 мл и довёл до метки дистиллированной водой? Перечислить посуду для приготовления раствора.
( Ответ: Сf=0,1021 моль/л )
6.Рассчитать навеску, необходимую для приготовления 2,5 л раствора оксалата натрия с Т=0,006547 г/мл?
( Ответ: m=16,3675 г )
7.Сколько граммов кристаллогидрата оксалата аммония нужно взять для приготовления 200 мл раствора с молярной концентрацией эквивалента 0,5 моль/дм3?
( Ответ: m=7,1060 г )
8.Рассчитать молярную концентрацию эквивалента раствора оксалата натрия, если для его приготовления навеску 1,6812 г оксалата натрия растворили в воде в мерной колбе объёмом 250 мл? Написать алгоритм приготовления раствора.
( Ответ: Сf=0,1004 моль/л )
9.Сколько граммов кристаллогидрата щавелевой кислоты нужно взять для приготовления 200 мл раствора с Т =0,003378 г/мл?
( Ответ: m=0,6756 г )
10.Сколько граммов H2C2O4*2H2O нужно взять для приготовления 1000 мл раствора с молярной концентрацией эквивалента 0,05 моль/дм3?
( Ответ: m=3,1515 г )
11.Рассчитать молярную концентрацию эквивалента раствора, если для его приготовления лаборант взвесил навеску 1,2715 г кристаллогидрата щавелевой кислоты, перенёс её количественно в мерную колбу объёмом 200 мл и довёл до метки дистиллированной водой? Перечислить посуду для приготовления раствора.
( Ответ: Сf=0,1009 моль/л )
12.Рассчитать навеску кристаллогидрата, необходимую для приготовления 250 мл раствора оксалата аммония с Т=0,006989 г/мл?
( Ответ: m=1,7473 г )
13.Сколько граммов оксалата натрия нужно взять для приготовления 250 мл раствора с молярной концентрацией эквивалента 0,1 моль/дм3?
( Ответ: m=1,6750 г )
14.Рассчитать молярную концентрацию эквивалента раствора оксалата аммония, если для его приготовления навеску 8,8528 г кристаллогидрата оксалата аммония растворили в воде в мерной колбе объёмом 500 мл? Написать алгоритм приготовления раствора.
( Ответ: Сf=0,2492 моль/л )
15.Рассчитать навеску, необходимую для приготовления 1000 мл раствора оксалата натрия с Т=0,003414 г/мл?
( Ответ: m=3,4140 г )
16.Сколько граммов кристаллогидрата оксалата аммония нужно взять для приготовления 500 мл раствора с молярной концентрацией эквивалента 0,25 моль/дм3?
( Ответ: m=8,8825 г )
17.Рассчитать молярную концентрацию эквивалента раствора, если для его приготовления лаборант взвесил навеску 3,3615 г оксалата натрия, перенёс её количественно в мерную колбу объёмом 1000 мл и довёл до метки дистиллированной водой? Перечислить посуду для приготовления раствора.
( Ответ: Сf=0,05018 моль/л )
18.Сколько граммов кристаллогидрата щавелевой кислоты нужно взять для приготовления 500 мл раствора с Т =0,006435 г/мл?
( Ответ: m=3,2175 г )
2.Приготовление рабочих растворов. |
Обучающие задачи |
