
Тверді тіла План
Кристалічні тіла
Аморфні тіла
Деформація.
Механічні властивості твердих тел.
Пластичність і крихкість
Плавлення і кристалізація
Полімери та рідкі кристали
Ключові поняття і терміни:
Твердий стан речовини
Кристал
Кристалічні гратки
Анізотропія кристалів
Кристалічна структура
Дефекти в кристалах
Деформації
Механічна напруга
Пружність
Пластичність
Крихкість
Твердість
Плавлення
Кристалізація
Питома теплота плавлення
Рівняння теплового балансу
Полімери
Рідкі кристали
1. Кристалічні тіла
Тверді тіла зберігають не тільки свій об'єм, як рідини, а й форму. Тверді тіла перебувають переважно в кристалічному стані.
Кристали — це тверді тіла, атоми й молекули яких займають певні, упоряджені положення в просторі. Результат цього — правильна зовнішня форма кристала. Наприклад, плоскі грані кристалика кухонної солі утворюють одна з однієї прямі кути. Це можна помітити, розглядаючи сіль через мікроскоп. А геометрично правильна форма сніжинки! Це також свідчить про геометричну правильність будови кристалічного тіла льоду.
Внутрішня будова кристалів. Залежність фізичних властивостей кристалів від напряму і правильність їхніх геометричних форм давали підстави для припущення про впорядкованість частинок, які утворюють кристал.
Частинки, з яких складається кристал, при тепловому русі коливаються навколо положень рівноваги, які називають вузлами.
Вузол – це положення рівноваги частинки, яка входить до складу кристала, тобто точка. Відстань між вузлами умовно позначає відстань між центрами атомів і молекул.
Розрізняють чотири типи кристалів (і кристалічних ґраток): іонні, атомні, металічні і молекулярні.
Іонні кристали. У вузлах ґраток іонних кристалів знаходяться позитивно і негативно заряджені іони. Сили взаємодії між ними в основному електростатичні. Іона кристалічна гратка надана на рис.1.
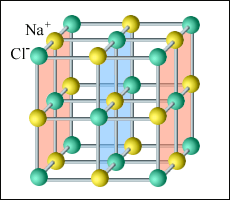
Рис.1. Іона кристалічна гратка кухонної солі
Атомні кристали. Їхні кристалічні гратки утворюються внаслідок щільної упаковки атомів, найчастіше однакових (під час взаємодії однакових атомів іони не утворюються. Атоми, що знаходяться у вузлах, зв’язані із своїми найближчими сусідами ковалентним зв’язком.
За умови ковалентного зв’язку електрони не переходять від одного атома до іншого (іони не утворюються), а виникає одна чи кілька спільних електронних пар.
Молекулярні кристали. У вузлах їх кристалічних граток знаходяться молекули речовини, зв’язок між якими забезпечується силами молекулярної взаємодії.
Металічні кристали. У всіх вузлах гратки металічних кристалів розміщені позитивні іони металу. Між ними хаотично, подібно до молекул газу, рухаються електрони, які відокремилися від атомів під час кристалізації металу. Разом з тим і електрони утримуються іонами в її межах. Наявність вільних електронів у металі забезпечує добру електропровідність і теплопровідність цих речовин.
Кожна частинка в кристалі (молекула, атом чи іон) знаходиться в певному положенні рівноваги, в якому сили відштовхування і притягання з боку інших частинок, які утворюють кристал, однакові. Різноманітні форми кристалічних ґраток розглянути на рис.2.
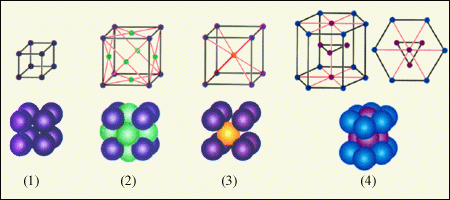
Рис.2. Форми кристалічних ґраток
Відхилення від ідеального порядку просторової (кристалічної) гратки називаються дефектами.
Монокристали й полікристали. Кристалічну структуру мають метали. Саме метали переважно використають тепер для виготовлення знарядь роботи, різних машин і механізмів.
Тверде тіло, що складається з великої кількості маленьких кристаликів, називають полікристалічним.
Одиночні кристали називають монокристалами.
Дотримуючись великої обережності, можна виростити кристал металу більших розмірів — монокристал. Звичайно виходить полікристалічне тіло, тому що одночасно росте багато кристалів.
До полікристалів належать не тільки метали. Наприклад, шматок цукру також має полікристалічну структуру.
