
- •Влияние температуры
- •Контактное окисление оксида серы (IV)
- •Производство метилового спирта
- •Принцип наилучшего использования энергии
- •Производство аммиака.
- •Выбор давления.
- •Технологическое оформление процесса синтеза аммиака.
- •Производство азотной кислоты
- •Сырье для производства азотной кислоты.
- •Выбор оптимальных условий проведения процесса.
- •Катализатор.
- •Температура.
- •Давление.
- •Соотношение исходных компонентов.
- •Конструкции контактных аппаратов.
- •Производство этанола
- •Элементарные стадии в гетерогенном катализе.
- •Производство азотной кислоты
- •Производство водорода.
- •Промышленные способы получения водорода.
- •Выбор температуры.
- •Выбор давления.
- •Вторая стадия конверсии метана.
- •Конверсия оксида углерода.
- •Очистка конвертированного газа.
- •Технологическое оформление конверсии природного газа.
- •Аппаратурное оформление процесса.
- •Принцип наилучшего использования сырья
- •Производство этилового спирта
- •Производство серной кислоты из серы
- •Получение серной кислоты.
- •1.Получение обжигового газа из серы.
- •2. Контактное окисление оксида серы (IV).
Элементарные стадии в гетерогенном катализе.
Все гетерогенно-каталитические реакции состоят из отдельных химических и физических элементарных стадий. Поскольку в процессе реакции исходные вещества должны достичь активных центров катализатора, а образующиеся продукты - выйти за пределы катализатора, то, помимо собственно химической реакции, необходимыми стадиями каталитического процесса являются процессы диффузии, адсорбции и десорбции.
Рассмотрим простейший случай газофазной реакции, протекающей на пористом катализаторе. Процесс включает в себя следующие стадии (Рис. 5.1):
-
Диффузия исходных веществ через приповерхностный слой к поверхности катализатора.
-
Диффузия исходных веществ в поры катализатора.
-
Адсорбция реагентов на внутренней поверхности катализатора.
-
Химическая реакция на поверхности катализатора.
-
Десорбция продуктов с поверхности катализатора.
-
Диффузия продуктов из пор катализатора.
-
Диффузия продуктов через приповерхностный слой в газовую фазу.
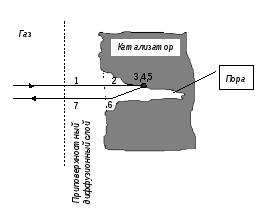
Рис. 5.1. Элементарные стадии гетерогенно-каталитической газофазной реакции.
------------------
В процессе эксплуатации любой катализатор подвергается дезактивации, зависящей от его химической, термической и механической стабильности. На стабильность катализатора оказывают влияние такие факторы как разрушение, закоксовываемость и отравление. Дезактивация может быть обратимой и необратимой. При обратимой дезактивации катализатору можно вернуть частично или полностью его каталитические свойства специальной обработкой (регенерация). С экономической точки зрения исключительно важным является общее время эксплуатации до полной замены катализатора, а также длительность циклов между регенерациями катализатора.
|
Производство азотной кислоты
Сырьем для получения азотной кислоты служат аммиак и воздух. Технологический процесс состоит из двух основных стадий: 1- окисление аммиака; 2- переработка нитрозных газов (абсорбция).
На первую стадию поступает смесь аммиака и воздуха (аммиачно-воздушная смесь – АВС), компоненты которой предварительно очищают и нагревают. В контактном аппарате протекает ряд реакций, из которых основными являются: 4NH3 + 5O2 4NO + 6Н2О, (1) 4NH3 + 3O2 2N2 + 6H2O. (2)
Реакция (1) является целевой, а (2) – побочной. Оксид азота (II) окисляется до оксида азота (IV): 2NO + O2 2NO2. (3) Полученные нитрозные газы направляют в абсорбционную колонну (стадия абсорбции), туда же подают воду и воздух. Химические процессы, протекающие в абсорбционной колонне, могут быть описаны следующим суммарным уравнением:
2NO + 1,5O2 + H2O = 2HNO3. (4)
Отходящие из колонны газы содержат небольшое количество оксидов азота и направляются на очистку в реактор каталитического восстановления. Процесс может быть описан суммарным уравнением: CH4 + 2NO = CO2 + N2 + 2H2O. (5)
В результате выхлопные газы состоят из азота, оксида углерода (IV), кислорода и паров воды. Суммарная реакция образования азотной кислоты выражается уравнением: NH3 + 2O2 → HNO3 + H2O (6)
|
|
Принцип наилучшего использования сырья Затраты на сырье являются одной из главных составляющих себестоимости химических продуктов. В среднем они составляют около 50 % себестоимости произведенных продуктов. Надо отметить, что многие виды сырья (руды, природный газ, нефть и др.) – невозобновляемы. Имеет место тенденция к истощению запасов сырьевых ресурсов, возникает необходимость в переработке бедных по содержанию ценных компонентов руд. Места добычи полезных ископаемых смещаются в труднодоступные районы. С экологической точки зрения, если сырье не превращается в целевые продукты, оно превращается в отходы, которые, так или иначе, попадают в окружающую среду. Существуют конкретные приемы, с помощью которых можно реализовать этот принцип.
|
