
- •Свойства растворов
- •Примеры решения задач с использованием концентрации растворов
- •Тогда в 1л 0,5н раствора содержится 26,5 г Na2co3
- •Контрольные вопросы и задачи Теоретические вопросы
- •Электролитическая диссоциация
- •Примеры решения типовых задач
- •Не распалось на ионы
- •Контрольные вопросы и задачи Теоретические вопросы
- •Домашние задания по теме «Растворы»
- •Домашние задания по теме «Электролитическая диссоциация»
Примеры решения типовых задач
Задача 1. Чему равна молярная концентрация частиц в растворе, содержащим 0,11 г CaCl2 в 200 мл раствора?
Решение.
CaCl2 Ca+2 + 2 Cl-
молярная концентрация CaCl2
CМ
=
![]() =
=![]() = 510-3
моль/л,
= 510-3
моль/л,
так как CaCl2 – соль (сильный электролит), а концентрация раствора мала, примем = 1 (100 %).
Тогда
[CaCl2]расп. на ионы = [CaCl2]общей = 510-3 моль/л;
[CaCl2]недис. = 0 моль/л.
Из уравнения электролитической диссоциации следует, что
[Ca+2] = [CaCl2]расп. на ионы = 510-3 моль/л;
[C1-] = 2[CaCl2]расп. на ионы =2510-3 = 10-2 моль/л.
Ответ. В растворе присутствуют ионы Ca+2 и C1-, молекулы CaCl2 – отсутствуют. [Ca+2] =510-3, [C1-] =10-2 моль/л.
Задача 2. Определить концентрации [Н+], [CН3СОО-] и [CН3СООН] в 0,1 M растворе CН3СООН, если =1,34 %.
Решение. CН3СООН Н+ + CН3СОО-]. Ионы CН3СОО- и Н+ образуются из молекул CН3СООН, участвующих в электролитической диссоциации. Из уравнения следует, что
[CН3СОО-] = [Н+]= [CН3СООН]расп. на ионы .
По определению = Срасп. на ионы / Cобщее кол-во, следовательно,
[CН3СОО-]
расп. на ионы
= [CН3СООН]общ.
= 0,1![]() =
1,34
10-3
моль/л, отсюда [Н+]=
[CН3СОО-]
= 1,34
10-3
моль/л.
=
1,34
10-3
моль/л, отсюда [Н+]=
[CН3СОО-]
= 1,34
10-3
моль/л.
Не распалось на ионы
[CН3СООН] = [CН3СООН]общ. - [CН3СОО-] расп. на ионы = С - С = С (1-) = 0,1(1-0,00134) = 0,099866 моль/л.
Ответ. [CН3СООН]недис. = 0,099866 моль/л;
[Н+]= [CН3СОО-] = 1,34 10-3 моль/л.
Задача
3.
Определить
[Н+]
и рН 1 10-2
M
растворе азотистой кислоты. Kдис.
![]() =
5,110-4.
=
5,110-4.
Решение.
HNO2 H+ + NO-2
[H+] = [HNO2]расп. неполн. = С (см. задачу 2).
По закону разведения Оствальда . Kдис. = СM 2, откуда
=
![]() =
=![]() =
2,310-1.
=
2,310-1.
[H+] = Собщ. = 2,310-110-2 =2,310-3 моль/л;
рН = -lg [H+] = -2,310-3 = 2,64.
Ответ. [H+] = 2,310-3 моль/л; pH = 2,64.
Задача 4. Чему равны [ОH-], [H+] и рН в 0,2 %-ном растворе NaOH? Плотность раствора равна 1 г/см3.
Решение.
Определим СM раствора NaOH.
Примем Vр-ра = 1л = 1000 см3,
mр-ра = V р-ра р-ра = 1000 1 = 1000 г,
mNaOH
= mр-ра
![]() = 1000
= 1000![]() = 2 г,
= 2 г,
СM
=
![]() =
=![]() =
0,05 моль/л.
=
0,05 моль/л.
NaOH Na+ + OH-, так как NaOH относится к сильным электролитам, то при СM = 0,05 моль/л примем = 1.
Следовательно, Срасп. на ионы = Собщ. = 0,05 моль/л;
[Na+] = [OH-] =[NaOH]расп. на ионы = 0,05 моль/л.
Из ионного произведения воды [Н+] [OH-] = 10-14
следует
[Н+]
=
![]() =
=
![]() = 210-13
моль/л.
= 210-13
моль/л.
4. Водородный показатель рН = -lg[Н+] = lg210-13 = 12,7.
Ответ. [ОH-] = 510-2 моль/л, [H+] = 210-13 моль/л и рН = 12,7.
Контрольные вопросы и задачи Теоретические вопросы
Какой процесс называется электролитической диссоциацией?
Какие вещества называются электролитами и неэлектролитами? Приведите примеры.
Какова роль сольватации (гидратации) в процессах растворения и электролитической диссоциации?
Что называется степенью электролитической диссоциации? Какие электролиты относятся к сильным, средним и слабым? Приведите примеры для различных классов неорганических соединений.
От каких факторов зависит степень электролитической диссоциации ? Влияние природы растворенного вещества и растворителя, концентрации растворенного вещества, температуры, наличия в растворе веществ, содержащих одноименные ионы, на степень диссоциации.
Что называется константой электролитической диссоциации? (Определение). От каких факторов зависит константа электролитической диссоциации?
Используя вывод закона разведения (разбавления) Оствальда, приведите взаимосвязь Kдис., и молярной концентрации. Для каких электролитов применим закон Оствальда?
Ступенчатая диссоциация кислот и оснований. Приведите примеры и напишите Kдис. Для каждой ступени. Сравните и Kдис. Для каждой из ступеней электролитической диссоциации.
К каким электролитам относят соли? Приведите примеры электролитической диссоциации для средних, кислых основных солей.
Приведите примеры (не менее 5) наиболее распространенных кислот и оснований. Какие из них относят к сильным электролитам, а какие - к слабым?
Какие электролиты относятся к сильным? Приведите примеры для каждого класса неорганических соединений. Состояние сильных электролитов в растворах. Понятие об активности и коэффициенте активности.
К каким электролитам относится вода? Напишите уравнение электролитической диссоциации воды. Константа диссоциации воды. Ионное произведение воды.
Каково соотношение концентраций ионов водорода и гидроксильных ионов в воде, растворах кислот и оснований?
Водородный показатель рН (определение) и его значения в нейтральных, кислых и щелочных растворах.
Задачи
Вычислите концентрацию гидроксид-иона и рН в 0,1 молярном растворе азотной кислоты.
Вычислите молярную концентрацию ионов водорода и рН в 0,01 молярном растворе гидроксида калия.
Водородный показатель раствора рН = 3. Определите молярную концентрацию иона водорода и гидроксид-иона в этом растворе.
Молярная концентрация гидроксид-иона равна 10-3 моль/л. Вычислите рН и концентрацию иона водорода в растворе.
Вычислите рН и концентрацию гидроксид-иона в 0,1%-ном растворе соляной кислоты. Степень электролитической диссоциации и плотность раствора считать равными единице.
Вычислите молярную концентрацию гидроксид-иона и рН в 0,01 нормальном растворе азотной кислоты.
Чему равна концентрация гидроксид-иона в растворе, рН которого равен 11?
Определите рН и концентрацию ионов водорода в растворе, в 1 литре которого содержится 0,4 грамма гидроксида натрия.
Определите концентрацию ионов водорода и рН в 10-3 молярном растворе гидроксида калия.
В одном литре раствора содержится 0,056 граммов гидроксида калия. Определите концентрацию ионов водорода и гидроксида-иона в этом растворе.
Степень диссоциации уксусной кислоты СН3СООН в 10-3 молярном растворе равна 10 %. Определите концентрацию ионов водорода и рН раствора.
Вычислите константу диссоциации и концентрацию ионов гидроксида в 210-3 молярном растворе гидроксида аммония NH4OH, если степень его диссоциации = 10 %.
Вычислите степень диссоциации, концентрацию ионов водорода и рН в 0,05 молярном растворе плавиковой кислоты. Константа диссоциации Kдис.HF равна 7,410-4.
Вычислите концентрацию ионов водорода, степень диссоциации и рН в 0,1 молярном растворе перекиси водорода Н2О2. Kдис.
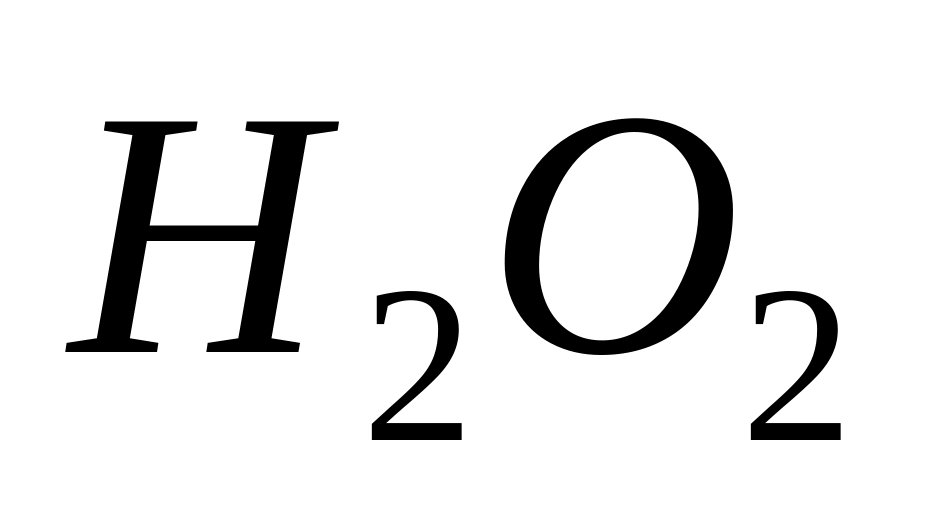 по
первой ступени равна 2,410-12.
по
первой ступени равна 2,410-12.Степень диссоциации сероводородной кислоты в 5 %-ном (по массе) растворе равна 3 %. Вычислите константу диссоциации сероводородной кислоты по первой ступени диссоциации. Плотность раствора принять равной 1 г/см3.
Вычислите степень диссоциации гидроксида аммония и концентрацию гидроксид-иона в 0,1 молярном растворе. Константа диссоциации Kдис.
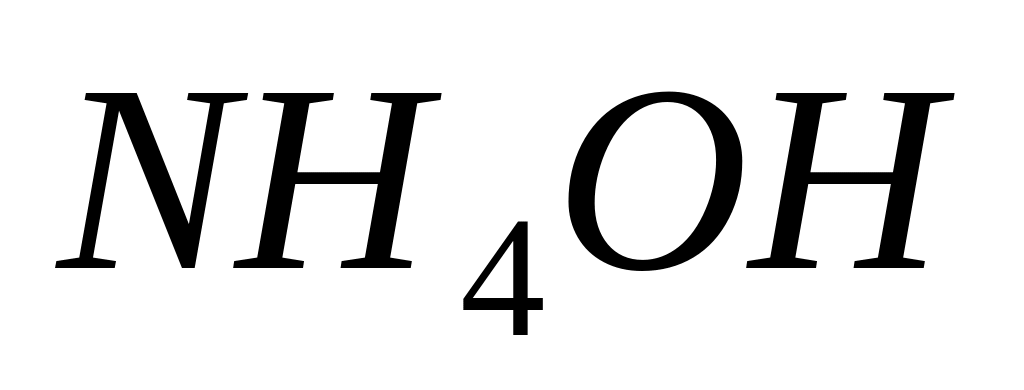 =
1,810-5.
=
1,810-5.Вычислите концентрацию ионов водорода и степень диссоциации уксусной кислоты в 1%-ном растворе. Плотность раствора принять равной 1 г/см3. Константа диссоциации Kдис.
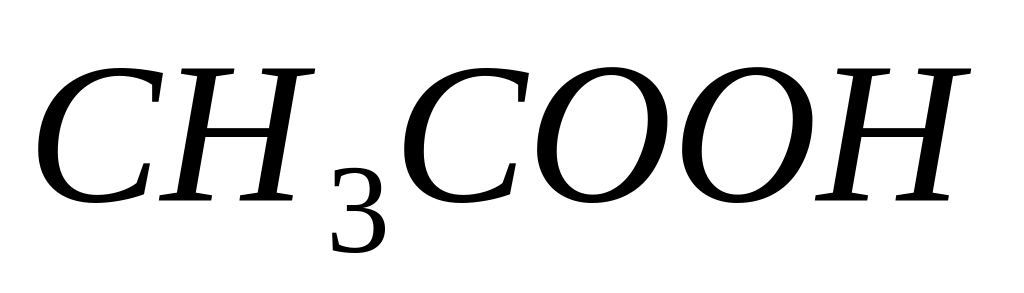 =
1,810-5.
=
1,810-5.Вычислите молярную концентрацию раствора плавиковой кислоты, если степень диссоциации равна 8 %. Константа диссоциации Kдис. НF =7,410-4.
Вычислите концентрацию ионов водорода, степень диссоциации и рН раствора угольной кислоты с массовой долей 3 %. Плотность раствора принять равной 1 г/см3. Константа диссоциации угольной кислоты по первой ступени Kдис.
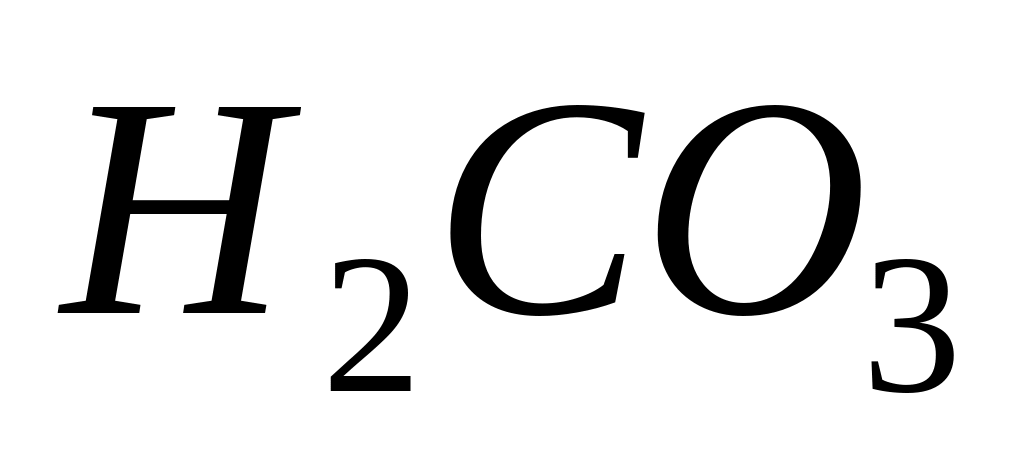 =
3,510-5.
=
3,510-5.Вычислите степень диссоциации и рН раствора сероводородной кислоты с массовой долей 3 %. Плотность раствора принять равной 1 г/см3. Константа диссоциации по первой ступени Kдис.
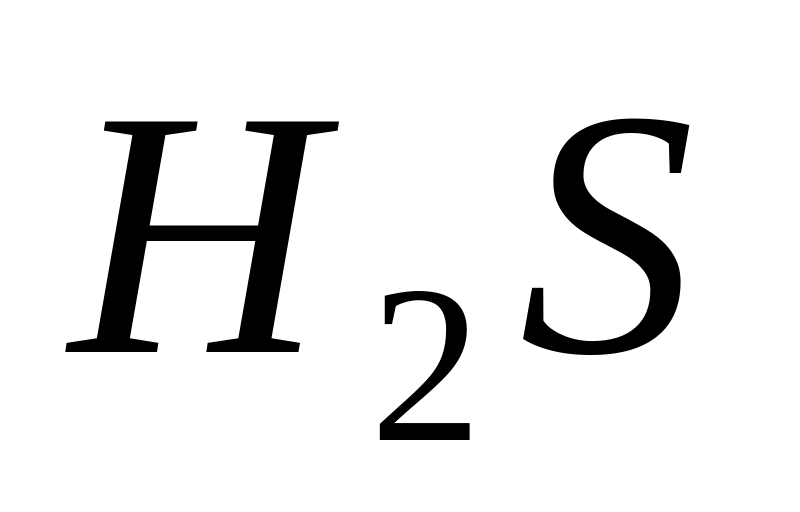 =
1,0210-7.
=
1,0210-7.
