
- •Модуль I
- •Классификация спиртов
- •Гомологический ряд одноатомных спиртов.
- •Радикало-функциональная и заместительная номенклатуры спиртов.
- •Изомерия спиртов.
- •Строение спиртов.
- •Химические свойства
- •Многоатомные спирты
- •Физические свойства спиртов.
- •Классификация фенолов.
- •Номенклатура и изомерия.
- •Строение фенола, взаимное влияние бензольного кольца и гидроксильной группы.
- •Физические свойства.
- •Химические свойства.
- •Фенол. Резорцин. Адреналин. Применение в медицине. Трехатомные фенолы.
- •По характеру углеводородного радикала различают:
- •Строение молекулы амина
- •Диамины.
- •Аминоспирты
- •Вопросы для самоконтроля:
- •Упражнения
- •Лабораторная работа
Фенол. Резорцин. Адреналин. Применение в медицине. Трехатомные фенолы.
Фенол и его производные обладают дезинфицирующим свойством.. Карболовая к-та – 3%-ный раствор фенола – для дезинфекции хирургических инструментов. В промышленности фенол используют для получения фенолоформальдегидных смол и ряда красителей.
Резорцин – используется при лечении кожных заболеваний в составе примочек или мазей.
Гидрохинон – в организме восстановительная способность замещенного гидрохинонового фрагмента делает его участником важного процесса транспоста электронов от окисляемого субстрата к кислороду.
Пирокатехин применяется для синтеза адреналина – гормона надпочечников. Адреналин является одним из важнейших регуляторов жизнедеятельности организма. Это первый гормон, который удалось получить синтетически.
Амины - Это производные аммиака NH3, где один, два или три атома Н замещены на радикал R (алифатический или ароматический).
Классификация
По количеству NH2 групп различают: моноамины, диамины:
СН3СН2NH2 NH2 – CH2 – CH2 – NH2
Этиламин Этилендиамин
В зависимости от числа атомов Н, замещенных на R, различают первичные, вторичные и третичные амины. NH2 – аминогруппа, –NH – иминогруппа.
СН3СН2NH2 – этиамин, первичный амин
СН3СН2NH - СН3СН3 – диэтиламин, вторичный амин
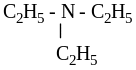 -
триэтиламин, третичный амин
-
триэтиламин, третичный амин
По характеру углеводородного радикала различают:
алифатические СН3-СН2-NH2 - этиламин
ароматические С6Н5NH2 – аминобензол, анилин
Номенклатура
Рациональная – название радикала (R) + «амин»:
СН3 – СН2– СН2– NН2 СН3 – NН– СН3
Пропиламин Диметиламин
МН рассматривает гр. –NH2 как заместитель в первичных аминах и ее название ставят в приставке перед названием основной цепи (корня):
![]() 2-Аминопропан
2-Аминопропан
Изомерия
Для первичных аминов – изомерия углерод-углеродной цепи и положения гр. – NH2 (1, 2); для вторичных и третичных аминов – изомерия радикала - метамерия
СН3 – СН2– СН2– NН2
Пропиламин Изопропиламин
СН3 – СН2– СН2– СН2– NН2
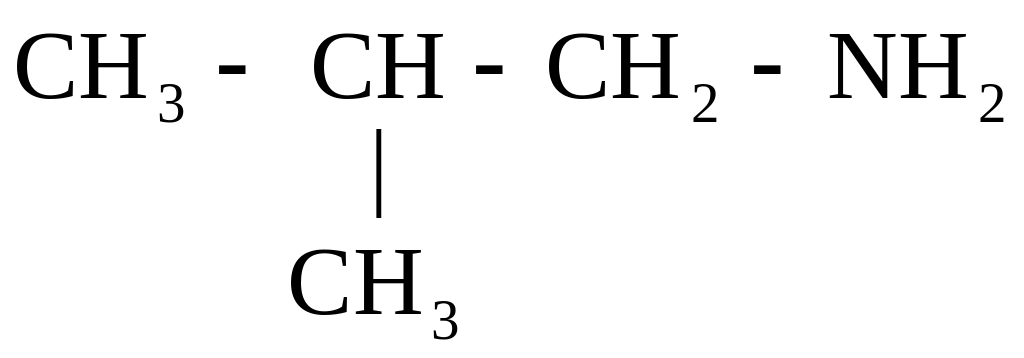
Бутиламин Изобутиламин
СН3 – СН2– СН2–NН–СН3 СН3 – СН2–NН – СН2–СН3
Метилпропиламин Диэтиламин
Физические свойства
Метиламин, диметиламин, триметиламин – газы, хорошо растворимые в воде; средние члены гомологического ряда аминов – жидкости, высшие – твердые вещ-ва.
Амины в заметных количествах образуются при гниении органических остатков, содержащих белки. Ряд аминов образуется в организме человека и животных из -аминокислот под действием ферментов. Такие амины принято называть биогенными аминами, например, кадаверин и путресцин.
Строение молекулы амина
Связи N – H, C – N полярны, однако полярность NH связи больше, чем CN согласно различной ЭО атомов N, С, Н. Поэтому первичные и вторичные амины, подобно спиртам, склонны к образованию Н-связей.
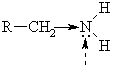
Нуклеофильный и оснóвный центры
В связи с меньшей полярностью связи С – N (0,45 D) по сравнению с полярностью N – Н (1,3 D) для аминов не характерны реакции замещения гр. NН2 – и кислотные свойства.
Важнейшее свойство аминов связано с наличием свободной электронной пары у атома N и его способностью присоединять «+» частицы. С этим связано проявление аминами свойств оснований, т.е. присоединять Н+ от воды и кислот, а также вступать в р-ции алкилирования, ацилирования, выполняя при этом роль Nu.
Химические свойства
I. Оснóвные свойства
Амины более сильные основания, чем NH3. Это объясняется + I эффектом радикалов. Чем больше электронная плотность на атоме N, тем больше основность. Вторичные амины более сильные основания, чем первичные. Основность третичных аминов уменьшается, что объясняется экранирующим влиянием атома N тремя алкильными группами.
Поскольку электроотрицательность атома N меньше электроотрицательности атома О, амины образуют менее прочные ассоциаты, чем соответствующие спирты и имеют более низкие температуры кипения. Температура кипения этанола 78 оС, а этиламина – 17 оС.
При растворении в воде к аминам присоединяется Н+ от молекулы НОН, поэтому растворы аминов имеют щелочную реакцию:
С2Н5![]() H2
+ HOH
[С2Н5
H2
+ HOH
[С2Н5![]() H3]OH
H3]OH
Гидроксидэтиламмония
При взаимодействии с кислотами образуются соли:
С2Н5 H2 + HС1 [С2Н5 H3]Сl
Хлоридэтиламмония
Щелочи разлагают соли аминов и выделяют свободные амины:
[С2Н5 H3]Сl + NaOH NaCl + С2Н5NH2 + H2O
Особенно сильные оснóвные свойства у чертвертичных аммониевых оснований, которые по силе соответствуют щелочам:
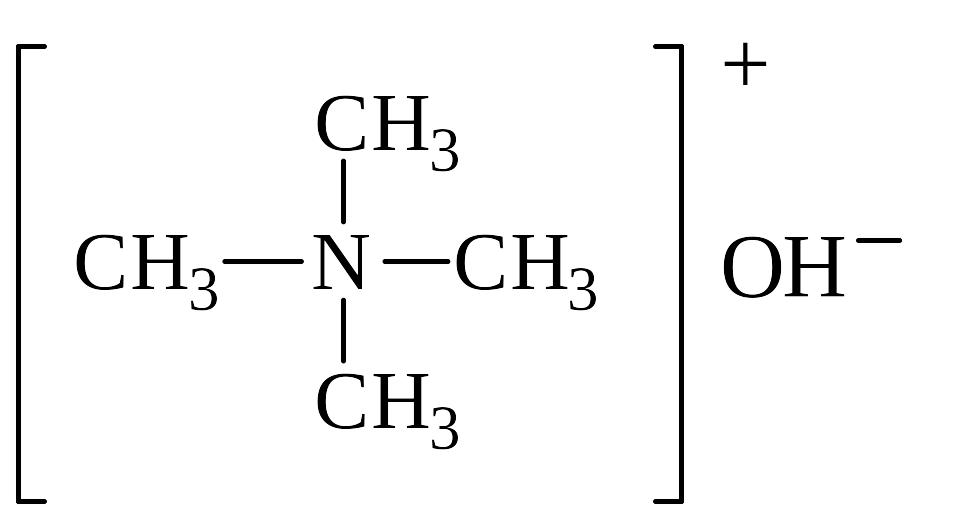
Оснóвные свойства ароматических аминов ослаблены за счет р,-сопряжения NH2 – группы с бензольным кольцом. Поэтому анилин образует соли только с сильными минеральными к-тами. Водный р-р анилина не изменяет окраску индикаторов.
II. Реакции алкилирования и ацилирования
В этом случае амины проявляют нуклеофильные свойства за счет электронной пары атома азота.
Реакция алкилирования (замещение атомов водорода в гр. NH2 на углеводородный радикал, в результате чего образуется вторичный амин):
С2Н5NH2 + СН3CI → С2Н5NH-CH3 + HCI
метилэтиламин
Реакция ацилирования (замещение атомов водорода в гр. NH2 на ацильный радикал):
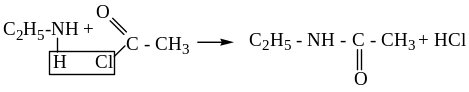
Подобным образом алкилируется и ацилируется С6Н5NH2.
С6Н5NH2 + СН3CI → С6Н5NH-CH3 + HCI (реакция алкилирования)
С6Н5NH2 + СН3 COCI → С2Н5NH-C-CH3 + HCI (реакция ацилирования)
║
О
III. Реакция с альдегидом с образованием основания Шиффа:
С2Н5
– NH2
+ O =
![]() – СН3
– СН3
![]() С2Н5
– N =
– СН3
С2Н5
– N =
– СН3
IV. Качественные реакции на амины (реакция с HNO2)
С2Н5 – NH2 + O = N – OH
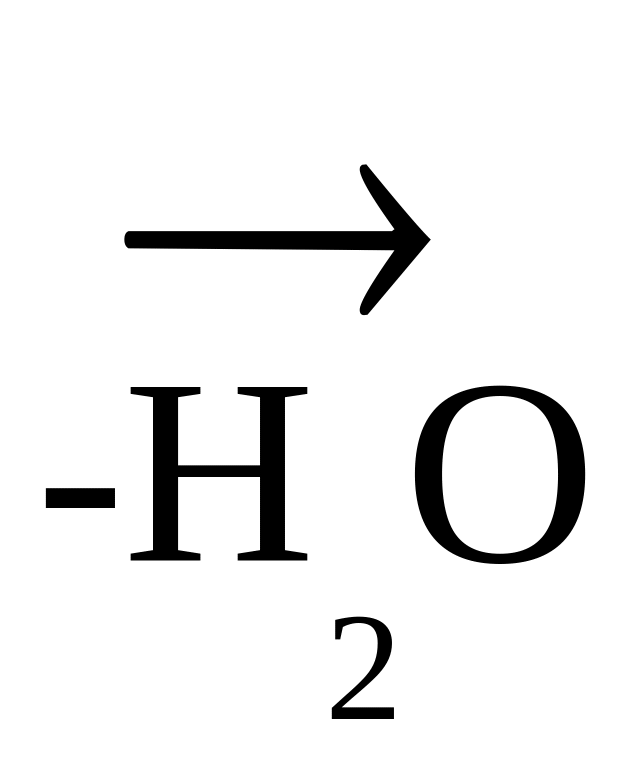 [С2Н5
– N= N – OH]
[С2Н5
– N= N – OH]
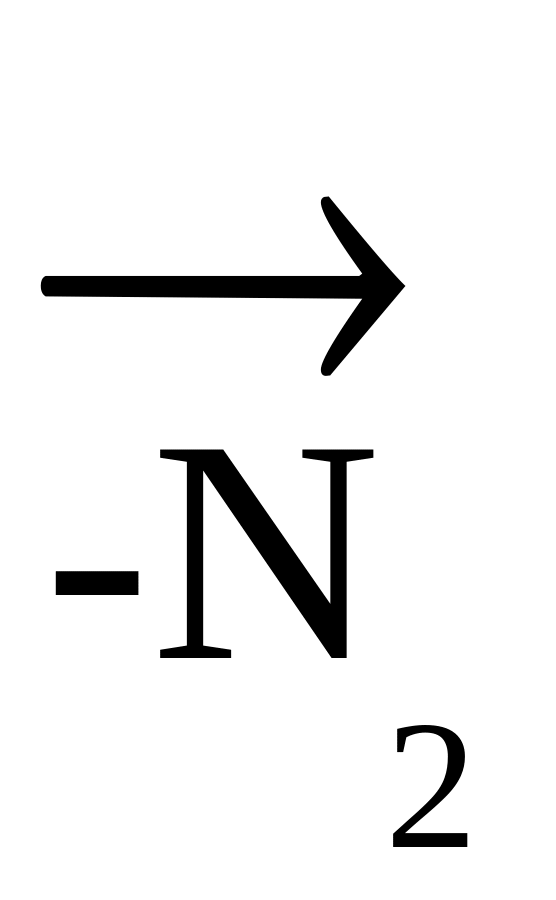 С2Н5OH
С2Н5OH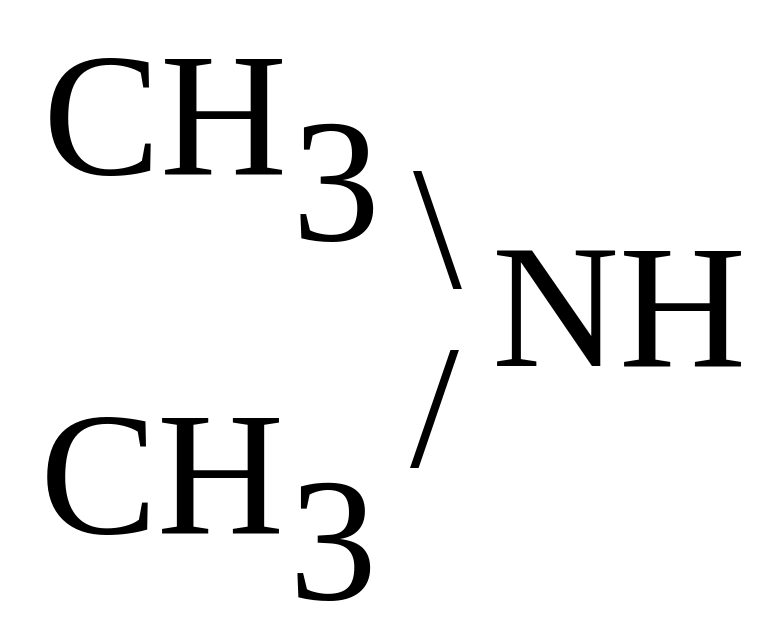 +
HONO
+
HONO
 -NO
-NO
Желтый
Нитрозоамины
Нитрозоамины являются канцерогенными веществами. Нитраты в организме восстанавливаются до нитритов.
R3N: + НNO2 [R3NH]+NO2
Соль
При действии HNO2 на соли анилина образуется не фенол, а соли диазония (широко используемые в химии красителей), которые при нагревании выделяют азот N2 с образованием фенола:
[С6Н5 H3]Cl + HONO [С6Н5 N]Cl + 2Н2О
Соль диазония
[С6Н5
N]Cl
+ 2Н2О
![]() N2
+ HCl + С6Н5OH
N2
+ HCl + С6Н5OH
Реакции по радикалу
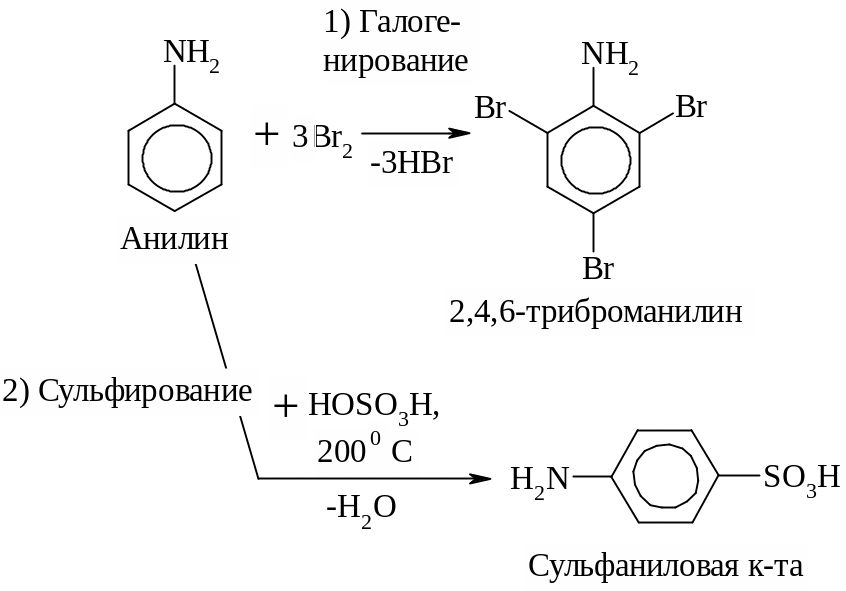
Сульфаниловая кислота – важный продукт в синтезе лекарственных веществ (сульфаниламидных препаратов) и красителей. Наибольшую активность имеют производные сульфаниламидов, в которых атом Н в группе – SO2NH2 замещен на гетероцикл. Например, сульфадиметоксин:
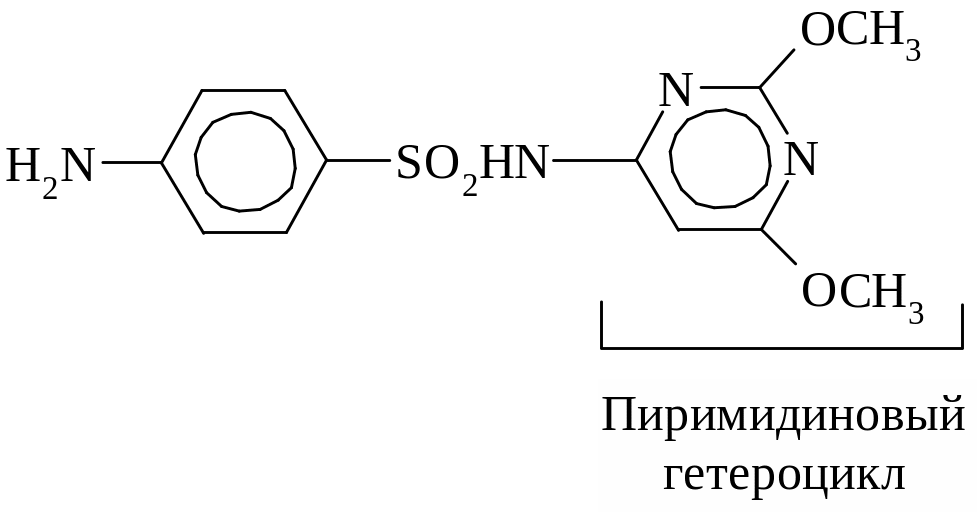
Сульфаниламиды, являясь антиметаболитами n-аминобензойной к-ты (ПАБК), блокируют биосинтез фолиевой к-ты (витамин Вс), необходимой для нормального развития и размножения микроорганизмов. Сульфаниламиды имеют сходные геометрические параметры с ПАБК, что позволяет им встраиваться вместо последней в синтез фолиевой к-ты.
