- •1. Основи термодинаміки. Однокомпонентні системи.
- •Робота № 1/1. Визначення теплоємності речовин.
- •Робота № 1/2. Визначення тиску насиченої пари індивідуальної рідини динамічним методом
- •2. Гомогенні багатокомпонентні системи. Розчини
- •Робота № 2/1. Визначення молекулярної маси розчиненої речовини кріоскопічним методом
- •Робота № 2/2. Визначення парціальних мольних об'ємів
- •Робота № 2/3. Визначення коефіцієнта розподілу оцтової кислоти між водною та органічною фазами
- •Робота № 2/4. Визначення активностей йоду методом розподілу
- •Робота № 2/5. Визначення термодинамічної активності компонентів розчину кріоскопічним методом
- •3. Фазові рівноваги в багатокомпонентних системах
- •Робота № 3/1. Дослідження рівноваги рідина - рідина в двокомпонентній системі з обмеженою розчинністю рідин
- •Робота № 3/2. Вивчення рівноваги рідина - пара у двокомпонентних системах з необмеженою розчинністю компонентів у рідкому стані
- •Робота № 3/3. Вивчення кристалізації бінарних сумішей
- •Робота № 3/4. Дослідження рівноваги рідина - рідина в трикомпонентній системі з однією областю розшарування
- •4. Хімічна рівновага та термохімія
- •Робота № 4/1. Визначення теплоти гідратації СиSо4
- •Робота № 4/2. Визначення теплоти нейтралізації калориметричним методом
- •Робота № 4/3. Визначення теплоти реакції окиснення.
- •Робота № 4/4. Дослідження рівноваги хімічної реакції.
- •Робота № 4/5. Дослідження хімічної рівноваги в реакції термічного розкладу карбонату кальцію
- •Робота № 4/6. Дослідження рівноваги хімічної реакції у рідкій фазі
- •5. Статистична термодинаміка
- •Завдання № 5/1. Виведення формул зв'язку між сумами за станами та основними термодинамічними функціями ідеального газу
- •Завдання № 5/2. Розрахунок молекулярної суми за станами q
- •Завдання № 5/3. Розрахунок термодинамічних функцій ідеального газу статистичним методом
- •Завдання № 5/4. Розрахунок констант хімічної рівноваги статистичним методом
- •6. Основи хімічної кінетики
- •Робота № 6/1. Визначення константи швидкості оксидації водного розчину органічної речовини пероксидом водню
- •Робота № 6/2. Вивчення кінетики інверсії цукру
- •7. Кінетика реакцій в гомогенних системах
- •Робота № 7/1. Визначити константу швидкості реакції гідратації оцтового ангідриду
- •Робота № 7/2. Вивчення швидкості реакції йодування ацетону
- •Робота № 7/3. Встановлення кінетичних параметрів реакції мутаротації глюкози
- •8. Фізико-хімія поверхневих явищ
- •Робота № 8/1. Визначення питомої поверхні твердого тіла за адсорбцією з розчину
- •9. Каталіз
- •Робота № 9/1. Дослідження швидкості реакції розкладу пероксиду водню
- •Робота № 9/2. Вивчення кінетики омилення складних ефірів у присутності іонів гідроксилу
- •Робота № 9/3. Вивчення кінетики омилення складних ефірів у присутності іонів водню
- •10. Електрохімія. Електроліти
- •Робота № 10/1. Визначення ступеня та константи дисоціації слабкого електроліту методом вимірювання електропровідності розчинів.
- •Робота № 10/2. Визначення розчинності та добутку розчинності важкорозчинної солі методом вимірювання електропровідності
- •Робота № 10/3. Визначення чисел переносу іонів у розчинах електролітів
- •11. Термодинаміка та кінетика електрохімічних процесів
- •Робота № 11/1. Визначення електрорушійних сил (ерс) гальванічних елементів і електродних потенціалів
- •Робота № 11/2. Електрорушійні сили концентраційних елементів
- •Робота № 11/3. Визначення стандартного окисно-відновного потенціалу
- •Робота № 11/4. Визначення коефіцієнта активності електроліту методом вимірювання ерс
- •Робота № 11/5. Визначення термодинамічних характеристик реакцій в гальванічних елементах
- •Робота № 11/6. Напруга розкладу електролітів
- •Робота № 11/7. Зарядка та розрядка акумуляторів
- •Робота № 11/8. Визначення рН розчинів та потенціометричне титрування.
- •Список літератури
Робота № 11/4. Визначення коефіцієнта активності електроліту методом вимірювання ерс
Мета роботи. Визначити середній коефіцієнт активності хлористого водню в розчинах соляної кислоти різної концентрації.
Методика роботи. Активність іона - це "ефективна" концентрація, яку використовують замість справжньої концентрації в термодинамічних рівняннях, виведених для ідеальних розчинів. Коефіцієнт активності іона - це відношення активності іона до його концентрації
![]() .
(1)
.
(1)
Виміряти активність (або коефіцієнт активності) окремого виду іонів неможливо, тому на практиці використовують середні коефіцієнти активності γ±, які виражаються через активності окремих іонів рівнянням
![]() ,
(2)
,
(2)
де νi - кількість іонів даного виду в молекулі електроліту. Щодо хлориду водню вказані рівняння мають вигляд:
![]() ;
;
![]() ;
;
![]() ;
(3)
;
(3)
![]() .
.
Найточніше середній коефіцієнт активності вимірюють методом ЕРС. Оскільки електрорушійна сила являє собою різницю двох електродних потенціалів, то при вимірюванні γ± треба один із електродів вибрати таким, щоб він був оберненим відносно аніона електроліту, активність якого вимірюється, а другий - оберненим відносно катіона цього електроліту. Треба також, щоб у побудованого з вибраних електродів гальванічного елемента не було переносу іонів, тобто щоб в ньому не виникали дифузійні потенціали.
При вимірюванні γ± хлориду водню один із електродів повинен бути оберненим відносно іона хлору (хлорсрібний, каломельний), другий - іонів водню (водневий, хінгідронний, скляний). Залежність потенціалів цих електродів від активності іонів виражається рівняннями Нернста:
 (4)
(4)
Електрорушійна сила гальванічного елемента, побудованого з водневого електроду і хлорсрібного або каломельного (з урахуванням (3)) дорівнює:
 (5)
(5)
Абсолютні
значення активностей залежать від
вибору стандартного стану розчиненої
речовини. Для електролітів стандартний
стан обирається відповідно до вимоги,
щоб активність і концентрація збігалися
в безмежно розведеному розчині. У цьому
разі
![]() ,
якщо
,
якщо
![]() .
Тоді з рівняння (5) випливає:
.
Тоді з рівняння (5) випливає:
![]() .
(6)
.
(6)
Порядок роботи. Готують розчини соляної кислоти концентрації 0,1; 0,05; 0,01; 0,005; 0,001 і 0,0005 моль/л. По черзі, використовуючи кожен із цих розчинів, складають гальванічні елементи із електродів, обернених відносно іонів хлору і водню, наприклад: (Pt) H2 | HCl | AgCl, Ag.
ЕРС
елемента вимірюють за допомогою
потенціометра, з одержаних результатів
розраховують величини Е + (2RT/F) ln m. Будують
залежність в координатах [Е + (2RТ/F)ln m] -
m (рис. 1). Згідно з рівнянням (6) за
![]()
![]() .
.
|
Рис. 1. Графічна залежність, що ілюструє визначення величини Е° |
Отже,
екстраполяцією на
![]() знаходять Е°. Після цього, використовуючи
рівняння (5), розраховують середній
коефіцієнт активності і середню
активність:
знаходять Е°. Після цього, використовуючи
рівняння (5), розраховують середній
коефіцієнт активності і середню
активність:
 (7)
(7)
У хінгідронного електрода потенціал є більш додатним, ніж у хлорсрібного або каломельного, тому, коли замість водневого електроду використовують хінгідронний, електрорушійна сила виражається рівняннями:
 (8)
(8)
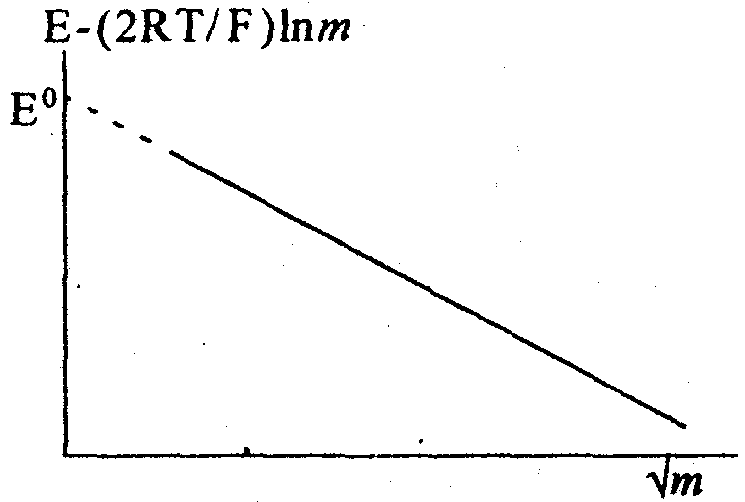
Ці рівняння відрізняються від рівняння (5) знаками перед доданками, що містять т і γ±. Тому при обробці результатів експерименту слід розраховувати величини Е - (2RТ/F) ln m і будувати графік, показаний на рис. 2.
|
Рис. 2. Графічна залежність, що ілюструє визначення величини E0 |
Як і у випадку з водневим електродом, E° знаходять екстраполяцією на , а середню активність і коефіцієнт активності (відповідно до рівняння (8)) обчислюють за формулами
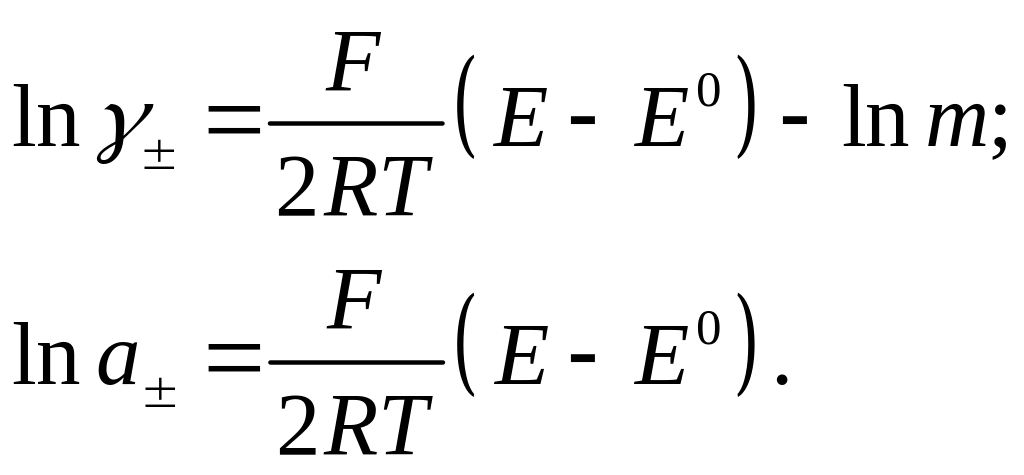 (9)
(9)
Результати вимірювань заносять у таблицю:
mHCl |
E |
E ± (2RT/F) ln m |
γ± |
a± |
|
|
|
|
|
Література: [21, с. 128-147, 171-173; 23, с. 262-277, 293-299, 301-303; 24, с. 298-302, 309-312; 25, с. 283-297, 314; 26, с. 130, 133, 135].