
- •1. Основи термодинаміки. Однокомпонентні системи.
- •Робота № 1/1. Визначення теплоємності речовин.
- •Робота № 1/2. Визначення тиску насиченої пари індивідуальної рідини динамічним методом
- •2. Гомогенні багатокомпонентні системи. Розчини
- •Робота № 2/1. Визначення молекулярної маси розчиненої речовини кріоскопічним методом
- •Робота № 2/2. Визначення парціальних мольних об'ємів
- •Робота № 2/3. Визначення коефіцієнта розподілу оцтової кислоти між водною та органічною фазами
- •Робота № 2/4. Визначення активностей йоду методом розподілу
- •Робота № 2/5. Визначення термодинамічної активності компонентів розчину кріоскопічним методом
- •3. Фазові рівноваги в багатокомпонентних системах
- •Робота № 3/1. Дослідження рівноваги рідина - рідина в двокомпонентній системі з обмеженою розчинністю рідин
- •Робота № 3/2. Вивчення рівноваги рідина - пара у двокомпонентних системах з необмеженою розчинністю компонентів у рідкому стані
- •Робота № 3/3. Вивчення кристалізації бінарних сумішей
- •Робота № 3/4. Дослідження рівноваги рідина - рідина в трикомпонентній системі з однією областю розшарування
- •4. Хімічна рівновага та термохімія
- •Робота № 4/1. Визначення теплоти гідратації СиSо4
- •Робота № 4/2. Визначення теплоти нейтралізації калориметричним методом
- •Робота № 4/3. Визначення теплоти реакції окиснення.
- •Робота № 4/4. Дослідження рівноваги хімічної реакції.
- •Робота № 4/5. Дослідження хімічної рівноваги в реакції термічного розкладу карбонату кальцію
- •Робота № 4/6. Дослідження рівноваги хімічної реакції у рідкій фазі
- •5. Статистична термодинаміка
- •Завдання № 5/1. Виведення формул зв'язку між сумами за станами та основними термодинамічними функціями ідеального газу
- •Завдання № 5/2. Розрахунок молекулярної суми за станами q
- •Завдання № 5/3. Розрахунок термодинамічних функцій ідеального газу статистичним методом
- •Завдання № 5/4. Розрахунок констант хімічної рівноваги статистичним методом
- •6. Основи хімічної кінетики
- •Робота № 6/1. Визначення константи швидкості оксидації водного розчину органічної речовини пероксидом водню
- •Робота № 6/2. Вивчення кінетики інверсії цукру
- •7. Кінетика реакцій в гомогенних системах
- •Робота № 7/1. Визначити константу швидкості реакції гідратації оцтового ангідриду
- •Робота № 7/2. Вивчення швидкості реакції йодування ацетону
- •Робота № 7/3. Встановлення кінетичних параметрів реакції мутаротації глюкози
- •8. Фізико-хімія поверхневих явищ
- •Робота № 8/1. Визначення питомої поверхні твердого тіла за адсорбцією з розчину
- •9. Каталіз
- •Робота № 9/1. Дослідження швидкості реакції розкладу пероксиду водню
- •Робота № 9/2. Вивчення кінетики омилення складних ефірів у присутності іонів гідроксилу
- •Робота № 9/3. Вивчення кінетики омилення складних ефірів у присутності іонів водню
- •10. Електрохімія. Електроліти
- •Робота № 10/1. Визначення ступеня та константи дисоціації слабкого електроліту методом вимірювання електропровідності розчинів.
- •Робота № 10/2. Визначення розчинності та добутку розчинності важкорозчинної солі методом вимірювання електропровідності
- •Робота № 10/3. Визначення чисел переносу іонів у розчинах електролітів
- •11. Термодинаміка та кінетика електрохімічних процесів
- •Робота № 11/1. Визначення електрорушійних сил (ерс) гальванічних елементів і електродних потенціалів
- •Робота № 11/2. Електрорушійні сили концентраційних елементів
- •Робота № 11/3. Визначення стандартного окисно-відновного потенціалу
- •Робота № 11/4. Визначення коефіцієнта активності електроліту методом вимірювання ерс
- •Робота № 11/5. Визначення термодинамічних характеристик реакцій в гальванічних елементах
- •Робота № 11/6. Напруга розкладу електролітів
- •Робота № 11/7. Зарядка та розрядка акумуляторів
- •Робота № 11/8. Визначення рН розчинів та потенціометричне титрування.
- •Список літератури
Робота № 7/3. Встановлення кінетичних параметрів реакції мутаротації глюкози
Мета роботи. Визначити константу швидкості реакції мутаротації глюкози та встановити її залежність від рН розчину.
Методика роботи. Кристалічні форми - та -глюкози є достатньо стійкими, але у розчині кожна з них повільно перетворюється на рівноважну суміш обох форм. За цим процесом легко спостерігати, визначаючи зменшення кута оптичного обертання -мономера (+112°) чи збільшення кута оптичного обертання -мономера (+18,7°) до рівноважного значення, яке становить 52,5°. Це явище відоме під назвою мутаротації. Мутаротація каталізується як кислотами, так і лугами (див. схему).
У рівноважній суміші знаходиться 64% -глюкози та 36% -глюкози.
Реакція
мутаротації - оборотна реакція 1-го
порядку. Для оборотних реакцій 1-го
порядку
![]() швидкість зміни концентрації речовини
А визначається за рівнянням:
швидкість зміни концентрації речовини
А визначається за рівнянням:
![]() (1)
(1)
де k1 та k2 - константи швидкості зменшення та збільшення концентрації речовини А. Інтегруючи це рівняння за умови, що початкові концентрації речовин А та В дорівнюють А0 та В0 відповідно, можна дійти до співвідношення:
![]() ,
(2)
,
(2)
де
![]() (3)
(3)
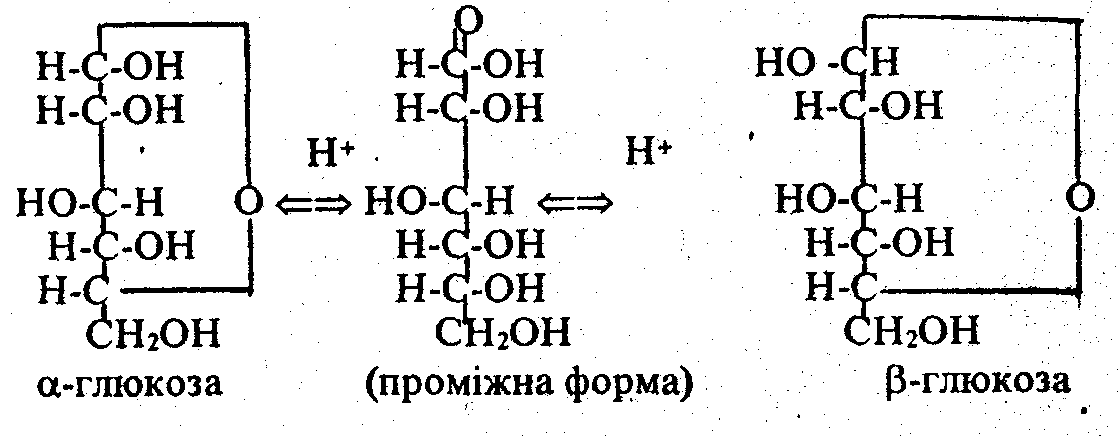
Якщо відоме значення величини xрівн, що показує наскільки зменшується концентрація речовини А від початкової (А0) до рівноважної (Арівн), то замість рівнянь (3) та (2) більш зручно користуватися рівняннями:
![]() (4)
(4)
та
![]() ,
(5)
,
(5)
які можна одержати за умови, що для константи рівноваги Кр виконується співвідношення:
![]() .
(6)
.
(6)
Коли за реакцією слідкують за допомогою поляриметра, рівняння (5) перетворюється на рівняння
![]() ,
(7)
,
(7)
де 0 та - кути оптичного обертання площини поляризації на початку реакції та при повному її завершенні; - поточне значення кута оптичного обертання площини поляризації у момент часу .
Порядок роботи. Реакцію досліджують за допомогою поляриметра. Сумарну константу швидкості знаходять за відсутності каталізатора та у його присутності.
Зважують дві наважки кристалічної глюкози, кожну по 5 г. Одну з них вносять у мірну колбу на 50 мл. Колбу швидко заповнюють водою. Колбу декілька разів струшують до повного розчинення глюкози. Розчин відфільтровують та зливають у поляриметричну трубку. З цього моменту починають заносити значення часу та відповідних кутів оптичного обертання площини поляризації до табл. 1.
Дослід повторюють у присутності НСl, концентрацію розчину якої вказує викладач (значення часу та відповідних кутів занести до табл. 2).
Сумарну константу швидкості знаходять для кожної пари значень та за рівнянням (7) або з тангенса кута нахилу залежності ln( - ) від за рівнянням
![]() .
(8)
.
(8)
Одержані за різних рН значення сумарної константи дозволяють знайти коефіціенти рівняння:
![]() .
(9)
.
(9)
Таблиця 1
Мутаротація за відсутності каталізатора. СН+ = 10-7 моль/л |
|||
|
|
- |
|
|
|
|
|
Kсер = ...
Таблиця 2
Мутаротація у присутності каталізатора. СН+ = ..... моль/л |
|||
|
|
- |
|
|
|
|
|
Kсер = ...
Література: [25, с. 195-208,210; 24, с. 322-354, 360; 22, с. 319-345].
