- •Ответы на билеты по химии
- •1. Периодический закон и периодическая система химических элементов д. И. Менделеева на основе представлений о строении атомов. Значение периодического закона для развития науки.
- •2. Предельные углеводороды
- •Строение молекулы метана
- •Разложение
- •Билет №2
- •2. Непредельные углеводороды ряда этилена (алкены)
- •1. Строение алкенов
- •Физические и химические свойства :
- •Отдельные представители
- •Билет №3.
- •1. Виды химической связи и способы ее образования в неорганических соединениях: ковалентная (полярная, неполярная, простые и кратные связи), ионная, водородная.
- •Химические свойства
- •1. Классификация химических реакций
- •2. Крахмал, целлюлоза
- •Билет 5.
- •1. Обратимость химических реакций, химическое равновесие
- •2. Ацетилен…
- •1. Скорость химических реакций
- •Катализ и катализаторы
- •2. Ароматические углеводороды (арены)
- •1. Основные положения теории химического строения а.М. Бутлерова
- •1. Изомерия органических соединений и ее виды.
- •2. Классификация оксидов
- •1. Металлы, их положение в периодической системе химических элементов д. И. Менделеева, строение их атомов, металлическая связь. Общие химические свойства металлов.
- •2. Фенол…
- •2. Предельные одноатомные спирты
- •2. Жиры, их состав и свойства. Жиры в природе, превращение жиров в организме. Продукты технической переработки жиров, понятие о синтетических моющих средствах.
- •1. Кислоты, их классификация и химические свойства на основе представлений об электролитической диссоциации. Особенности свойств концентрированной серной кислоты на примере взаимодействия с медью.
- •2. Общая характеристика высокомолекулярных соединений: состав, строение, реакции, лежащие в основе их получения (на примере полиэтилена или синтетического каучука).
- •1. Основания, их классификация и химические свойства на основе представлений об электролитической диссоциации.
- •2. Глюкоза — представитель моносахаридов, химическое строение, физические и химические свойства, применение.
- •1. Средние соли, их состав, названия, химические свойства (взаимодействие с металлами, кислотами, щелочами, друг с другом с учетом особенностей реакций окисления-восстановления и ионного обмена).
- •2. Взаимное влияние атомов в молекулах органических веществ на примере этанола и фенола.
- •Алюминий…
- •2. Анилин
- •Физические свойства
- •Важнейшие химические свойства анилина
- •Применение
- •2. Белки
- •Структура белка
- •Физические свойства
- •Химические свойства
- •Функции белков в организме
Билет 5.
1. Обратимость химических реакций, химическое равновесие
Реакции, протекающие при данных условиях во взаимно противоположных направлениях, называются обратимыми.
N2 + 3H2 2NH3 + Q
Одну из реакций называют прямой, другую обратной. В таких реакциях концентрация реагирующих веществ уменьшается, следовательно, уменьшается скорость прямой реакции. При этом скорость обратной реакции постепенно увеличивается, наступает химическое равновесие, при котором скорость прямой реакции равна скорости обратной реакции. Это значит: сколько молекул образуется в единицу времени, столько и расходуется.
Состояние химического равновесия при неизменных условиях сохраняется длительное время. При изменении условий (t, давления (P) и концентрации (C)) состояние равновесия нарушается. Смещение химического равновесия определяется по принципу Ле Шателье: если на систему находящуюся в равновесии оказывать какое-либо воздействие, то равновесие смещается в направление ослабления этого воздействия.
Если реакции идёт с выделением тепла,
то при повышении t равновесие
смещается в направление «![]() »
и наоборот «
»
и наоборот «![]() ».
».
[Если + Q и t![]() ,
то
]
,
то
]
Если с уменьшением объёма (V), то при повышении давления (P) равновесие смещается в направлении и наоборот .
N2 + 3H2 2NH3 + Q
1V 3V 2V
всегда к меньшему объёму, если V
При увеличении концентрации (C) исходных веществ равновесие смещается в сторону прямой реакции и наоборот .
[Если С , то ]
если увел. С прод. реакции, то
если умен. С прод. реакции, то .
2. Ацетилен…
Ацетиле́н — ненасыщенный углеводород C2H2. Имеет тройную связь между атомами углерода, принадлежит к классу алкинов.
Атомы
углерода
в ацетилене sp-гибридизованы. Они связаны
одной![]() и
двумя
и
двумя![]() связями,
макс. плотности к-рых расположены в двух
взаимно перпендикулярных областях,
образуя цилиндрич. облако
связями,
макс. плотности к-рых расположены в двух
взаимно перпендикулярных областях,
образуя цилиндрич. облако![]() электронной
плотности; за его пределами
находятся атомы
Н (см. рис.).
электронной
плотности; за его пределами
находятся атомы
Н (см. рис.).
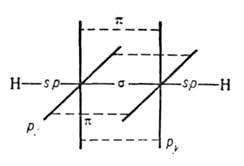
Молекула
ацетилена линейна; все 4 атома
расположены на прямой. Расстояния С![]() С
и С—Н равны соотв. 0,1205 и 0,1059 нм.
С
и С—Н равны соотв. 0,1205 и 0,1059 нм.
Для
ацетилена характерны р-ции присоединения,
к-рые происходят в две стадии: сначала
образуются замещенные этилена,
затем - замещенные алканов.
Галогены
присоединяются непосредственно,
галогеноводороды
- в присут. катализаторов
(напр., CuCl, HgCl2):
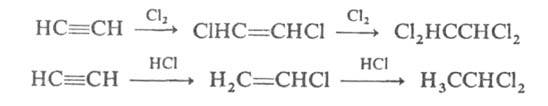
Эти р-ции используются при произ-ве тетрахлорэтилена, трихлорэтилена, винилхлорида и др. хлорсодержащих соединений.
. Гидрирование. Реакция протекает в тех же условиях, что и в случае алкенов (катализаторы Pt, Pd, Ni). При восстановлении алкинов вначале образуются алкены, а затем — алканы:
H2 H2 HC≡CH —→ H2C=CH2 —→ H3C—CH3 ацетилен этилен этан
Гидрогалогенирование. Реакции присоединения галогеноводородов, как и галогенов, идут в основном по механизму электрофильного присоединения:
HCl HCє≡CH + HCl —→ H2C=CHCl —→ H3C—CHCl2 хлорэтен 1,1-дихлорэтан (хлористый винил)
Вторая молекула галогеноводорода присоединяется в соответствии с правилом Марковникова.
Присоединение воды (реакция М.Г.Кучерова,. 1881). Катализатор — соль ртути:
HgSO4 HC≡CH + HOH ——→ H2C=CH—OH →H3C—C=O \ H виниловый уксусный спирт альдегид (промежуточный неустойчивый продукт)
Неустойчивое промежуточное соединение — виниловый спирт — перегруппировывается в уксусный альдегид.
При нагревании ацетилена в присутствии активированного угля (реакция Зелинского) осуществляется циклическая тримеризация с образованием бензола.
|
+ |
|
––600C,C |
|
При полном сгорании ацетилена на воздухе образуются два продукта оксид углерода (IV) и вода:
2НС≡СН + 5O2 → 4СO2 + 2Н2O
. ПОЛУЧЕНИЕ
Ацетилен в промышленности и в лаборатории можно получать следующими способами:
1. Высокотемпературным разложением (крекинг) природного газа — метана:
2СН4 1500°C→ НС≡СН + 3Н2
или этана:
С2Н6 1200°C→ НС≡СН + 2Н2
2. Разложением водой карбида кальция СаС2, который получают спеканием негашеной извести СаО с коксом:
СаО + 3C 2500°C→CaC2 + CO
СаС2 + 2Н2O → НС≡СН + Са(ОН)2
Билет 6.