
6. Физические свойства пластовых вод:
1
температура;2 прозрачность;3 цвет;4
запах;5 вкус;6 привкус;7плотность
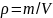 (кг/м3)
определяется количеством массы в
единице объема;8 сжимаемость;9 вязкость
– это свойство жидкости оказывать
сопротивление перемещению ее частиц
при движении.
(кг/м3)
определяется количеством массы в
единице объема;8 сжимаемость;9 вязкость
– это свойство жидкости оказывать
сопротивление перемещению ее частиц
при движении.
10 электропроводность, сименс;
11радиоактивность(наличиерадиоактивных
изотопов в воде);12 коэффициент сжимаемости
или коэффициент объемной упругости
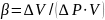 ,
м3/(Па·(м/с))=м2·с/Па,
ΔV – изменение объема, ΔР – изменение
давления, V – скорость.
,
м3/(Па·(м/с))=м2·с/Па,
ΔV – изменение объема, ΔР – изменение
давления, V – скорость.
Химические свойства пластовых вод:
Минерализация – это сумма всех минеральных веществ найденных при химическом анализе воды.
Величина сухого остатка характеризует общее содержание в воде нелетучих, минеральных и частично органических соединений, т.е. сухой остаток получают после выпаривания 1л воды и высушивания при температуре 110ºС.
Классификация пластовых вод по минерализации:
1 сверхпресные до 0,2 г/л;2 пресные 0,2÷1 г/л;3слабосолоноватые1÷3г/л;4 сильносолоноватые3÷10г/л;5соленые10÷35 г/л;6 рассолы более 35 г/л.
Компоненты:
1 Макрокомпоненты:
анионы: Cl-, SO42-, HCO3-, СО32-.
катионы: Na+, К+, Ca2+, Mg2+.
Хлор (Cl-). Источниками поступления Cl- в пластовые воды являются:
- древние морские бассейны,
- растворение каменной соли;
- поступление из вулканических газов и атмосферы;
- продукты жизнедеятельности.
Сульфат ион (SO42-) накапливается в воде в результате растворения гипсов и ангидрита; окисление сернистых соединений и сульфидных минералов.
Гидрокарбонат ион (HCO3-) поступает в пластовые воды вследствие выщелачивания известняков, доломитов, мергелей, т.е. карбонатных пород.
Натрий (Na+). Источниками поступления Na+ в пластовые воды являются:
- океанические морские воды (поверхностные воды);
- растворение и отложение каменной соли и других соленных пород.
Магний (Mg2+). Присутствие Mg2+ в пластовых водах связано с его присутствием с морскими водами в результате растворения минералов и выщелачиванием доломитов (СаMgCO3).
Кальций (Ca2+) поступает в пластовые воды в результате выщелачивания известняков, доломитов, гипсов, ангидритов.
Калий (К+), так-же как и натрий (Na+).
Жесткость воды обусловлена наличием в ней ионов кальция (Ca2+) и магния (Mg2+).
2 Микрокомпоненты – это химические элементы или соединения, содержащиеся в пластовых водах в количестве менее 10 или менее 100 мг/л (т.е. получается вся система Менделеева: Литий, Бор и т.д.).
В воде растворены следующие газы:
- кислород О2;- углекислый газ СО2;- сероводород Н2S;- водород Н2;- метан СН4;- тяжелые углеводороды;- азот N2;- инертные (благородные) газы.
7. Фазов. Сост. Ув систем
В процессе разработки месторождений в пластах изменяются давление, количественное соотношение нефти и газа, а иногда и температура. Это сопровождается непрерывными изменениями состава газовой и жидкой фаз. Закономерности фазовых переходов и фазовое состояние газонефтяных смесей необходимо знать для решения многих задач. Например, с учетом закономерностей фазовых изменений УВ составляется проект разработки газоконденсатных месторождений. Теорией фазовых изменений пользуются для расчета количества и состава газа, выделяющегося из нефти при различных давлениях и температуре.
С приближением давления и температуры к их критическим значениям, свойства газовой и жидкой фаз становятся одинаковыми, поверхность раздела между ними исчезают и плотности их уравниваются.
Для фазовых превращений однокомпонентных газов характерно постоянство давления в двухфазной области, т.е. после начала конденсации газа дальнейшее превращение его в жидкость происходит при постоянном давлении до тех пор, пока весь газ не превратится в конденсат. Точно так же со снижением давления после начала парообразования дальнейшее кипение жидкой фазы происходит при постоянном давлении.
Обе фазы (жидкость и пар) при данной температуре присутствуют в системе только в том случае, если давление равно упругости насыщенного пара этой жидкости.
С появлением в системе двух и более компонентов в закономерностях фазовых изменений возникают свои особенности.
В области чистого газа свойства многокомпонентных систем аналогичны свойствам чистых компонентов. Для двух- и многокомпонентных систем давление в процессе сжатия в двухфазной области не остается постоянным и для конденсации газа необходимо повышать его для полного превращения газовой фазы в жидкость. Поэтому давление точки кипения для многокомпонентной смеси выше давления конденсации.
Критическая температура смесей находится между критическими температурами компонентов. Критическое давление обычно выше, чем критическое давление чистых компонентов. Наибольшее критическое давление наблюдается у смеси с близким массовым содержанием обоих компонентов.
Для углеводородной бинарной смеси свойственно увеличение растворимости жидких УВ в газе с повышением p и t. При этом с ростом р увеличивается переход в газовую фазу все более тяжелых УВ.
