
- •Вопросы-ответы для экзамена.
- •Общие закономерности
- •Реакции в растворах электролитов.Гидролиз солей. Жесткость воды.
- •2. Водородный показатель (рН) величина, характеризующая активность или концентрацию ионов водорода в растворах. Водородный показатель обозначается рН.
- •Окислительно-восстановительные реакции.
- •Коррозия металлов. Гальванические элементы
- •2. Гальванические элементы- это устройство, в которых химическая энергия овр превращается в электростатическую.
- •Элементы органической химии
- •Гетерогенные системы.
- •1. Гетерогенная система состоит из двух или неск. Фаз, т.Е. Частей, отличающихся по св-вам и соприкасающихся по пов-стям раздела.
- •3. Сорбция- это процесс поглощения вещ-в из окружающей среды всем объёмом или поверхностью другого вещества.
- •4. Смачивание, поверхностное явление, наблюдаемое при контакте жидкости с твердым телом в присут. Третьей фазы-газа (пара) или др. Жидкости. Она может эту жидкость:
Вопросы-ответы для экзамена.
СТРОЕНИЕ ВЕЩ-ВА
Атом электронейтрален потому что количество протонов (положительно заряженных частиц) равно числу электронов (отрицательно заряженных частиц).
Массу атома можно определить: A = Z+N, где Z - заряд ядра (число протонов),а N - число нейтронов, A - это массовое число атома.
е=1/1840а.е.м.
р=1а.е.м.
n=1а.е.м.
В
 алентность
– способность атома к образованию
хим.связей. Валентные электроны – эл-ны
находящиеся на внешней, или валентной
оболочке атома.
алентность
– способность атома к образованию
хим.связей. Валентные электроны – эл-ны
находящиеся на внешней, или валентной
оболочке атома.
С
 .О.-
условный показатель, характеризующй
заряд атома в соединениях, исходя из
предположения, что все связи в соединениях
ионные.
.О.-
условный показатель, характеризующй
заряд атома в соединениях, исходя из
предположения, что все связи в соединениях
ионные.
Положительную С.О. проявляют все эл-ты.
Отрицательную С.О. проявляют только неМЕ, исключения:
Ge, Sn, Pb – c.o.= -4, 0, -2.
Bi – C.O.= -3, 0, +3, +5.
Po- C.O.= -2, 0, +2, +4, +6.
Отрицательная С.О. количественно равна числу е- сколько не хватает до 8ми на внешнем уровне.
–ковал.поляр
-ковал.неполяр
-ионная
-металлическая
-другие межмолекулярные связи
ОБМЕННЫЙ МЕХАНИЗМ - в образовании связи участвуют одноэлектронные атомные орбитали, т.е. каждый из атомов предоставляет в общее пользование по одному электрону:
![]() (Н2
Н. +Н. →Н:Н)
(Н2
Н. +Н. →Н:Н)
ДoНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ - образование связи происходит за счет пары электронов атома-донора и вакантной орбитали атома-акцептора:

![]()
Электроотрицательность атома- величина, характеризующая способность атома в молекуле притягивать электроны, участвующие в образовании хим.связи.
У каждого элемента своя электроотрицательность, трудно обобщить ее для Ме и для неМе, самой большой электроотрицательностью обладает F, самой маленькой Fr.
Ч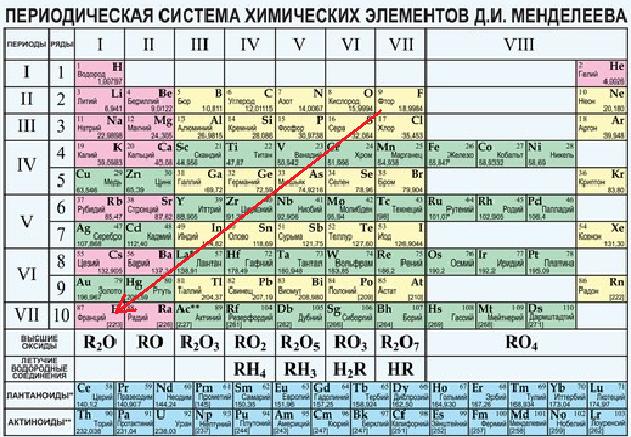 ем
ближе к Fr,
тем меньше электроотрицательность, чем
ближе к F,
тем она больше.
ем
ближе к Fr,
тем меньше электроотрицательность, чем
ближе к F,
тем она больше.
Ковалентная неполярная связь образуется между атомами неметалла одного и того же химического элемента. Такую связь имеют простые вещества, например О2; N2; C12.
Ковалентная полярная связь образуется между атомами различных неметаллов NaCl.
Общие закономерности
–Внутренняя энергия- термодинамическая функция состояния система, ее энергия, определяемая внутренним состоянием. (в ДЖ)
-Свободная энергия- изохорный потенциал, одна из характеристических функций термодинамической системы, обозначается А, определяется через внутр.энергию U,энтропию S и температуру Т. (A=U-TS)
-Потенциал Гиббса- термодинамический потенциал.(G==U-TS+PV)
-энтальпия- сложная термодинамическая функция определяет энергию необходимую для приведения системы из 1го состояния в другое и учитывающая внутреннюю энергию и работу [H].
2. реакции бывают: -экзотермические (теплота увеличивается, Н<0)
-эндотермические (Q уменьшается, Н>0)
3. з-н Гесса- изменения энтальпии в ходе реакции зависит только от природы начального и конечного состояния системы и не зависит от пути перехода от одного состояния перехода т.е. не зависит от числа промежуточных стадий.
Следствия:
-тепловой эффект прямой реакции равен по величине и противоположен по знаку тепловому эффекту обратной реакции.
-теплота образования сложного в-ва равна по абсолютной величине и противоположна по знаку теплоте разложения.
4. В химических процессах одновременно действуют 2 противоположных фактора – энтропийный (TS, степень ее беспорядка, не совершающая работу энергия).) и энтальпийный (H, изменения энергетического запаса энергии).
Суммарный эффект этих этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре определяет изменение энергии Гиббса:
ΔG = ΔH + TΔS
Если ΔG<0, то протекает прямая реакция.
Если ΔG>0, то осуществляется только обратный процесс.
Если ΔG=0, - химическое равновесие.
Термодинамическое равновесие- состояние системы, при котором остаются неизменными по времени макроскопические величины этой системы (t,p,v,энтропия).
Травн = |ΔH/ΔS|
Под скоростью реакции понимают изменение концентрации реагирующих веществ в единицу времени.

Влияющие факторы на скорость реакции:
-природа в-ва
-агрегатное состояние
-степень измельчения вещества
-природа растворителя
-концентрация веществ
-температура
-давление (только для газа)
-присутствие катализатора
-облучение
Природа в-ва- под природой в-ве понимают тип химической связи, пространственное строение молекул, межмолекулярные взаимодействия.
Скорость хим.реак. при постоянном давлении и температуре прямопропорционально произведению концентрации реагирующих веществ возведенных в степени коэффициента реакции.
При повышении температуры возрастает скорость реакции т.к.:
-увеличивается кинетическое движение частиц и возможность их соударения;
-температура повышается- повышается число активных молекул, столкновения между которыми приводят к хим. реакции, чтобы неактивные молекулы стали активными, им нужно сообщить энергию активации.
Катализаторы- в-ва которые изменяют скорость реакции и сами после реакции остаются в неизменном виде.
Положительные катализатор- увеличение скорости реакции
Отрицательный катализ – уменьшение скорости реакции.
Инициаторы- в-ва способные зарождать цепные радикальные процессы в результате распада или других химических реакций образования свободных радикалов.
Ингибиторы- в-ва замедляющие реакцию и сами в ходе реакции расходующиеся.
 Правило
Вант-Гоффа:
скорость большинства химических реакций
при повышении температуры на каждые 10
возрастает в 2-4 раза.
Правило
Вант-Гоффа:
скорость большинства химических реакций
при повышении температуры на каждые 10
возрастает в 2-4 раза.
Гетерогенные реакции- хим.реакции протекающие на границе раздела двух фаз.

Гомогенные реакции- химические реакции протекающие полностью в одной фазе.

Обратимые реакции протекают в 2х взаимопротивоположных направлениях, молекулы исходных в-в не могут полностью превратиться в молекулы продуктов реакции.
3H2 + N2 ⇌ 2NH3.
Необратимые протекают в 1м направлении, молекулы исходных веществ превращаются в молекулы продуктов реакции.
Ba(ClO2)2 + H2SO4 → 2HClO2 + BaSO4↓
Признаки необратимости:
-осадок
-выделение газа
-малодиссоциирующего в-ва
-образование комплексного иона
Состояние системы в которой скорость прямой реакции равняется скорости обратной реакции называется состоянием химического равновесия.

Принцип Ле-Шателье гласит- если на систему находящуюся в состоянии равновесия оказать какое либо внешнее воздействие (изменить температуру,давление,концентрацию), то равновесие сместится в сторону той реакции которая противодействует оказанному воздействию.
Влияние концентрации на смещение давления:

Смотреть фото выше.
