
- •1) Внутренняя энергия – функция состояния системы. 1 закон термодинамики.
- •2. Связь с термодинамическими параметрами
- •3) Энтальпия
- •4) Приложение первого закона термодинамики к идеальным газам (изохорный, изобарный процесс).
- •5) Приложение первого закона термодинамики к идеальным газам (изотермический, адиабатический процесс).
- •6) Теплоемкость и ее зависимость от температуры
- •7) Закон Гесса – основной закон термохимии.
- •8) Уравнение Кирхгоффа в дифференциальной форме.
- •9) Уравнение Кирхгоффа в интегральной форме.
- •11. Работа обратимого и необратимого процессов
- •12.Цикл Карно
- •13. Энтропия обратимых процессов.
- •14. Энтропия не обратимых процессов.
- •15. Статический смысл энтропии.
- •16. Вычисление изменения энтропии в различных термодинамических процессах
- •17. Свободная энергия Геймгольца
- •18.Свободная энергая Гиббса
- •19 Уравнение Гибса-Гельмгольца
- •20 Понятие о химическом потенциале
- •21. Химический потенциал идеального и реального газов. Летучесть
- •22 Закон действующих масс. Константа равновесия
- •23 Изотерма химической реакции Ван Гоффа.
- •24 Уравнение изобары Вант Гоффа
- •25 Уравнение изохоры Вант Гоффа
- •26 Теорема Нернста 3 закон термодинамики
- •27 Постулат Планка
8) Уравнение Кирхгоффа в дифференциальной форме.
Определяет зависимость теплового эффекта реакции от температуры.
Для определения функциональной зависимости теплового эффекта от температуры необходимо воспользоваться температурным коэффициентом теплового эффекта.
Температурный коэффициент теплового эффекта – это приращение теплового эффекта, соответствующее изменению температуры на 1 градус при условии, что постоянно давление.
Рассмотрим систему:
Рассмотрим цикл исходные вещества нагревают от T до T+dT затем протекает химическая реакция и полученные продукты охлаждаются обратно, затем реакция протекает в обратном направлении.
В соответствии с законом Гесса сумма тепловых эффектов в результате завершения цикла будет равна 0.
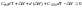
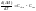 (1)
– выражение уравнения Кирхгоффа в
дифференциальной форме.
(1)
– выражение уравнения Кирхгоффа в
дифференциальной форме.
Температурный коэффициент теплового эффекта – равен изменению суммарной теплоемкости системы, обусловленному протеканием данной реакции в отсутствии фазовых превращений в противном случае формулу необходимо включить теплоты этих превращений.
Анализ: в уравнение Кирхгоффа
1)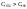
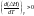 с увеличением температуры тепловой
эффект увеличивается.
с увеличением температуры тепловой
эффект увеличивается.
2)
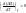 тепловой коэффициент от температуры
не зависит.
тепловой коэффициент от температуры
не зависит.
3)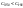
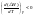 с увеличением температуры тепловой
эффект уменьшается.
с увеличением температуры тепловой
эффект уменьшается.
Уравнение Кирхгоффа в дифференциальном виде может качественно указать на характер изменения теплового эффект (энтальпии) с изменением температуры
9) Уравнение Кирхгоффа в интегральной форме.
Для определения количественных зависимостей необходимо получить уравнение Кирхгофа в интегральном виде.
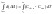
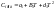
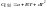
 -
тепловой эффект реакции при стандартных
условиях или тепловой эффект данной
реакции при какой-либо другой
температуры(если он известен).
-
тепловой эффект реакции при стандартных
условиях или тепловой эффект данной
реакции при какой-либо другой
температуры(если он известен).
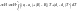
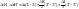
 -
уравнение Кирхгофа в интегральном
виде.
-
уравнение Кирхгофа в интегральном
виде.
Вывод: уравнение Кирхгофа позволяет определить тепловой эффект реакции при любой температуре (если известен ее тепловой эффект) или при нормальных условиях, или при любой другой-либо температуре.
11. Работа обратимого и необратимого процессов
W1<Wравновесии W2>Wравн Т=const p - изменяется
W1=pΔV W2= -pΔV W1< W2
Работа данного процесса будет определяться площадью фигуры под нижней кривой.
Проведём обратный процесс(ставим гири на поршень)
При уменьшении массы гирь до бесканечно малых величин , величина ступенек будет уменьшаться и при бесконечно малой массе гирь скорость изменения давления будет равна скорости изменения объёма. Таким образом мы получаем обратимый процесс.
W1=W2=Wравн.
Вывод: Работа совершённая системой при необратимом процессе меньше чем при обратимом и наобарот. Работа совершённая над системой больше больше работы совершённой при обратимом процессе. Таким образом при неравновесном (необратном) процессе часть энергии не обратима переходит в другой вид или теряется в виде теплоты, каторая рассеивается в окружающей среде. В реальных условиях не существует обратимых процессов. Все реальные процессы являются не обратимыми, для них невозможно найти способ возврата их в первоначальное состояние.
