
Отёк
|
ОТЁК |
|
типовая форма нарушения водного баланса организма, |
|
характеризующаяся накоплением избытка жидкости |
|
в межклеточном пространстве и/или полостях тела. |
Виды отёчной жидкости
Отёчная жидкость может иметь различный состав и консистенцию. Она может быть в виде:
• Транссудата — бедной белком (менее 2%) жидкости.
• Экссудата — богатой белком (более 3%, иногда до 7–8%) жидкости, часто содержащей форменные элементы крови.
• Слизи, представляющей собой смесь из воды и коллоидов межуточной ткани, содержащих гиалуроновую и хондроитинсерную кислоты. Этот вид отёка называют слизистым, или микседемой. Микседема развивается при дефиците в организме йодсодержащих гормонов щитовидной железы.
Виды отёков
Отёки дифференцируют в зависимости от их локализации, распространённости, скорости развития и по основному патогенетическому фактору развития отёка.
• В зависимости от локализации отёка различают анасарку и водянки.
† Анасарка — отёк подкожной клетчатки.
† Водянка — отёк полости тела (скопление в ней транссудата).
‡ Асцит — скопление избытка транссудата в брюшной полости.
‡ Гидроторакс — накопление транссудата в грудной полости.
‡ Гидроперикард — избыток жидкости в полости околосердечной сумки.
‡ Гидроцеле — накопление транссудата между листками серозной оболочки яичка.
‡ Гидроцефалия — избыток жидкости в желудочках мозга (внутренняя водянка мозга) и/или между мозгом и черепом — в субарахноидальном или субдуральном пространстве (внешняя водянка мозга).
• В зависимости от распространённости различают местный и общий отёки.
† Местный (например, в ткани или органе в месте развития воспаления или аллергической реакции).
† Общий — накопление избытка жидкости во всех органах и тканях (например, гипопротеинемические отёки при печёночной недостаточности или нефротическом синдроме).
• В зависимости от скорости развития отёка говорят о молниеносном и остром развитии или хроническом течении отёка.
† Молниеносный отёк развивается в течение нескольких секунд после воздействия (например, после укуса насекомых или змей).
2) Острый отёк развивается обычно в пределах часа после действия причинного фактора (например, отёк лёгких при остром инфаркте миокарда).
3) Хронический отёк формируется в течение нескольких суток или недель (например, нефротический, отёк при голодании).
• В зависимости от основного патогенетического фактора различают гидродинамический, лимфогенный, онкотический, осмотический и мембраногенный отёки.
Патогенетические факторы развития отёка
Гидродинамический фактор
Гидродинамический (гемодинамический, гидростатический, механический) фактор характеризуется увеличением эффективного гидростатического давления.
• Причины активации гемодинамического отёка приведены на рис. 1.
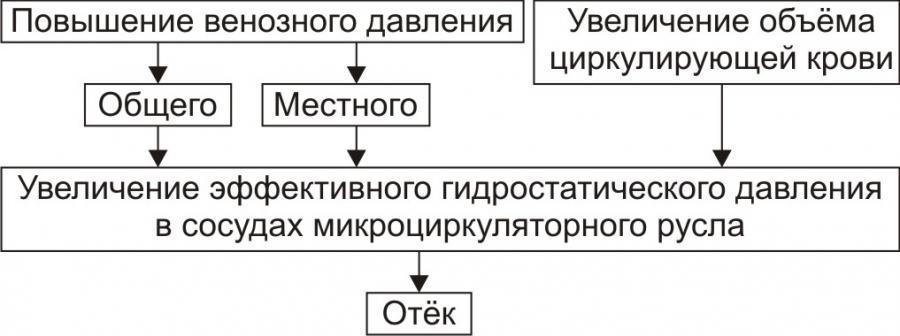
Рис. 1. Причины включения гидродинамического фактора развития отёка.
† Повышение венозного давления
‡ Общее венозное давление повышается при недостаточности сердца в связи со снижением его сократительной и насосной функции.
‡ Местное венозное давление повышается при обтурации венозных сосудов (например, тромбом или эмболом) и при сдавления вен и/или венул (например, опухолью, рубцом, отёчной тканью).
† Увеличение ОЦК (например, при гиперволемии, полицитемии, водном отравлении).
• Механизмы реализации гидродинамического фактора приведены на рис. 2.
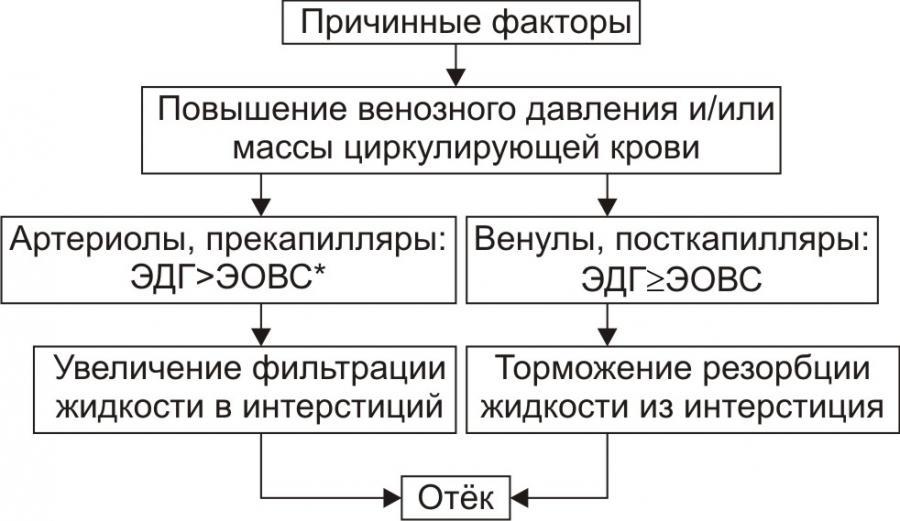
Рис. 2. Механизмы реализации гидродинамического фактора развития отёка. ЭДГ>ЭОВС — эффективное гидростатическое давление > эффективной онкотической всасывающей силы.
† Увеличение фильтрации жидкости в артериальной части капилляра вследствие повышения эффективного гидростатического (следовательно — фильтрационного) давления. Как правило, этот механизм активируется при значительном возрастании ОЦК и/или АД.
† Снижение тургора тканей. Тургор характеризует напряжённость, эластичность ткани. Он определяет степень её механического сопротивления давлению. Уменьшение тургора является важным фактором, потенцирующим фильтрацию жидкости из сосуда в ткань.
Причины снижения тургора ткани:
‡ Уменьшение содержания коллагеновых волокон (например, по мере старения организма, при кахексии, длительном общем голодании).
‡ Увеличение активности гиалуронидазы. Под её влиянием разрушаются кислые гликозаминогликаны. Это повышает рыхлость соединительной ткани и способность её вмещать больший объём жидкости при сравнительно небольшом увеличении эффективного гидростатического давления.
† Торможение резорбции интерстициальной жидкости в посткапиллярах и венулах в результате повышения эффективного гидростатического давления — разницы между гидростатическим давлением межклеточной жидкости (оно ниже атмосферного и равно в среднем 7 мм рт.ст.) и гидростатическим давлением крови в микрососудах. В норме эффективное гидростатическое давление составляет в артериальной части микрососудов 36–38 мм рт.ст., а в венозной — 14–16 мм рт.ст.
‡ Резорбция жидкости в венозной части капилляра потенцируется эффективной онкотической всасывающей силой крови. Она равна 19–22 мм рт.ст. и является разницей онкотического давления крови (25–28 мм рт.ст.) и интерстициальной жидкости (около 6 мм рт.ст.).
‡ Там, где эффективное гидростатическое давление больше эффективной онкотической всасывающей силы крови, осуществляется фильтрация воды в межклеточное пространство (в норме это происходит в артериолах и прекапиллярах); в микрососудах, где эффективное гидростатическое давление меньше эффективной онкотической всасывающей силы крови, происходит резорбция жидкости из интерстиция в просвет микрососуда (в норме — в посткапиллярах и венулах).
‡ При различных формах патологии эффективное гидростатическое давление может увеличиваться. В связи с этим тормозится резорбция интерстициальной жидкости в венозной части капилляра: в межклеточном пространстве накапливается вода — развивается отёк.
Лимфогенный фактор
Лимфогенный (лимфатический) фактор характеризуется затруднением оттока лимфы от тканей вследствие либо механического препятствия, либо избыточного образования лимфы.
• Причины включения лимфогенного фактора перечислены на рис. 3.
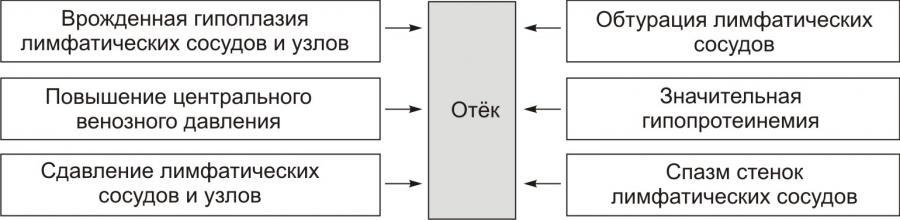
Рис. 3. Причины включения лимфогенного фактора развития отёка.
† Врождённая гипоплазия лимфатических сосудов и узлов.
† Сдавление лимфатических сосудов (например, опухолью, рубцом, гипертрофированным соседним органом).
† Эмболия лимфатических сосудов (например, клетками опухоли, фрагментами тромба, паразитами, последнее нередко наблюдается при попадании в лимфатические сосуды филярий).
† Опухоль лимфоузла (например, лимфома или лимфосаркома), а также метастазы опухолей других тканей.
† Повышение центрального венозного давления (например, при сердечной недостаточности или увеличении внутригрудного давления).
† Спазм стенок лимфатических сосудов (например, при активации симпатикоадреналовых влияний при стрессе, неврозе; выбросе избытка катехоламинов при феохромоцитоме).
† Значительная гипопротеинемия (менее 35–40 г/л при норме 65–85 г/л). Это является результатом возрастания тока жидкости из сосудов в интерстициальное пространство по градиенту онкотического давления. Вследствие этого значительно повышается образование лимфы в тканях.
• Механизмы реализации лимфогенного патогенетического фактора развития отёка (рис. 4) различны при динамической и механической лимфатической недостаточности.
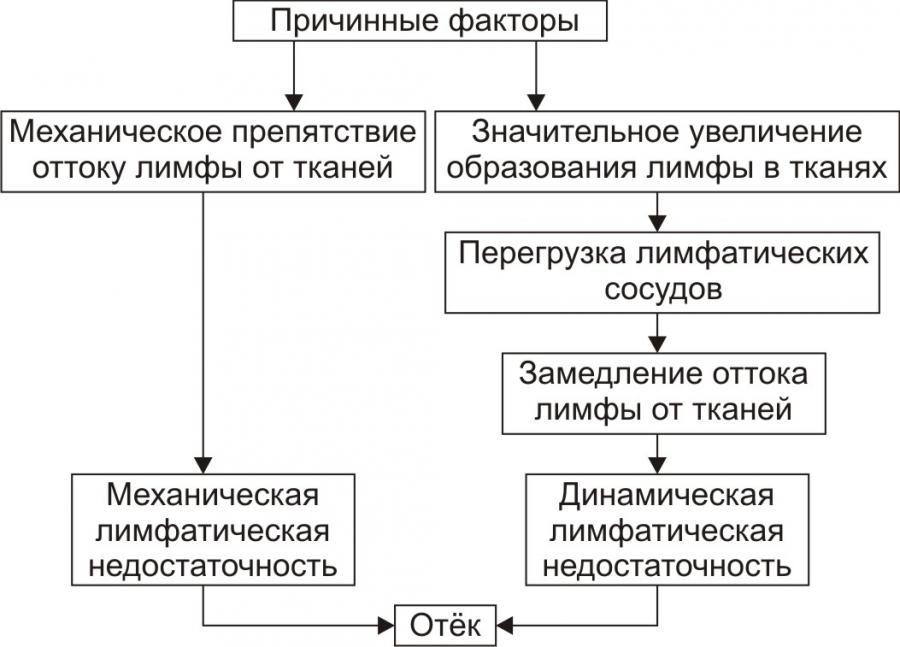
Рис. 4. Механизм реализации лимфогенного фактора развития отёка.
† Динамическая лимфатическая недостаточность.
Динамическая лимфатическая недостаточность является результатом значительного возрастания лимфообразования. При этом лимфатические сосуды не способны транспортировать в общий кровоток существенно увеличенный объём лимфы. Подобная картина может наблюдаться при гипопротеинемии у пациентов с нефротическим синдромом или печёночной недостаточности.
† Механическая лимфатическая недостаточность является следствием механического препятствия оттоку лимфы по сосудам в результате их сдавления или обтурации. Формирование отёка по такому механизму на нижних конечностях обозначают как слоновость. При слоновости нога может достигать огромных размеров и веса (до 40–50 кг). Такой же механизм может лежать в основе отёка верхних конечностей, половых органов и других регионов тела, часто обширных.
Существенно, что при лимфогенных отёках в тканях накапливается жидкость, богатая белком (до 3–4 г%), а также наблюдается избыточное образование коллагеновых волокон и других элементов соединительной ткани, что деформирует органы и ткани.
Онкотический фактор
Для онкотического (гипоальбуминемического, гипопротеинемического) фактора развития отёка характерно снижение онкотического давления крови и/или увеличение его в межклеточной жидкости.
• Причины (рис. 5).
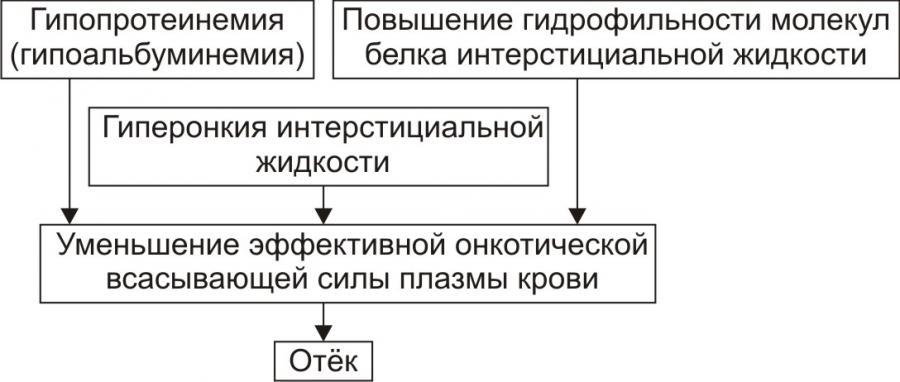
Рис. 5. Причины включения онкотического фактора развития отёка.
† Снижающие онкотическое давление крови в результате гипопротеинемии. Гипопротеинемия (в основном за счёт гипоальбуминемии; альбумины примерно в 2,5 раза более гидрофильны, чем глобулины) наиболее часто является следствием:
‡ Недостаточности поступления белков в организм при:
§ общем или белковом голодании,
§ нарушении полостного и/или мембранного пищеварения (например, при резекции фрагментов кишечника, дисбактериозе, синдромах мальабсорбции).
‡ Снижении синтеза альбуминов в печени (например, при воздействии на неё гепатотропных ядов, выраженном циррозе).
‡ Избыточной потере белка организмом (например, с мочой при нефротическом синдроме, с плазмой крови при обширных ожогах; с калом при расстройстве пищеварения в желудке и кишечнике).
† Повышающие онкотическое давление интерстициальной жидкости. Эти причины имеют в основном регионарное значение и вызывают или потенцируют развитие местных отёков. Гиперонкия интерстициальной жидкости является результатом:
‡ Избыточного транспорта белков плазмы крови в межклеточное пространство. Обычно это обусловлено повышением проницаемости стенок микрососудов при:
§ развитии воспаления или местных аллергических реакций (под влиянием медиаторов воспаления и аллергии, например, кининов, гистамина, серотонина);
§ действии некоторых химических веществ (например, хлора, фосгена, люизита);
§ попадании в ткань ядов насекомых и пресмыкающихся;
§ воздействии ядов микробов (например, возбудителей дифтерии или сибирской язвы).
‡ Выхода в межклеточную жидкость белков клеток при их повреждении или разрушении (например, в очаге воспаления, при ишемии, аллергической реакции).
‡ Увеличения гидрофильности белковых мицелл интерстициальной жидкости. Это может быть при:
§ накоплении в интерстиции избытка некоторых ионов (например, H+, K+, Na+),
§ дефиците в межклеточном пространстве ионов Ca2+,
§ избытке БАВ (например, гистамина и серотонина),
§ дефицита йодсодержащих тиреоидных гормонов.
• Механизм реализации онкотического фактора (рис. 6) заключается в уменьшении эффективной онкотической всасывающей силы (как следствие гипопротеинемии и/или гиперонкии ткани). В результате возрастает объём фильтрации воды из микрососудов в интерстициальную жидкость по градиенту онкотического давления и уменьшается резорбция жидкости из межклеточного пространства в посткапиллярах и венулах.
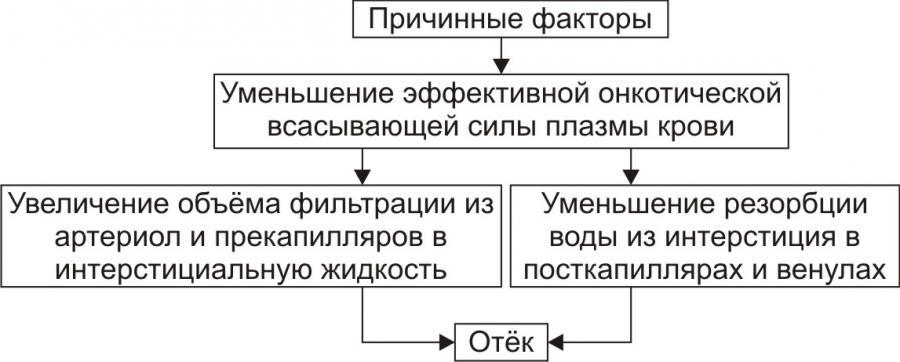
Рис. 6. Механизм реализации онкотического фактора развития отёка.
Осмотический фактор
Осмотический фактор развития отёка заключается либо в повышении осмоляльности интерстициальной жидкости, либо в снижении осмоляльности плазмы крови, либо в сочетании того и другого.
• Причины включения осмотического фактора отёка представлены на рис. 7.
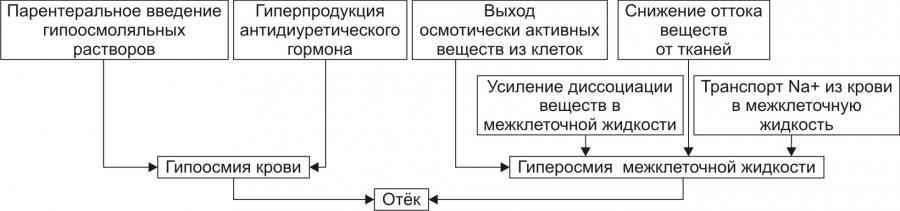
Рис. 7. Причины включения осмотического фактора отёка.
† Факторы, снижающие осмотическое давление крови.
‡ Парентеральное введение больших объёмов растворов, содержащих соли в недостаточном количестве. В реальной клинической практике это встречается чрезвычайно редко (являясь следствием врачебной ошибки, например, при проведении мероприятий по устранению гипогидратации организма или отклонений показателей КЩР). Даже в этих случаях избыточная жидкость быстро выводится почками при условии нормальной их экскреторной функции.
‡ Гиперпродукция АДГ. Может наблюдаться при повышении внутричерепного давления, повреждении структур гипоталамуса (особенно нейронов его супраоптических ядер), после энцефалитов. Повышение в связи с этим продукции АДГ в гипоталамусе и его уровня в крови стимулирует избыточную реабсорбцию воды в почках. Однако, и в данном случае, как правило, в почках повышена и реабсорбция Na+, что препятствует развитию гипоосмии крови.
† Факторы, повышающие осмоляльность интерстициальной жидкости.
‡ Выход из повреждённых или разрушенных клеток осмотически высокоактивных веществ (например, ионов Na+, K+, Ca2+, глюкозы, МК, азотистых соединений).
‡ Повышение диссоциации в интерстициальной жидкости солей и органических соединений (например, в условиях гипоксии или ацидоза).
‡ Снижение оттока осмотически активных веществ (ионов, органических и неорганических соединений) от тканей в результате расстройств микроциркуляции.
‡ Транспорт Na+ из плазмы крови в интерстициальную жидкость. Это может наблюдаться, например, при гиперальдостеронизме.
• Механизм реализации осмотического фактора развития отёка (рис. 8) заключается в избыточном транспорте воды из клеток и сосудов микроциркуляторного русла в межклеточную жидкость по градиенту осмотического давления (более высокого в интерстиции). Данный механизм включается как компонент патогенеза при сердечном, почечном (нефритическом), печёночном и других отёках.
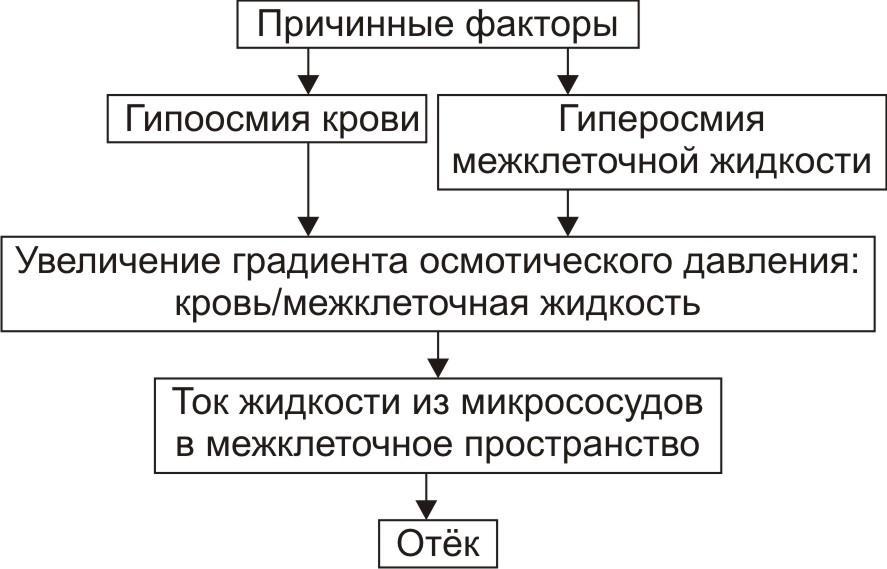
Рис. 8. Механизм осмотического фактора отёка.
Мембраногенный фактор
Мембраногенный фактор характеризуется существенным повышением проницаемости стенок сосудов микроциркуляторного русла для воды, мелко- и крупномолекулярных веществ (наибольшее значение среди последних имеют белки).
• Причины повышения проницаемости стенок микрососудов перечислены на рис. 9.
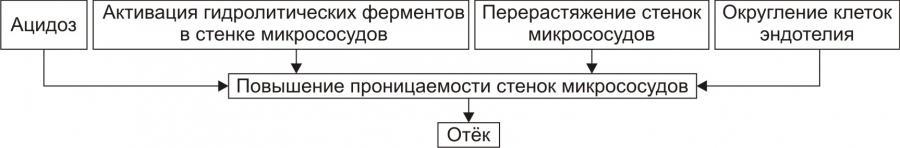
Рис. 9. Причины включения мембраногенного фактора развития отёка.
† Ацидоз. В условиях ацидоза возрастает неферментный («кислотный») гидролиз основного вещества базальной мембраны сосудистой стенки. Это и приводит к её разрыхлению и как следствие — возрастанию проницаемости.
† Повышение активности гидролитических ферментов в стенке микрососудов и/или прилегающих к ним тканях. Это интенсифицирует процесс ферментативного гидролиза гликозаминогликанов, а также волокнистых структур сосудистой стенки. Такая картина наблюдается при выраженной гипоксии, ацидозе, при воздействии так называемых лабилизаторов лизосом (например, лизофосфолипидов, продуктов липопероксидации, протеолитических ферментов).
† Перерастяжение стенок микрососудов. Это наблюдается при:
‡ Развитии артериальной гиперемии нейромиопаралитического типа (т.е. в условиях длительного снижения нейрогенного и мышечного тонуса артериол и прекапилляров).
‡ Венозной гиперемии и лимфостазе.
• Механизмы реализации мембраногенного фактора развития отёка (рис. 10).
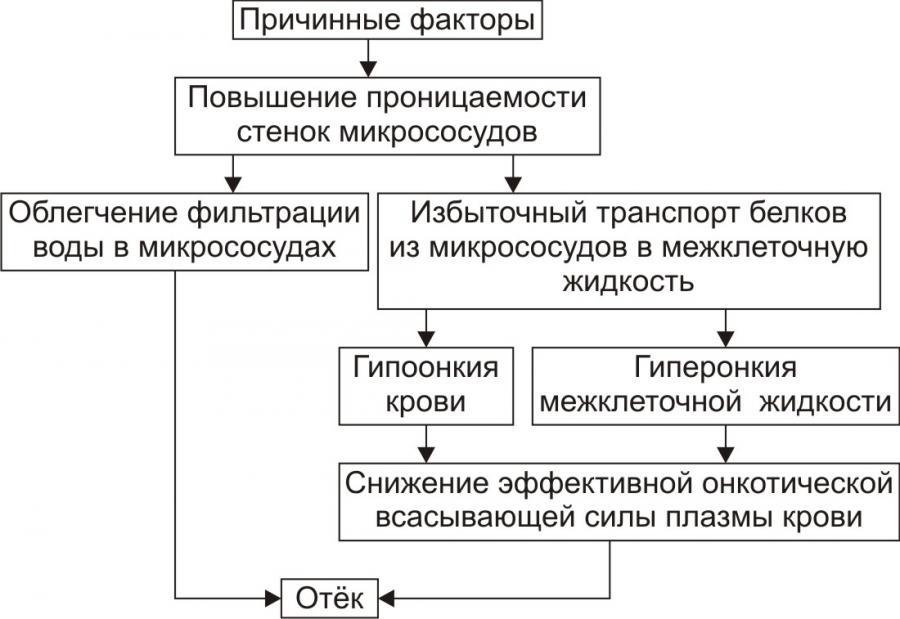
Рис. 10. Механизм реализации мембраногенного фактора развития отёка.
† Облегчение фильтрации воды. В связи с этим увеличивается выход жидкости из крови и лимфы в интерстициальное пространство. Однако, этот механизм может быть сбалансирован повышением реабсорбции воды в венозном отделе капилляров в связи с истончением их стенок.
† Увеличение выхода молекул белка из микрососудов в межклеточную жидкость. Это ведёт к снижению онкотического давления плазмы крови и лимфы и одновременно к развитию гиперонкии межклеточной жидкости. В условиях повышенной проницаемости стенок микрососудов жидкость из них интенсивно поступает в межклеточное пространство по градиенту онкотического давления. Именно такой механизм (помимо других) лежит в основе развития отёка тканей при их воспалении, местных аллергических реакциях, укусах насекомых и змей, действии некоторых отравляющих веществ, чистого кислорода, особенно при избыточном атмосферном давлении.
Многофакторность
В клинической практике, как правило, не встречаются отёки, развивающиеся на основе только одного из описанных выше патогенетических факторов (иначе говоря нет монопатогенетических отёков). В связи с этим в каждом конкретном случае при наличии отёка выделяют: 1) инициальный (стартовый, первичный) патогенетический фактор у данного пациента и 2) патогенетические факторы, включающиеся в процессе развития отёка вторично.
