
- •Банк тестовых заданий
- •Содержание гос
- •Тематическая структура тестовых материалов
- •Тестовые задания
- •*Возрастает
- •*Размером электронной орбитали
- •*Нейтронов
- •*Число химических связей, образованных данным атомом в соединении
- •*Моль/л
- •*Добавлении щелочи в раствор
- •*Добавлении щелочи в раствор
- •*Гидроксида калия
- •*Индикатором
- •*Средняя
- •*Нитрат бария
- •*Черного осадка
- •*Первого;
- •*В 2 раза;
- •*50 Часов;
- •*3. Большей энергией по сравнению с молекулами в объеме фазы;
- •*Суспензиями;
- •*Седиментационной,
- •*Размера частиц,
- •*Голубой.
- •Повышению; 2. Понижению.
- •*Вязкости среды и температуры;
-
нитрат натрия
-
*Нитрат бария
-
нитрат аммония
-
нитрат калия
Черный
осадок с сульфид-ионом
![]() образует ион…
образует ион…
-

-

-
*
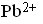
-
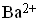
При действии сероводорода на раствор, содержащий ионы Cu2+, наблюдается образование…
-
синего раствора
-
*Черного осадка
-
белого осадка
-
красного раствора
Образование осадка наблюдается при сливании растворов…
-

-
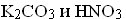
-

-
*

Медная пластинка чернеет под действием раствора, содержащего…
-
*

-
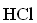
-
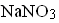
-
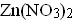
Выделение газа при добавлении сильной кислоты в исследуемый раствор указывает на наличие ионов…
-
Cl-
-
PO43-
-
NO3-
-
*CO32-
Дидактическая единица №2. Аналитическая химия: Тема 9. Количественный химический анализ.
Для осаждения хлорид-ионов из 100 мл раствора соляной кислоты с молярной концентрацией 0,1 моль/л требуется раствор, содержащий ____грамма нитрата серебра.
-
10,2
-
5,1
-
6,8
-
*1,7
Количество азотной кислоты, содержащееся в растворе, на нейтрализацию которого израсходовано 100мл раствора NaOH с молярной концентрацией 0,2моль/л, составляет ____ моль.
-
0,01
-
*0,02
-
0,1
-
0,2
Объем 0,1М раствора NaOH, необходимый для нейтрализации 20 мл 0,1М HCl равен ____мл.
-
4
-
*20
-
2
-
40
Объем 0,2н раствора H2SO4 , необходимый для осаждения ионов бария из 100 мл 0,2н раствора BaCl2, равен ____мл.
-
200
-
20
-
*100
-
50
Метод анализа, основанный на точном измерении массы определяемого вещества или его составных частей, выделяемых виде соединений постоянного состава, называется …
-
колориметрическим
-
физическим
-
*гравиметрическим
-
титриметрическим
Дидактическая единица 2. Аналитическая химия: Тема задания 10. Методы разделения и концентрирования веществ.
В методе экстракции в качестве экстрагентов чаще других используются…
-
*органические вещества,
-
сильные основания,
-
сильные кислоты,
-
неорганические вещества.
Дидактическая единица 2. Аналитическая химия: Тема задания 11. Физико-химические и физические методы анализа.
Метод анализа, основанный на зависимости массы преобразованного вещества от количества электричества, называется …
-
потенциометрией
-
полярографией
-
*кулонометрией
-
кондуктометрией
Хроматографические методы анализа основаны на различной _________ способности определяемых веществ.
-
*сорбционной
-
электрохимической
-
фотохимической
-
окислительно-восстановительной
Методы анализа, основанные на способности вещества поглощать свет определенной длины волны, называются…
-
*спектрофотометрическим
-
потенциометрическим
-
радиометрическим
-
фотоэмиссионным
Метод определения молярной массы растворенного вещества по понижению температуры замерзания его раствора называется…
-
перегонкой
-
эбуллиоскопией
-
*криоскопией
-
экстракцией
Метод определения молярной массы растворенного вещества по повышению температуры кипения раствора называется…
-
перегонкой
-
*эбуллиоскопией
-
криоскопией
-
экстракцией
Метод анализа, основанный на зависимости электропроводности раствора от концентрации электролита, называется…
-
полярометрией
-
рефрактометрией
-
*кондуктометрией
-
кулонометрией
К физико-химическим методам анализа относятся…
-
гравиметрический и титрометрический
-
*электрохимические и спектральные
-
титрометрические и электрохимические
-
спектральные и гравиметрические
Для получения керосина из нефти используется метод…
-
кристаллизации
-
флотации
-
*дистилляции
-
экстракции
Дидактическая единица 2. Аналитическая химия: Тема задания 12. Физические методы анализа.
Физический метод анализа, в основе которого используется способность электромагнитного излучения вызывать свечение исследуемого объекта, называется…
-
атомно-адсорбционным,
-
*люминесцентным,
-
эмиссионным,
-
спетрофотомерическим.
Методы анализа, основанные на способности вещества поглощать свет определенной длины волны, называются…
*1) спектрофотометрическим
2) потенциометрическим
3) радиометрическим
4) фотоэмиссионным
Дидактическая единица 3. Физическая химия: Тема задания 13. Основы химической термодинамики.
Функциями состояния термодинамической системы являются …
1. работа;
*2. внутренняя энергия;
*3. энтальпия;
4. теплота;
*5. энтропия;
6. все величины.
Закон, отражающий зависимость между работой, теплотой и внутренней энергией системы …
1. закон Гесса;
2. второй закон термодинамики;
*3. первый закон термодинамики;
4. закон Гиббса.
Укажите уравнения, отражающие математическую запись первого закона термодинамики в интегральной и дифференциальной форме …
1. Q=U+A;
*2. Q=dU+A;
3. dQ=dU+A;
4. Q=dU+A;
5. Q=U+A;
*6. Q=U+A.
Для изолированной системы …
1. U=0;
*2. U=const;
*3. U=0;
4. все утверждения верны.
Тепловой эффект химической реакции не зависит от …
1. агрегатного состояния исходных веществ;
*2. числа стадий химического процесса;
3. температуры;
4. агрегатного состояния продуктов реакции.
Энтальпия образования хлора (ΔH0) при стандартных условиях принята равной … кДж/моль.
1. 8,314;
2. 273;
*3. 0;
4. 1.
Исходя из уравнения реакции 2С(графит) + 2Н2(г) С2Н4, ΔH0 r, 298=52,3 кДж, стандартная
энтальпия образования этилена равна …
1. -104,6 кДж/моль;
*2. 52,3 кДж/моль;
3. -52,3 кДж/моль;
4. 104,6 кДж/моль.
Для получения 1132 кДж тепла по реакции
2NO(г) + О2(г) ↔ 2NO2(г), ΔH r =566 кДж необходимо затратить кислорода в объеме (н.у.) …
1. 22,4 л;
2. 11,2 л;
3. 5,6 л;
*4. 44,8 л.
Если при разложении перхлората калия, согласно термохимическому уравнению KClО4 (тв) KCl (тв) + 2 О2 (г), ∆rН0 = 33 кДж, образовалось 10 моль кислорода, то количество затраченного тепла равно ______ кДж.
1. 132
2.*165
3. 66
-
330
Для получения 1132 кДж тепла по реакции 2NO (г) + О2 (г) 2NO2 (г), ∆rН0 = - 566 кДж, необходимо затратить ______ литров кислорода.
-
22,4
-
56
-
*44,8
-
11,2
Для реакций, протекающих с участием веществ только в конденсированном состоянии (твердое или жидкое) …
1. Hреак>Uреак;
2. Hреак<Uреак;
*3. Hреак=Uреак;
4. могут реализоваться все случаи.
К эндотермическим процессам, для которых ΔH0r >ΔU0r относятся (два ответа) …
*1. 2NH3(г) = N2(г) + 3H2;
*2. CaCO3(г) = CaO(тв) + CO2;
3. 2N2(г) + O2(г) = 2N2O.
Тенденцию системы к достижению состояния, которому соответствует максимальная беспорядочность распределения частиц, отражает функция состояния …
1. внутренняя энергия;
2. энтальпия;
*3. энтропия;
4. энергия Гиббса.
При 0 0С вода может находиться в трех агрегатных состояниях: твердом (лед), жидком (вода) и газообразном (пар). Минимальная энтропия для одного килограмма вещества будет у …
1. пара;
2. воды;
*3. льда;
4. одинакова.
Для определения направления самопроизвольных процессов, протекающих при постоянном давлении и температуре, используют величину изменения …
*1. изобарно-изотермического потенциала, G0;
2. энтропии S0;
3. энтальпии 0.
Выберите значения величин H0 и S0, для которых процесс будет возможен при любых температурах;
Б – процесс будет невозможен ни при каких температурах …
1. 0>0S0>0;
2. 0>0S0<0;
3. 0<0S0<0;
* 4. 0<0S0>0.
Выберите значения величин H0 и S0, для которых процесс будет невозможен ни при каких температурах …
1. 0>0S0>0;
*2. 0>0S0<0;
3. 0<0S0<0;
4. 0<0S0>0.
Дидактическая единица 3. Физическая химия: Тема задания 14. Химическая кинетика и катализ.
Основной постулат химической кинетики утверждает, что скорость химической реакции …
1. определяется изменением числа реагирующих молекул в единицу
времени в единице объема;
2. возрастает с увеличением температуры;
3. состоящей из ряда последовательных стадий, определяется скоростью
самой медленной стадии;
*4. пропорциональна произведению концентраций реагирующих
веществ, возведенных в степени, равные порядку реакции по веществу.
Численное значение константы скорости и скорости реакции совпадают для реакций…
1. первого порядка;
2. второго порядка при равной концентрации реагирующих
веществ;
*3. любого порядка при концентрации реагентов, равной 1 моль/л;
4. протекающих в одну стадию (простых) реакций.
Скорость элементарной химической реакции с увеличением времени её протекания …
1. увеличивается;
*2. уменьшается;
3. изменяется неоднозначно;
4. не изменяется.
Математическое выражение для скорости химической реакции, идущей в одну стадию по схеме:
А(г)+2В(г)→С(г), описывается уравнением …
1. =k[A][2B];
*2. =k[A][B]2;
3. =2k[A][B];
4. =k[A][2B]2.
Порядок и молекулярность совпадают для … реакций.
1. сложных;
*2. простых;
3. последовательных;
4. параллельных.
Простая реакция протекает согласно уравнению: A + 2B → C + D. Если концентрация вещества А много больше концентрации вещества В, то (два ответа) …
1. порядок реакции равен трем;
2. порядок реакции равен единице;
*3. порядок реакции равен двум;
4. реакция мономолекулярная;
5. реакция бимолекулярная;
*6. реакция тримолекулярная.
Период полупревращения не зависит от концентрации исходных веществ для реакции … порядка.
