
- •1. Простейшие стехиометрические расчеты
- •Задания для выполнения контрольной работы
- •2. Строение атома.
- •3. Химическая связь. Примеры решения типовых задач
- •4. Основные понятия о химической кинетике. Примеры решения типовых задач
- •5. Растворы электролитов
- •6. Основы электрохимии. Примеры решения типовых задач
- •7. Классификация неорганических веществ. Примеры решения типовых задач
- •Варианты контрольных заданий
- •Список литературы
Методические указания по предмету ХИМИЯ
Среди дисциплин, составляющих базовую подготовку специалистов и бакалавров, важное место занимает химия— наука, изучающая общие свойства и формы движения материи. С успехами химии и смежных с ней наук связано появление новых источников энергии, создание синтетических материалов, расширение сырьевой базы. Знание химии необходимо не только для понимания основ создания новых материалов и технологических процессов, но и для сохранения здоровья людей. Безответственное отношение к этим вопросам, отсутствие элементарной «химической культуры» уже сегодня пагубно отразилось на окружающей среде и поставило человечество на край экологической пропасти. Химия является одним из основных компонентов, составляющих методологическую базу подготовки специалистов в области естественных и технических наук.
Основной составляющей учебного процесса для студента-заочника является самостоятельная работа с литературой.
В обязательный план входит посещение лекций, выполнение трех контрольных заданий, написание реферата, индивидуальные и групповые консультации, выполнение лабораторного практикума, сдача зачета по лабораторному практикуму, сдача экзамена по всему курсу.
Работа с учебником и методической литературой. Учебники и методическую литературу студент получает в библиотеке института, филиала или учебно-консультационного пункта, к которому он прикреплен. Курс общей и неорганической химии изучают в соответствии с разделами программы.
Контрольные задания. При изучении курса общей и неорганической химии студент выполняет три контрольные работы. После проработки главы учебника и усвоения теоретического материала студент приступает к выполнению контрольных задач по этой теме из контрольных заданий. Решение задач и ответы на вопросы должны быть обоснованы с использованием основных теоретических положений. При решении числовых задач приводится весь ход решения и математического преобразования.
Контрольная работа выполняется в отдельной тетради с полями 40 мм. Номера и условия задач переписываются в порядке, указанном в контрольной работе. В конце работы приводится список использованной литературы, наименование учебника и года издания. Работа подписывается студентом с указанием даты и представляется на факультет для рецензирования.
Если контрольная работа не зачтена, то неверно решенные задачи исправляются студентом в этой же тетради на чистых листах, а не в рецензируемом тексте, согласно требованиям, предъявляемым к оформлению контрольных задач. Контрольная работа, выполненная по своему варианту, который указывает преподаватель.
1. Простейшие стехиометрические расчеты
Для решения задач, заключающих стехиометрические расчеты, необходимо уяснить простейшие стехиометрические, а также газовые понятия и законы.
МВ – молярная масса вещества В, г/моль,
nВ – количество вещества В, моль,
mВ – масса вещества В, г
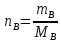
VM – молярный объем газообразного вещества В, при нормальных условиях для любого газа составляет 22,4 л
Моль – количество вещества, содержащие в себе 6,02*1023 структурных единиц (атомов, молекул, ионов, электронов и т. д.).
Число 6,02*1023 было установлено итальянским учёным Авогадро.
Для любого вещества молярная масса численно равно его молекулярной массе, выраженной в граммах.
Во многих химических реакциях принимает участие не целая частица вещества В, а лишь её часть, которую называют эквивалентом.
Эквивалентом вещества называется некая реальная или условная частица вещества В, которая в данной кислотно – основной реакции эквивалентна одному иону водорода Н+ или в данной реакции окисления – восстановления эквивалента одному электрону. Под условной частицей понимают атом, молекулу, ион, электрон.
Эквивалентом вещества также называют количество эквивалентов вещества, т.е. число молей вещества эквивалентное 1 молю катионов водорода в рассматриваемой реакции.
Meq B – молярная масса эквивалента вещества В, г/моль,
neq B – количество эквивалентов вещества В, моль
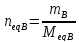
Закон эквивалентов: массы реагирующих веществ пропорциональны молярным массам эквивалентов этих веществ
Для химической реакции:
аА + bB = cC + dD (10)
neq A = neq B = neq C = neq D (11)
Фактор эквивалентности (feq) – это число, обозначающее, какая часть реальной частицы вещества В эквивалента одному иону водорода в данной кислотно – основной реакции или одному электрону в данной реакции окисления – восстановления.
Фактор эквивалентности – безразмерная величина, равная единице или доле единицы, например, 1/2, 1/3, 1/5.
Эквивалент есть 1/z часть частицы вещества. При z = 1 эквивалент идентичен самой частицы. Число z называется числом эквивалентности. Оно показывает, какое число эквивалентов вещества В условно «содержится» в одной формульной единице этого вещества.
Эквивалент быть приписан веществу только тогда, когда оно участвует в конкретной химической реакции. Для одних веществ значение zB меняется от реакции к реакции, для других – остается постоянным. Без указания реакции понятие «эквивалент» не имеет смысла.
Например в реакции:
Cr3+ + 6OH- = [Cr(OH)6] – (12)
Один ион Cr3+ присоединяет шесть ионов OH- (zOH- =1). Значит эквивалентное число Cr3+

Молярная масса эквивалента вещества В (Meq B) в конкретный реакции всегда в zB раз меньше молярной массы этого вещества (МВ):
Meq B = MB/zB [г/моль].
Например, в реакции
H3PO4 +3NaOH = Na3PO4 + 3H2O
одна молекула H3PO4 взаимодействует с тремя ионами OH- (ZOH - = 1). Значит эквивалентное число H3PO4 zH3PO4 = 3, а молярная масса эквивалента
Meq H3PO4 = M H3PO4/ z = 98/3 = 32,7 г/моль.
В случае газообразных веществ используется понятие эквивалентный объем, т.е объем занимаемый эквивалентом данного газа при нормальных условиях (Т = 2730С, Р = 101,3 кПа).
V eq B(r) = VM/zB.
Например, эквивалентный объем кислорода V eq О2(r) = 5,6 л,
эквивалентный объем водорода – V eq Н2(r) = 11,2 л.
Пример 1. При взаимодействии 2,7 г. Алюминия с хлором образовалось 13,35 г хлорида алюминия ALCL3. Найти эквивалентную массу алюминия Meq AL и его эквивалент, если известно, что эквивалентная масса хлора равна 35,5 г/моль.
Решение:
1. По условию задачи на 2,7 г алюминия приходится 13,35 г хлора.
2.Согласно закону эквивалентов
n eq AL = n eq CL
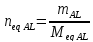 ;
;

Тогда
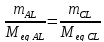
Откуда Meq AL = 2,7*35,5/10,65 = г/моль.
Молярная масса атомов алюминия равна 27 г/ моль. Поскольку эквивалентная масса алюминия (9 г/ моль) в 3 раза меньше мольной массы (27:9=3), то в 1 моле алюминия содержится три его эквивалента. Следовательно, эквивалент алюминия равен 1/3 моля.
Пояснение. Эквивалент элемента выражается в молях. Так в HCL эквивалент хлора zCL = 1 моль. Эквивалентная масса выражается в единицах массы г/моль. Эквивалентная масса хлора Meq CL = 35,5 г/моль.
Пример 2. Определить эквиваленты и эквивалентные массы элементов в соединениях H2S, H2O, PH3.
Решение. В данных соединениях с 1 моль атомов водорода соединяется 1/2 моль атомов серы, 1/2 моль атомов кислорода и 1/3 моль атомов фосфора. Следовательно, эквиваленты серы и кислорода равны 1/2 моля, а эквивалент фосфора равен 1/3 моля. Эквивалентная масса кислорода 8 г/моль, серы 16 г/моль, фосфора 10,3 г/моль.
На основе закона эквивалентов можно рассчитать эквивалентную массу любого из взаимодействующих веществ, а также объем, в случае, если вещество газообразное.
Пример 3. Некоторое количество металла, эквивалентная масса которого равна 34,7 г/моль, вытесняет из кислоты 0,8 л водорода, измеренного при нормальных условиях. Определить массу металла.
Решение. Эквивалентный объем водорода равен 11,2 л/моль, что соответствует 34,7 г металла.
По закону эквивалентов mMe / Meq Me = Vгаз /V eq газ
MMe /34,5 = 0,8/11,2
m Me = 2,48
