
- •Содержание курса химии:
- •Основные понятия и законы химии.
- •Для простых веществ:
- •Масса эквивалента соли
- •Закон Авогадро.
- •Строение вещества.
- •Модель атома вещества по Бору.
- •Квантово механическая модель атома.
- •Основной принцип квантовой механики.
- •Квантовые числа.
- •Распределение электронов в атоме по энергетическим состояниям.
- •Принцип Паули.
- •Энергия ионизации, сродство к электрону и Электроотрицательность.
- •Строение молекул. Химическая связь.
- •Природа и свойства ковалентной связи на примере строения молекул (h2, hCl, h2o).
- •Свойства ковалентной связи:
- •Ионная связь.
- •Влияние природы химической связи на свойства веществ.
- •Металлическая связь, сходство и различие между металлической и ковалентной связями.
- •Основные закономерности протекания химических реакций. Энергетические эффекты химических реакций. Внутренняя энергия и энтальпия. Стандартная энтальпия образования вещества.
- •Основные понятия и законы в термодинамике.
- •Стандартное состояние.
- •Термохимические законы и расчёты по ним:
- •Закон Гесса.
- •2. Закон Лавуазье-Лапласа.
- •Направленность химических реакций.
- •Кинетика химических реакций. Основные понятия химической кинетики.
- •Скорость реакции.
- •Смещение равновесий.
- •Особенности кинетики гетерогенных реакций.
- •Дисперсные системы.
- •Растворы.
- •Законы Рауля.
- •Энергетические эффекты при растворении.
- •Электролитическая диссоциация.
- •На практике оказывается, что
- •Электролитическая диссоциация. Степень диссоциации - отношение числа молекул распавшихся на ионы (n) к общему числу растворенных молекул (n).
- •Сильные электролиты.
- •Кислоты, основания, соли с точки зрения теории электрической диссоциации.
- •Слабые электролиты.
- •Ионное произведение воды. Водородный показатель.
- •Гидролиз солей.
- •Окислительно-восстановительные реакции.
- •Электрохимия.
- •Возникновение скачка потенциала на границе электрод-электролит.
- •Гальванические элементы.
- •Химические источники тока.
- •Стаканчиковый
- •Аккумуляторы.
- •Ряд напряжений металлов.
- •Измерение электродных потенциалов. Ряд стандартных электродных потенциалов, водородный электрод.
- •Электролиз расплавов и растворов электролитов.
- •Явление поляризации при электролизе. Природа этого явления.
- •Последовательность разрядки ионов при электролизе на катоде.
- •Электролиз водных растворов электролитов.
- •Законы Фарадея.
- •Коррозия металла.
- •Защита металлов от коррозии.
Гальванические элементы.
Рассмотрим гальванический элемент Даниэля- Якоби.
Элемент Даниэля–Якоби
1 – сифоновая трубка, как правило заполненная KCl
![]() Потенциал,
определяющий равновесие:
Потенциал,
определяющий равновесие:

При замыкании цепи цинковая пластина начинает терять электроны. Тогда появляется возможность для переходов катиона цинка из пластины в электроны. Электрод, который имеет меньший потенциал (Zn) в гальваническом элементе является анодом, при замыкании цепи потенциал, измеряющий равновесие перемещается в сторону окисления металла. Анодный процесс:
![]()
Цинковая
пластина растворяется (![]() )
медная пластина наращивается. Работает,
пока цинковая пластина не растворится
)
медная пластина наращивается. Работает,
пока цинковая пластина не растворится
![]() .
.
Гальванический элемент (химический источник тока) – устройство, в котором химическая энергия окислительно-восстановительных реакций преобразуется в электрическую энергию.
В гальваническом элементе процессы окисления и восстановления пространственно разделены. За счет чего становится возможным движение зарядов электронов во внешней цепи, а ионов во внутренней цепи.
![]()
![]() -электролитическая
сила гальванического элемента
-электролитическая
сила гальванического элемента
![]()
Электронная схема гальванического элемента начинается для электрона с меньшего потенциала, то есть с анода.
Z n0/Zn2+//Cu2+/Cu0
n0/Zn2+//Cu2+/Cu0
Возрастает
![]()
Химические источники тока.
Химические источники тока – это устройства, используемые в быту и технике для получения электрической энергии за счет химических реакций. Их достоинство иметь источник энергии, не имея доступа к центральному источнику электрической энергии.
1. Марганцево-цинковые элементы (сухие элементы) бывают стаканчиковые, пуговичные, галетные (кубические).
Действие элемента основано на реакции:
![]()
Работа марганцево-цинкового элемента протекает следующим образом:
Цинковый стаканчик – анод – растворяется:
![]()
электролит – паста из NH4Cl – взаимодействует с ионами Zn2+:
![]() Электроны
от цинка по внешней цепи идут к катоду,
изготовленному из пакета MnO2,
и сюда же приходят ионы H+
по внутренней цепи:
Электроны
от цинка по внешней цепи идут к катоду,
изготовленному из пакета MnO2,
и сюда же приходят ионы H+
по внутренней цепи:
![]()
Водород не выделяется, так как MnO2 очень хороший деполяризатор.
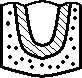
Стаканчиковый
-
2
3
4

1
Цинковый стаканчик -
Угольный стержень
-
Материал пропитанный пастой из MnO2
-
Электролит NH4Cl
При разомкнутой цепи на электродах равновесие следующее
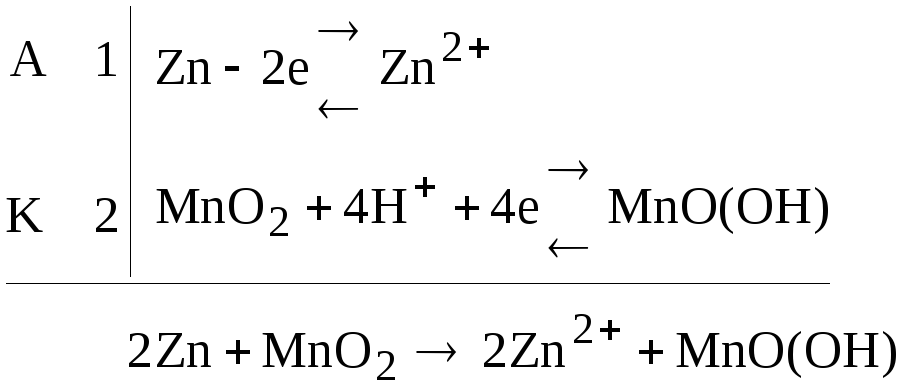
Катионы цинка связываются электролитом

Галетный. Отличие: отсутствует угольный электрод, что позволяет монтировать батареи значительно компактнее.

1-биполярный проводящий слой;
2-цинковый электрод;
3-хлорвиниловый корпус;
4-паста-электролит;
5-бумажная прокладка;
6-положительный электрод (MnO2);
Пуговичный. Отличие: самый компактный и упрощённый вид батареи.
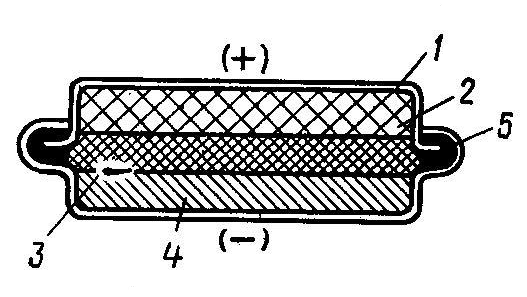
1-оболочка из металла;
2-положительный электрод (MnO2);
3-сепаратор с щелочным электролитом;
4-цинковый электрод;
5-изолятор
Аккумуляторы.
Аккумуляторы – это системы позволяющие накапливать заряды, поддерживать разность потенциалов и восстанавливать возможность дальнейшей работы в качестве источников тока за счет обратимости электродных процессов при использовании внешних источников энергии.
Свинцово-кислотный аккумулятор. Основы и сущность процессов протекающих на электродах при его работе, применение.
Свинцово-кислотный
аккумулятор основан на
окислительно-восстановительной реакции
![]()
Свинцово-кислотный аккумулятор состоит из решётчатых свинцовых пластин, поры в решётках заполнены. В одной – губчатый свинец (Pb), в другой решётке паста из оксида свинца (PbO2). Пластины погружены в электролит H3SO4 (ρ=1,23г/см3,ω(H3SO4)=35,4%)
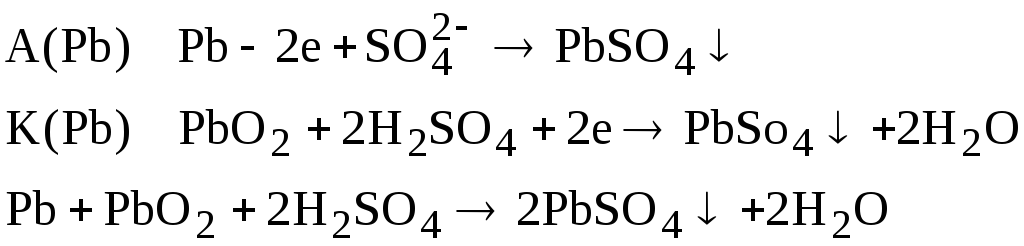
Путем присоединения к внешнему источнику постоянного тока, то можно осуществить обратный процесс.
![]()
![]()
Электрохимическая связь.
Pb/PbSO4//H2SO4//PbSO4/PbO2
Преимущество свинцового аккумулятора – большая электрическая ёмкость, устойчивость в работе, большое количество циклов (разрядка-зарядка).
Недостатки – агрессивность электролита, токсичность свинца, высокая масса, большие габариты.
Применение: наиболее широко применяется в технике. Он служит источником тока для стартёров двигателей внутреннего сгорания, для аварийного освещения и других целей.
