
- •1. Основные понятия теории растворов электролитов
- •2. Теория с Аррениуса/
- •3. Равновесие электролитической диссоциации в растворе
- •4. Ионное произведение воды
- •5. Водородный показатель. Расчет рН растворов кислот и оснований
- •1. Классификация кислотно-основных буферных систем:
- •Механизм действия буферных систем и расчетные формулы для определения рН в этих растворах
- •Вычисление рН буферных растворов Уравнение Гендерсона -Хассельбаха
- •2. Отсюда находим:
- •4. Буферная емкость. Факторы, определяющие буферную емкость
-
Механизм действия буферных систем и расчетные формулы для определения рН в этих растворах
Для объяснения механизм поддержания рН на одном уровне воспользуемся ацетатным буферным раствором (CH3COONa– как сильный электролит в водном растворе распадается на ионы нацело и СНзСООН –как слабый электролит – лишь частично). В такой смеси протекают следующие реакции
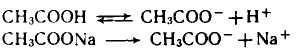
Первая из реакций оказывается почти полностью подавленной из-за большой концентрации ацетат-ионов, вызванной диссоциацией сильного электролита — ацетата натрия.
А) Если к такому раствору добавить сильную кислоту, то ионы водорода будут взаимодействовать с анионами с образованием молекул СНзСООН и реакция среды не измениться, т.е. рН≈const.
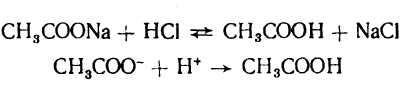
Б) Если к раствору добавлять сильное основание, то гидроксид-ионы будут взаимодействовать с ионами водорода (или с молекулами СН3СООН), хоть и в небольшом количестве, но содержащимися в растворе. Образование воды не влияет на реакцию среды. Пошедшие на реакцию с ОН- ионы водорода будут компенсированы за счет смещения равновесия реакции диссоциации СН3СООН вправо.
![]() рН≈const.
рН≈const.
Для системы аммиачной буферной системы NH3/NH4+ (самостоятельно на практике);
-
Вычисление рН буферных растворов Уравнение Гендерсона -Хассельбаха
1) Аналитическое выражение для расчета рН буферного раствора, например, ацетатного буфера можно получить из уравнения для константы диссоциации (к реакциям диссоциации применим закон действующих масс).
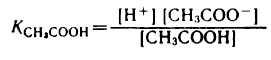 ,
,
разрешив его относительно концентрации ионов водорода [H+] можно написать:
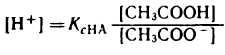
Уксусная кислота присутствует в растворе в смеси с CH3COONa в виде неионизированных молекул. Поэтому концентрацию молекул можно принять равной общей молярной концентрации кислоты в растворе, т. е. [СН3СООН] = Скисл. Концентрацию анионов уксусной кислоты можно принять равной концентрации соли, т. е. [СН3СОО-] = Ссоли, так как CH3COONa— сильный электролит, диссоциирующий в растворе на 100%. Приняв эти упрощения, получим:
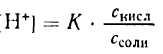
2. Логарифмируя полученное уравнение и заменяя знаки логарифмов на обратные, получаем:
![]()
но – Ig [Н+] есть рН, а – Ig К есть рК — силовой показатель кислоты.
С учетом этого получим:
![]() Это уравнение
называют уравнением буферного раствора
(или уравнением Гендерсона-Гассельбаха).
Это уравнение
называют уравнением буферного раствора
(или уравнением Гендерсона-Гассельбаха).
Если при приготовлении буферной системы взять одинаковые концентрации кислоты и соли, то концентрация ионов водорода в таком растворе будет равна константе ионизации кислоты, так как отношение Скис/Ссоли = 1 и [Н+]=К1, т.е. [Н+]=К, поэтому рН=рК.
Аналогично для систем NH4OH + NH4C1получают выражения:
1. Запишем уравнение константы ионизации NH4OH и найдем [ОН-]:
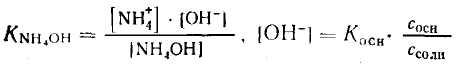
2. Отсюда находим:
![]()
Зная, что рН + рОН = 14, получим:
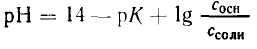
Задача 1. Сколько 0,5 М раствора CH3COONa нужно прибавить к 100 мл 2М раствора СН3СООН, чтобы получить буферный раствор с рН=4?
Решение:
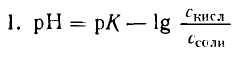
Откуда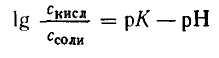
Подставляем числовые данные и получаем:
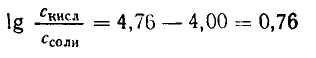
Число Ig 0,76 = 5,754. Следовательно, отношение концентрации кислоты к концентрации соли должно быть равно 5,754 : 1.
2. Находим концентрацию кислоты в буферной системе:
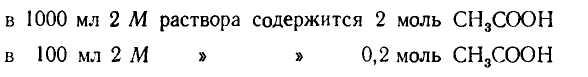
-
Зная концентрацию кислоты, находим концентрацию солив буферной системе; она должна быть равна 0,2:5,754= 0,03475 (моль).
-
Находим количество 0,5 М раствора ацетата натрия, содержащего 0,03475 моль:
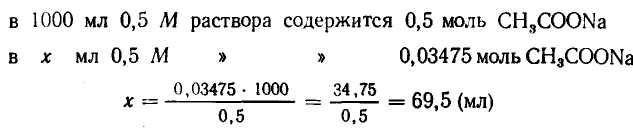
Задача 2. Вычислить рН аммиачной буферной системы, содержащей по 0,5 М NH4ОН и NH4C1. Как изменится рН при добавлении к 1 л этой смеси 0,1 М НС1 и при добавлении к 1 л этой смеси 0,1 М NaOH и при разбавлении раствора водой в 10 раз, если рК (NH4ОН) =4,75?
