
- •Київський національний університет імені тараса шевченка
- •Протокол № засідання кафедри
- •Вплив антибіотиків групи цефалоспоринів на оксидантно-антиоксидантну систему слизової оболонки товстої кишки щурів.
- •3.7.1. Визначення дієнових кон’югатів ненасичених жирних кислот..19
- •Список скорочень
- •Моніторинг клінічного стану щурів на фоні 5-ти добового та 14-ти добового введення цефтріаксону.
- •Дослідження активності сод в слизовій оболонці тк щурів після 5-ти та 14-ти добового введення цефтріаксону.
- •1.2 Класифікація цефалоспоринів
- •1.3 Біологічна активность цефтріаксону
- •Антибіотик асоційована діарея та механізми її розвитку
- •Експериментальна частина розділ 3 матеріали та методи досліджень
- •3.1. Матеріали
- •3.2. Лабораторні тварини
- •3.3. Схема проведення експерименту
- •3.4. Моніторинг клінічних параметрів стану щурів
- •3.5. Отримання гомогенату слизової оболонки
- •3.6. Визначення концентрації протеїнів методом Лоурі
- •3.7.1. Визначення дієнових кон’югатів ненасичених жирних кислот
- •3.7.2. Визначення вмісту тбк-активних продуктів
- •3.7.3. Визначення активності каталази.
- •3.7.4. Визначення активності сод
- •3.8. Статистична обробка даних
- •Розділ 4 результати досліджень та їх обговорення
- •4.1.Моніторинг клінічного стану щурів на фоні 5-ти добового та 14-ти добового введення цефтріаксону
- •4.2. Дослідження активності сод в слизовій оболонці товстої кишки щурів після 5-ти та 14-ти добового введення цефтріаксону
- •4.2. Дослідження активності каталази
- •4.4. Дослідження вмісту дієнових кон'югатів
- •4.3. Дослідження вмісту мда
- •Висновки
- •Список використаних джерел
-
Моніторинг клінічного стану щурів на фоні 5-ти добового та 14-ти добового введення цефтріаксону.
-
Дослідження активності сод в слизовій оболонці тк щурів після 5-ти та 14-ти добового введення цефтріаксону.
-
Дослідження активності каталази в слизовій оболонці ТК щурів після 5-ти та 14-ти добового введення цефтріаксону.
-
Дослідження вмісту МДА в слизовій оболонці ТК щурів після 5-ти та 14-ти добового введення цефтріаксону.
-
Дослідження вмісту дієнових кон'югатів в слизовій оболонці ТК щурів після 5-ти та 14-ти добового введення цефтріаксону.
ОГЛЯД ЛІТЕРАТУРИ
РОЗДІЛ 1
АНТИБІОТИКИ ЦЕФАЛОСПОРИНОВОГО РЯДУ
1.1. Загальні відомості та представники
Створення і впровадження в клінічну практику антибіотиків класу цефалоспоринів є, безумовно, однією з найважливіших подій в історії хіміотерапії бактеріальних інфекцій. На даний час, очевидно, що за спектром антибактеріальної дії, фармакокінетики, безпеки та ін., цефалоспорини перевершують антибіотики багатьох інших класів, чим і пояснюється їх статус найбільш широко вживаних антибіотиків антибактеріальної дії в багатьох країнах світу.
Народження цефалоспоринів справедливо пов'язують з роботами G. Brotzu, що передбачив на початку 40-х років, що періодичне самоочищення стічних вод в Сардінії може бути обумовлене активністю особливих мікроорганізмів, що пригнічують ріст бактеріальної флори. У 1945 р. йому вдалося виділити гриб Cephalosporium acremonium (пізніше названий Acremonium chrysogenum), що володіє вираженою антибактеріальною активністю по відношенню до грам-позитивних і грам-негативних мікроорганізмів.
Наступним етапом було детальне вивчення С. acremonium робочими групами H. Florey і E.P. Аbraham (з 1955 по 1962 р.). З продуктів обміну речовин цього гриба вдалося виділити бактерицидну субстанцію - цефалоспорин С, що стала вихідною речовиною для синтезу 7-аміноцефалоспоринової кислоти - структурної основи цефалоспоринів [4].
У 1962 р. в клінічну практику був введений перший антибіотик класу цефалоспоринів - цефалорідин, проте широка клінічна практика цефалоспоринів почалася лише в кінці 70-х років. В даний час налічується більше 50 антибіотиків цефалоспоринового ряду.

Рис.1.1. "Дерево" цефалоспоринів
 Цефалоспорини
представляють собою біциклічні з'єднання,
що складаються з бета-лактамного і
дигідротіазинового кілець. Обидва
кільця входять до складу 7-аміноцефалоспоранової
кислоти (7-АЦК) - загальне ядро молекули
цефалоспоринів. При цьому модифікація
хімічної структури 7-АЦК супроводжується
істотними змінами властивостей
(антибактеріальної активності, параметрів
фармакокінетики та ін.) (рис. 1.2.).
Цефалоспорини
представляють собою біциклічні з'єднання,
що складаються з бета-лактамного і
дигідротіазинового кілець. Обидва
кільця входять до складу 7-аміноцефалоспоранової
кислоти (7-АЦК) - загальне ядро молекули
цефалоспоринів. При цьому модифікація
хімічної структури 7-АЦК супроводжується
істотними змінами властивостей
(антибактеріальної активності, параметрів
фармакокінетики та ін.) (рис. 1.2.).
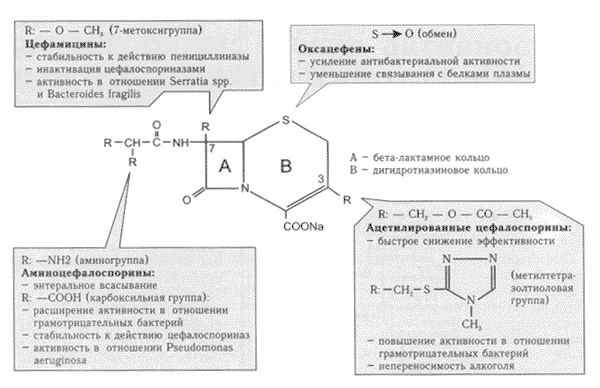
Рис.1.2. Цефалоспорини: зв'язок між хімічною структурою і ефектом
Антибактеріальна активність цефалоспоринів, як і інших бета-лактамних антибіотиків, принаймні частково, обумовлена гальмуванням синтезу пептидоглікану - структурної основи мікробної стінки. Пептидоглікани є довгими полісахаридними ланцюгами зі своєрідною сітчастою просторовою конформацією, в яких чергуються залишки N-ацетилглюкозаміна (NAG) і N-ацетилмурамінової кислоти (NAM). NAG- і NАМ-пентапептидні залишки пептидогліканів що синтезуються в цитоплазмі мікробної клітини і транспортуються через цитоплазматичну мембрану. Далі ці залишки вбудовуються в існуючу пептидогліканову мережу (в процесі росту і ділення клітини) за участю різних ензимів - транспептидаз, карбоксипептидази, ендопептидаз. Власне ці ензими, що знаходяться в цитоплазматичній мембрані, є місцем реалізації антибактеріальної активності (мішенями) бета-лактамних антибіотиків, у тому числі цефалоспоринів; вони отримали назву пеніцилін зв'язувальні протеїни (penicillin-binding proteins - РВР). В результаті утворення "тривалого" ковалентного зв'язку бета-лактамного антибіотика і РВР останні інактивуються. При цьому ефект бета-лактамного антибіотика, що призначається, залежить від того, які РВР інактивуються і яку роль вони відіграють в синтезі пептидогліканів і виживанні мікробної клітини. Важливо також підкреслити, що бактерицидний ефект цефалоспоринів реалізується лише в процесі росту і розмноження мікроорганізмів, тоді як клітини у стані "спокою" невразливі для дії антибіотиків [4, 5].
