
- •10. Електрохімічні процеси
- •10.1 Електродний потенціал, класифікація електродів.
- •10.2 Гальванічні елементи. Приклади розв’язання типових задач
- •10.3. Електрохімічна корозія металів і сплавів. Приклади розв’язання типових задач
- •10.4. Електроліз. Приклади розв’язання типових задач
- •Має бути мінімальним, має бути максимальним
- •Cередовище стає лужним.
- •Кількісні розрахунки по електролізу потрібно виконувати згідно з законом Фарадея:
- •10.5. Запитання для самоконтролю
10.2 Гальванічні елементи. Приклади розв’язання типових задач
Нагадаємо,
що гальванічний
елемент
– це технічний пристрій, в якому енергія
окисно-відновної реакції безпосередньо
перетворюється в електричну за рахунок
розподілення у просторі процесів
окислення (анод) і відновлення (катод).
Необхідно пом’ятати,
що
 >
>
 .
Електрорушійна
сила
гальванічного елементу ( ЕРС або просто
Е) розраховується як:
.
Електрорушійна
сила
гальванічного елементу ( ЕРС або просто
Е) розраховується як:
ЕРС
=
 -
-
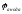 .
.
Вона також вимірювається у Вольтах і має додатне значення.
ЕРС можна також розрахувати згідно термодинамічних даних:
ΔGхім.реакції = -nFE
Задача. 1. Складіть схему гальванічного елементу, утвореного пластинками цинку і феруму, зануреними у розчини солей цих металів з концентраціями відповідно 0,01 і 0,1 моль-іонів/л. Запишіть рівняння електродних реакцій і сумарної струмо-утворюючей реакції. Розрахуйте стандартне значення ЕРС гальванічного елементу двома способами і ЕРС при даних концентраціях солей металів.
Розв’язання: Для визначення аноду і катоду в більшості випадків достатньо скористатись значеннями стандартних електродних потенціалів (табл.., додаток):

 =
- 0,76,B
<
=
- 0,76,B
<
 = - 0,44,B;
тому анодом буде цинк:
= - 0,44,B;
тому анодом буде цинк:
А(-):
Zn - 2e
= Zn
- 2e
= Zn .
.
Це є рівняння анодного процесу. Анод негативно заряджений відносно зовнішньої електричної цепі.
К(+):
Fe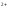 + 2e
= Fe
+ 2e
= Fe
Це є рівняння катодного процесу. Катод позитивно заряджений відносно зовнішньої електричної цепі. Якщо скласти обидва рівняння, то одержимо рівняння сумарної струмо-утворюючей реакції в іонно-молекулярному вигляді:
Zn +
Fe
+
Fe = Zn
= Zn + Fe
+ Fe ,
або
,
або
Zn + FeSO
+ FeSO = ZnSO
= ZnSO + Fe
у молекулярному вигляді.
+ Fe
у молекулярному вигляді.
Схема гальванічного елементу записується як:
Zn |Zn
|Zn ||
Fe
||
Fe |Fe
|Fe .
.
Вертикальної рисою позначають межу поділу між електродом та електролітом, двома рисами – межу поділу між електролітами (пориста електропроводяща перегородка).
Розрахуємо значення потенціалів аноду і катоду згідно з рівнянням Нернста:
 =
-0,76 +
=
-0,76 +
 = - 0,76 +
= - 0,76 +

 -0,82 (В),
-0,82 (В),
 =
-0,44 +
=
-0,44 +

 -0,47 (В).
-0,47 (В).
Тоді ЕРС =
 -
-
 = -0,47 - (-0,82) = + 0,35 (В).
= -0,47 - (-0,82) = + 0,35 (В).
Задача 2. Складіть схеми двох гальванічних елементів, в одному з яких нікель негативно заряджений відносно зовнішнього кола, а в іншому позитивно. Запишіть рівняння електродних процесів і сумарних струмо-утворюючих реакцій. Розрахуйте значення стандартних електрорушійних сил цих елементів.
Розв’язання:
Якщо
нікель є негативно зарядженим електродом
відносно зовнішнього кола, то він виконує
роль анода в гальванічному елементі, і
його потенціал має бути меншим ніж
катода ( = -0,25 В). Тому можна в якості катода взяти,
наприклад, станум (
= -0,25 В). Тому можна в якості катода взяти,
наприклад, станум (
 = -0,14 В
). Запишемо схему
гальванічного
елементу , рівняння електродних реакцій,
та рівняння струмо-утворюючей реакції:
= -0,14 В
). Запишемо схему
гальванічного
елементу , рівняння електродних реакцій,
та рівняння струмо-утворюючей реакції:
Ni|Ni2+||Sn2+|Sn або Ni|NiSO4||SnSO4|Sn
A(-): Ni0 - 2e = Ni2+
K(+): Sn2+ + 2e = Sn0
Ni0 + Sn2+ = Ni2+ + Sn або Ni + SnSO4 = NiSO4 + Sn
Так
як ЕРС =
 -
-
 , то стандартне значення ЕРС буде
рівнятись:
, то стандартне значення ЕРС буде
рівнятись:
ЕРС0 = -0,14 - (-0,25) = 0,11 (В).
Якщо
нікель є позитивно зарядженим електродом
відносно зовнішнього кола, то він виконує
роль катода в гальванічному елементі,
і його потенціал має бути більшим ніж
анода.
Тому можна в якості анода взяти, наприклад,
цинк (
 = -0,76 В
). Запишемо схему гальванічного елементу
, рівняння електродних реакцій, та
рівняння струмоутворюючей реакції:
= -0,76 В
). Запишемо схему гальванічного елементу
, рівняння електродних реакцій, та
рівняння струмоутворюючей реакції:
Zn|Zn2+||Ni2+|Ni або Zn|ZnSO4||NiSO4|Ni
A(-): Zn0 - 2e = Zn2+
K(+): Ni2+ + 2e = Ni0
Zn0 + Ni2+ = Zn2+ + Ni або Zn + NiSO4 = ZnSO4 + Ni
Так
як ЕРС =
 -
-
 , то стандартне значення ЕРС буде
рівнятись:
, то стандартне значення ЕРС буде
рівнятись:
 =
-0,25
- (-0,76)
= 0,51
(В).
=
-0,25
- (-0,76)
= 0,51
(В).
Задача 3. Складіть схему гальванічного елемента, утвореного водневим електродом зі значенням рН = 4(а) і рН = 7(б) та електродом, виконаним з метала – магній (а) та мідь (б), зануреного в розчин солі цього ж металу з концентрацією- (а)[Mg2+] = 0,1 моль/л та (б) [Cu2+] = 1 моль/л. Запишіть рівняння електродних процесів, сумарної струмо-утворюючої хімічної реакції. Розрахуйте величину електрорушійної сили кожного гальванічного елемента. Розв’язання: Перш за все розрахуємо значення електродних потенціалів згідно з рівнянням Нернста (10.2 та 10.3):
 =
-2,27 +
=
-2,27 +
 1x10-1
= -2.27 +
1x10-1
= -2.27 +
 (-1)
= -2,30 (B)
(-1)
= -2,30 (B)
 =
+0,34 +
=
+0,34 +
 1
= +0,34 (B)
1
= +0,34 (B)
а)

 = - 0,059 pH
= -0,059x4
= - 0,059 pH
= -0,059x4
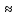 -0,24 (B)
-0,24 (B)
б
)

 = - 0,059 pH
= -0,059x7
= - 0,059 pH
= -0,059x7
 - 0,41 (B)
- 0,41 (B)
В
випадку а
водневий електрод виконує роль катода
( -0,24
 -2,30), а в випадку б
- він є анодом ( -0,41
-2,30), а в випадку б
- він є анодом ( -0,41
 + 0,34 ). Тоді схеми гальванічних елементів,
рівняння електродних процесів і
струмо-утворюючих реакцій будуть
виглядати: а) Mg|Mg2+||H+|H2(адсорб.)Pt
або Mg|MgSO4||H2SO4|H2(адсорб.)Pt
+ 0,34 ). Тоді схеми гальванічних елементів,
рівняння електродних процесів і
струмо-утворюючих реакцій будуть
виглядати: а) Mg|Mg2+||H+|H2(адсорб.)Pt
або Mg|MgSO4||H2SO4|H2(адсорб.)Pt
A(-): Mg0 - 2e = Mg2+
K(+): 2H+ + 2e = H20
Mg + 2H+ = Mg2+ + H2 або Mg + H2SO4 = MgSO4 + H2
ЕРС
=

 -
-
 = -0,24 - (-2,30) = +2,06 (В).
= -0,24 - (-2,30) = +2,06 (В).
б) Pt,H2(адсорб.)|H2O ||Cu2+|Cu або Pt,H2(адсорб.)|H2O ||CuSO4|Cu
A(-): H20 - 2e = 2H+
K(+): Cu2+ + 2e = Cu0
H2 + Cu2+ = 2H+ + Cu або H2 + CuSO4 = H2SO4 + Cu
ЕРС
=
 -
-

 =
0,34
- (-0,41) = 0,75 (В)
=
0,34
- (-0,41) = 0,75 (В)
Задача 4. ЕРС гальванічного елементу, утвореного з алюмінієвої пластинки, зануреної в розчин солі алюмінію з концентрацією 0,003 моль/л, і платинової пластинки, насиченої воднем і зануреної в розчин хлоридної кислоти, дорівнює 1,48 В. Складіть схему гальванічного елемента, запишіть рівняння електродних процесів та сумарної струмо-утворюючої хімічної реакції. Визначте концентрацію хлоридної кислоти в розчині.
Розв’язання: Розрахуємо потенціал алюмінієвого електроду:
 =
-1,66 +
=
-1,66 +
 =-1,66+
=-1,66+
 =-1,66
+ (-0,05) = - 1,71 (B).
=-1,66
+ (-0,05) = - 1,71 (B).
Тоді потенціал водневого електроду буде:
 =
E +
=
E +
 = 1,48 + (-1,71) = -0,23 (B).
= 1,48 + (-1,71) = -0,23 (B).
Рахуємо концентрацію іонів гідрогену:
lg =
=
 /0,059
= -
/0,059
= -

 - 3,90 (B),
- 3,90 (B),
[H+] = 1x10-3,90 = 1,26x10-4 (моль-іонів/л).
Так як, хлорідна кислота – сильний електроліт (α = 1), то її концентрація також дорівнює 1,26x10-4 (моль-іонів/л).
Задача 5. Складіть схему гальванічного елемента, в основі якого лежить реакція, що перебігає за наведеним рівнянням. Напишіть електродні рівняння анодного та катодного процесів. Розрахуйте ЕРС цього елемента, знаючи концентрації солей металів: Mg + FeSO4 = MgSO4 + Fe; [Mg2+] = 0,1 моль/л, [Fe2+] = 0,1 моль/л.
Розв’язання: З рівняння струмоутворюючей реакції бачимо, що окислюється магній (анод), а відновлюється ферум (катод). Запишемо рівняння електродних реакцій , потенціали електродів та ЕРС елемента:
А(-): Mg0 - 2e = Mg2+
К(+): Fe2+ + 2e = Fe0
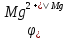 =
- 2,27 +
=
- 2,27 +
 1x10-1
= -2,27 + (-0,03) = -2,30 (B),
1x10-1
= -2,27 + (-0,03) = -2,30 (B),
 =
-0,44 +
=
-0,44 +
 1x10-1
= -0,44 + (-0,03) = -0,47 (B).
1x10-1
= -0,44 + (-0,03) = -0,47 (B).
ЕРС
=
 -
-
 =
-0,47 - (-2,30) = 1,83 (В).
=
-0,47 - (-2,30) = 1,83 (В).
Задача 6. З чотирьох наведених нижче металів виберіть ті пари, які дають найбільшу та найменшу стандартну ЕРС складеного з них гальванічного елемента. Для будь-якого з них складіть схему, запишіть рівняння електродних процесів і сумарної струмо-утворюючої хімічної реакції. Розрахуйте ЕРС цього гальванічного елемента, якщо концентрації солей металів для анода і катода дорівнюють 0,01 і 0,1 моль/л відповідно: Ag, Cu, Al i Sn.
Розв’язання: Згідно даних таблиці №…. найбільша різниця стандартних значень електродних потенціалів буде для пари срібло і алюміній (ЕРС0 = 0,80 – (-1,66) = 2,44), а найменша – срібло і мідь ( ЕРС0 = 0,80 – 0,34 = 0,46). Характеризуємо, наприклад, перший з цих елементів:
схема срібло-алюмінієвого елемента – Al|Al3+||Ag+|Ag,
рівняння
електродних процесів - К(-): Al0
- 3e
= Al3+ x1

A(+): Ag+ + e = Ag0 x3
Al + 3Ag+ = Al3+ + 3Ag – рівняння струмо-утворюючей реакції.
Рахуємо потенціали анода і катода при даних концентраціях солей алюмінія і срібла:
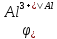 =
-1,66 +
=
-1,66 +
 lg1x10-2
= -1,66 +
lg1x10-2
= -1,66 +
 (-2)
= -1,70 (B)
(-2)
= -1,70 (B)
 =
+0,80 +
=
+0,80 +
 lg1x10-1
= +0,80 + 0,059(-1) = + 0,74 (B)
lg1x10-1
= +0,80 + 0,059(-1) = + 0,74 (B)
Тоді ЕРС = 0,74 - (-1,70) = 2,44 (В).
Задача 7. Який гальванічний елемент називають концентраційним? Складіть схему, напишіть рівняння електродних процесів і розрахуйте ЕРС гальванічного елемента, що утворений із срібних електродів, занурених у розчини AgNO3 з концентраціями 0,01 і 0,1 моль/л.
Розв’язання: В концентраційному гальванічному елементі електродами є одна й таж окислювально-відновна система але з різними значеннями концентрацій потенціал-утворюючих іонів. У анода ця величина менша. Тому схема елемента в цьому випадку буде такою:
Ag|Ag+(0,01)||Ag+(0,1)|Ag .
В дужках вказані концентрації розчинів. В загальному випадку ЕРС концентраційного елементу з металічних електродів розраховується як:
EPC
= -
- =
= +
+
 катода
-
катода
-
 -
-
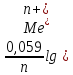 анода
або
ЕРС =
анода
або
ЕРС =
 (10.4)
(10.4)
Задача 8. Для реакції, що наведена в розділі 9.3 в якості приклада розстановки коефіцієнтів:
2KMn+7O4 + 10 KI-1 + 8 H2SO4 = 2 Mn+2SO4 + 5 I20 + 6 K2SO4 + 8 H2O,
визначте напрямок її перебігу, використовуючи значення стандартних потенціалів окисника та відновника. Запишіть рівняння анодного і катодного процесів, схему відповідного окисно-відновного гальванічного елементу. Розрахуйте стандартну електрорушійну силу цього гальванічного елементу.
Розв’язання: Для перебігу реакції зліва направо (у прямому напрямку) потрібно, щоб окисно-відновний потенціал окисника був би більшим ніж відновника, а з точки зору електрохімічних процесів – електродний потенціал катоду має бути більшим ніж аноду. В нашому випадку маємо:
Mn+7 + 5e = Mn+2 (окисник відновлюється) - катод
2I-1 - 2e = I20 (відновник окислюється) – анод
Згідно
даних таблиці ….
 = +1,51B
;
= +1,51B
;
 = +0,53B.
= +0,53B.
Тобто, маємо, що потенціал катоду більший ніж у анода. Тож реакція перебігає зліва направо. Тепер схема окисно-відновного елементу буде в іонно-молекулярному та молекулярному вигляді відповідно як:
(-)Pt|I2|I-
|| ,
Mn2+|Pt(+)
,
Mn2+|Pt(+)
(-)Pt|I2|KI ||KMnO4, MnSO4|Pt(+) ,
а рівняння анодного та катодного процесів співпадають з вже приведеними вище.
