
- •Раздел 2. Устойчивость макроскопических систем к флуктуациям в равновесном состоянии, процессы релаксации, фазовые переходы и критические явления.
- •2. 1. Термодинамические условия устойчивости систем к флуктуациям
- •2. 2.Термодинамическое описание релаксационных процессов.
- •2.3. Потеря устойчивости макроскопических систем при отклонениях от равновесного состояния, фазовые переходы и критические явления.
2.3. Потеря устойчивости макроскопических систем при отклонениях от равновесного состояния, фазовые переходы и критические явления.
Из
предыдущего раздела следует, что любая
материальная система в заданном фазовом
состоянии при сравнительно малом
отклонении от равновесия вследствие
изменения независимых переменных
(температуры, давления, числа молей
компонентов, в том числе вследствие
химических превращений) или воздействия
внешних силовых полей, сохраняет
устойчивость к флуктуациям или внешним
возмущениям и релаксирует в равновесное
термодинамически стабильное состояние,
соответствующее измененным параметрам,
вследстаие эффекта Ле Шателье - протекания
самопроизвольных процессов, уменьшающих
внешнее воздействие. Если при достижении
определенных независимых параметров
(температуры, давления, состава) фазовое
состояние системы становится
термодинамически неравновесным, а
равновесным является другое фазовое
состояние, то ее переход в новое
равновесное фазовое состояние является
фазовым переходом, связанным с потерей
устойчивости системы к внешним или
внутренним (локальным, микроскопическим)
возмущениям (флуктуациям). Теоретически
этот переход соответствует определенной
точке (температуре, давлению или составу
системы), в которой зависимости
термодинамических потенциалов обоих
фазовых состояний от этих параметров
пересекаются, т.ее. их разность равна
нулю. Очевидно, что условия потери
устойчивости однородной (гомогенной)
фазы к флуктуациям должны быть
противоположными условиям ее устойчивости
к ним. Соответственно,
наиболее общий критерий нестабильности
гомогенной фазы, в противоположность
предложенному Гиббсом общему критерию
стабильности гомогенной фазы, можно
сформулировать так: если энергетическое
выражение фундаментального
термодинамического уравнения в
интегральной форме
![]() при
определенных значениях интенсивных
параметров Т, р,
при
определенных значениях интенсивных
параметров Т, р,
![]() для какой-либо фазы не равно нулю, а для
любой другой фазы, образованной из тех
же компонентов, при тех же условиях
будет равно нулю, то рассматриваемая
фаза по отношению к распаду на другие
фазы является термодинамически
неустойчивой к флуктуациям или внешним
возмущениям. В
соответствие с энергетической теорией
устойчивости Гиббса-Дюгема гомогенная
система становится неустойчивой к
флуктуациям, если их возникновение и
рост становится энергетически выгодным
(ΔфF<0
и ΔфG<0).
При этом в случае гомогенных материальных
систем возможны два варианта потери
устойчивости и, соответственно, два
типа фазовых переходов:
для какой-либо фазы не равно нулю, а для
любой другой фазы, образованной из тех
же компонентов, при тех же условиях
будет равно нулю, то рассматриваемая
фаза по отношению к распаду на другие
фазы является термодинамически
неустойчивой к флуктуациям или внешним
возмущениям. В
соответствие с энергетической теорией
устойчивости Гиббса-Дюгема гомогенная
система становится неустойчивой к
флуктуациям, если их возникновение и
рост становится энергетически выгодным
(ΔфF<0
и ΔфG<0).
При этом в случае гомогенных материальных
систем возможны два варианта потери
устойчивости и, соответственно, два
типа фазовых переходов:
- при небольшом отклонении параметров состояния от их значений, соответствующих точке перехода, система может оставаться устойчивой к малым флуктуациям, что соответствует так называемому метастабильному состоянию, и быть неустойчивой к большим (сверхкритическим) флуктуациям объема (плотности) или состава (концентрации), переходя в новое фазовое состояние через образование и термодинамически выгодный устойчивый рост таких флуктуаций (зародышей новой фазы): ΔфF<0 и ΔфG<0 и претерпевать так называемый фазовый переход 1-го рода;
- при большом отклонении параметров состояния от их значений, соответствующих точке перехода и при условии, что фазовый переход 1-го рода невозможен из-за геометрических (стерических) или кинетических ограничений, могут достигаться условия термодинамически выгодного роста любых флуктуаций и происходить переход системы в новое состояние через рост любых флуктуаций, т.е. через непрерывное перерождение первоначальной состояния - критический фазовый распад, или непрерывный фазовый переход 2-го рода.
Фазовое равновесие и температурные фазовые переходы первого рода простых гомогенных материальных систем хорошо описываются классическими теориями конденсации паров в жидкое состояние, кристаллизации жидкостей и нуклеационного фазового разделения бинарных смесей ограниченно растворимых некристаллизующихся жидкостей при сравнительно небольшом их переохлаждении ниже равновесной (термодинамической) температуры перехода Tm, определяемой по соотношению изменений энтальпии и энтропии системы в равновесных слостояниях до и после перехода. При этом в современных подходах материальные системы подразделяются на два основных тип в зависимости от межатомных и межмолекулярных связей на «жесткие» (hard matter) и мягкие (soft matter) системы. К первому типу относятся металлы и неорганические неметаллические материалы (керамики, стекла – окидные, нитридные и др.) с металлическими, ионными, ковалентными и ионноковалентными межатомными связями), а ко второму – органические вещества, в том числе полимеры со слабыми, преимущественно ван-дер-ваальсовскими связями. Рассматриваемое ниже относится преимущечтвенно к системам второго типа.
А) Однокомпонентные системы (чистые вещества).
В
случае чистых веществ, способных
находиться в парообразном, жидком и
кристаллическом (твердом) (п-ж-т)
состояниях равновесному сосуществованию
двух фаз (п-ж,
п-т, ж-т
или
т-т)
и точке фазового перехода 1-го рода
соответствует равенство нулю разности
мольных свободных энергий фаз (ΔGm=0),
т.е. пересечению кривых зависимостей
мольных свободных энергий фаз от
температуры (при постоянном давлении).
Слева от точки пересечения (при более
низкой температуре) мольная свободная
энергия 2-й фазы (например, жидкой в
системе п-ж
и твердой - в системе ж-т)
меньше, чем 1-й фазы (парообразной и
жидкой соответственно), а справа (при
более высокой температуре) - наоборот.
Следовательно, в равновесном состоянии
при более низкой температуре должна
быть термодинамически стабильна 2-я
фаза, а при более высокой температуре
- 1-я фаза. Точка пересечения кривых
соответствует температурному фазовому
переходу - превращению одной фазы в
другую, что соответствует
испарению/конденсации, возгонке/конденсации,
кристаллизации/плавлению или превращению
двух твердых фаз чистого вещества. В
этой точке кривая мольной свободной
энергии одной фазы плавно переходит в
другую кривую, претерпевая излом, т.е.
при фазовом превращении свободная
энергия системы изменяется непрерывно
(без скачка). Однако ее первые производные
по интенсивным независимым переменным
Т
и р,
(экстенсивные независимые переменные):![]() и
и
![]() при таком превращении изменяются
скачком. Такое превращение соответствует
равновесному
фазовому переходу 1-го рода
при температуре
при таком превращении изменяются
скачком. Такое превращение соответствует
равновесному
фазовому переходу 1-го рода
при температуре
![]() .
В этом случае для изолированных
материальных систем скачок энтропии в
соответствии с фундаментальным
определением энтропии (
.
В этом случае для изолированных
материальных систем скачок энтропии в
соответствии с фундаментальным
определением энтропии (![]() )
связан с мольной теплотой перехода
)
связан с мольной теплотой перехода![]() ,
обратной по знаку мольной энтальпии
перехода
,
обратной по знаку мольной энтальпии
перехода
![]() .
Таким образом, фазовые переходы 1-го
рода сопровождаются скачкообразным
изменением объема и поглощением или
выделением теплоты перехода. Если в
1-компонентной системе одновременно
изменять температуру и давление таким
образом, чтобы мольные свободные энергии
фаз оставались одинаковыми, то в
координатах Т-р
две равновесно существующие фазы,
разделяются линией
(кривой) сосуществования,
дифференциальное уравнение которой
соответствует уравнению
Клаузиуса-Клапейрона.
Это уравнение выведено с использованием
уравнения Гиббса-Дюгема при условии
равенства мольных свободных энергий
сосуществующих фаз:
.
Таким образом, фазовые переходы 1-го
рода сопровождаются скачкообразным
изменением объема и поглощением или
выделением теплоты перехода. Если в
1-компонентной системе одновременно
изменять температуру и давление таким
образом, чтобы мольные свободные энергии
фаз оставались одинаковыми, то в
координатах Т-р
две равновесно существующие фазы,
разделяются линией
(кривой) сосуществования,
дифференциальное уравнение которой
соответствует уравнению
Клаузиуса-Клапейрона.
Это уравнение выведено с использованием
уравнения Гиббса-Дюгема при условии
равенства мольных свободных энергий
сосуществующих фаз:
![]() ,
где
,
где
![]() -
разности мольных энтропий, объемов и
энтальпий между двумя фазами соответственно.
Величина
-
разности мольных энтропий, объемов и
энтальпий между двумя фазами соответственно.
Величина
![]() соответствует
мольной энтальпии фазового перехода.
Для одновременно сосуществующих трех
фаз (например, парообразной, жидкой и
твердой) в 1-компонентной системе
производная
соответствует
мольной энтальпии фазового перехода.
Для одновременно сосуществующих трех
фаз (например, парообразной, жидкой и
твердой) в 1-компонентной системе
производная
![]() изменяется скачком, и кривые сосуществования
двух фаз сходятся в одной точке, называемой
тройной, т.е. каждая кривая претерпевает
излом. Равновесная
(термодинамическая) температура (точка)
фазового перехода Tm
определяется из условия равенства нулю
разности свободной энергии Гиббса для
двух сосуществующих и находящихся в
равновесии фаз в точке перехода:
изменяется скачком, и кривые сосуществования
двух фаз сходятся в одной точке, называемой
тройной, т.е. каждая кривая претерпевает
излом. Равновесная
(термодинамическая) температура (точка)
фазового перехода Tm
определяется из условия равенства нулю
разности свободной энергии Гиббса для
двух сосуществующих и находящихся в
равновесии фаз в точке перехода:
![]() ,
т.е.
,
т.е.
![]() .
Зависимость температуры фазового
перехода Tm
от давления описывается рассмотренным
выше уравнением Клаузиуса-Клапейрона.
При температуре фазового перехода
первого рода из-за скрытой теплоты и
неизменности температуры вторые
производные свободной энергии, в
частности, удельная теплоемкость
.
Зависимость температуры фазового
перехода Tm
от давления описывается рассмотренным
выше уравнением Клаузиуса-Клапейрона.
При температуре фазового перехода
первого рода из-за скрытой теплоты и
неизменности температуры вторые
производные свободной энергии, в
частности, удельная теплоемкость
![]() претерпевает «сингулярность, т.е.
обращается в бесконечность, так как
претерпевает «сингулярность, т.е.
обращается в бесконечность, так как
![]() -
подводимая или отводимая теплота, равная
скрытой теплоте фазового перехода, а
ΔТ
=0, так при фазовом переходе Т
остается постоянной.
-
подводимая или отводимая теплота, равная
скрытой теплоте фазового перехода, а
ΔТ
=0, так при фазовом переходе Т
остается постоянной.
Если
рассматривать изобарно-изотермический
фазовый переход 1-го рода между двумя
фазами однокомпонентной системы как
реакцию α→β,
то мольную свободную энергию этого
процесса можно рассчитать по выражению,
полученному решением уравнения
Гиббса-Гельмгольца:![]() ,
где
,
где
![]() ,
,
![]()
![]() ;
;
![]() ;
;
![]() и
и
![]() -
мольная энтальпия и энтропия процесса
при 0 К соответственно. Анализ этих
соотношений позволил Нернсту сформулировать
так называемый тепловой закон для
изобарно-изотермического процесса α→β:
-
мольная энтальпия и энтропия процесса
при 0 К соответственно. Анализ этих
соотношений позволил Нернсту сформулировать
так называемый тепловой закон для
изобарно-изотермического процесса α→β:
 или ΔSm0=0,
который связан с постулатом о недостижимости
абсолютного нуля.
или ΔSm0=0,
который связан с постулатом о недостижимости
абсолютного нуля.
С
позиций термодинамической устойчивости
материальных однокомпонентных систем
к флуктуациям равновесные фазовые
переходы 1-го рода, в частности переходы
из жидкого, или аморфного, в кристаллическое
состояние, рассматриваются как потеря
устойчивости к флуктуациям больше
некоторого критического размера
(образование стабильно растущего
зародыша новой фазы), определяемого
вкладом в общее изменение свободной
энергии объемного (отрицательного) и
поверхностного (положительного) вклада
при увеличении размера флуктуаций:
![]() ,
где gv,
gs
– соответственно, удельная объемная
(на единицу объема) и поверхностная (на
единицу поверхности) свободная энергия
при заданных условиях, r
– радиус флуктуации. Для флуктуации,
содержащей n
частиц:
,
где gv,
gs
– соответственно, удельная объемная
(на единицу объема) и поверхностная (на
единицу поверхности) свободная энергия
при заданных условиях, r
– радиус флуктуации. Для флуктуации,
содержащей n
частиц:
![]() и
и
![]() ,
где
,
где
![]() - химические потенциалы фаз, приходящиеся
на молекулу; а – активность пара,
переохлаждение или пересыщение; А(n)
– площадь поверхности флуктуации; V
– мольный объем конденсированной фазы;
γ – удельная межфазная энергия. Условие
потери устойчивости системы к флуктуациям
и формирования устойчивых зародышей
новой фазы соответствует максимальному
положительному значению суммарной
- химические потенциалы фаз, приходящиеся
на молекулу; а – активность пара,
переохлаждение или пересыщение; А(n)
– площадь поверхности флуктуации; V
– мольный объем конденсированной фазы;
γ – удельная межфазная энергия. Условие
потери устойчивости системы к флуктуациям
и формирования устойчивых зародышей
новой фазы соответствует максимальному
положительному значению суммарной
![]() при
некотором критическом значении
при
некотором критическом значении
![]() ,
после которого она начинает уменьшаться.
Энергетический барьер, который должна
преодолеть флуктуация для формирования
зародыша критического размера, число
частиц в нем и его радиус равны
соответственно:
,
после которого она начинает уменьшаться.
Энергетический барьер, который должна
преодолеть флуктуация для формирования
зародыша критического размера, число
частиц в нем и его радиус равны
соответственно:
![]() .
.
Классическим
примером неустойчивого состояния
(потери механической устойчивости) в
условиях, далеких от равновесия, и
критического непрерывного перехода
является переход чистого вещества в
критическое состояние в результате
фазового перехода второго рода при
критических температуре и давлении.
Критическое состояние жидкость-пар, в
котором отсутствует четкая граница
раздела, может существовать в некоторых
областях изотерм p-V
и
обобщенной диаграммы p-V-Т.
Устойчивые равновесные состояния
жидкость-пар и пар-жидкость могут
существовать только в тех случаях, когда
выполняется условие (85):![]() >0
или
>0
или![]() <0.
При условии
<0.
При условии
![]() >0
состояние жидкость-пар является
неустойчивым: жидкость находится в
перегретом метастабильном состоянии
(до минимума справа на изотерме p-V,
при
котором
>0
состояние жидкость-пар является
неустойчивым: жидкость находится в
перегретом метастабильном состоянии
(до минимума справа на изотерме p-V,
при
котором
![]() ),
а пар – в пересыщенном состоянии (после
максимума справа на изотерме p-V,
при
котором
),
а пар – в пересыщенном состоянии (после
максимума справа на изотерме p-V,
при
котором
![]() ).
Температура, при которой на изотерме
p-V
исчезает минимум и максимум и появляется
точка
перегиба
).
Температура, при которой на изотерме
p-V
исчезает минимум и максимум и появляется
точка
перегиба
![]() соответствует критической точке Тс,
а область между минимумами и максимумами
изотерм – нестабильной области
критического состояния.
соответствует критической точке Тс,
а область между минимумами и максимумами
изотерм – нестабильной области
критического состояния.
Другим
классическим примером возможности
перехода в нестабильное состояние и
критического поведения является
спинодальное расслоение (распад) бинарных
растворов двух ограниченно растворимых
жидкостей. Условием стабильности
(устойчивости к флуктуациям концентрации)
таких растворов служит неравенство
(86):
![]() <0.
Термодинамические расчеты, проведенные
для нормальных бинарных смесей
органических жидкостей, в том числе
полимеров, формулируют ют это условие
в следующем виде:
<0.
Термодинамические расчеты, проведенные
для нормальных бинарных смесей
органических жидкостей, в том числе
полимеров, формулируют ют это условие
в следующем виде:
![]() >0
(88),
где, х1,
х2
- мольные доли компонентов (х1+х2=1);
χ – параметр взаимодействия компонентов,
учитывающий различия в энергии их
межмолекулярного взаимодействия
(константа, слабо зависящая от температуры
и соотношения компонентов),
>0
(88),
где, х1,
х2
- мольные доли компонентов (х1+х2=1);
χ – параметр взаимодействия компонентов,
учитывающий различия в энергии их
межмолекулярного взаимодействия
(константа, слабо зависящая от температуры
и соотношения компонентов),
![]() -
газовая
постоянная и температура соответственно.
Так как обычно
-
газовая
постоянная и температура соответственно.
Так как обычно
![]() >0,
а произведение
х1х2
- мало, то при достаточно высокой
температуре условие стабильности
выполняется в широком диапазоне
соотношений компонентов. При низких Т
это условие может нарушаться, система
становится неустойчивой флуктуациям
концентрации и способна разделяться
на две фазы в результате неограниченного
роста таких флуктуаций. Соотношение
>0,
а произведение
х1х2
- мало, то при достаточно высокой
температуре условие стабильности
выполняется в широком диапазоне
соотношений компонентов. При низких Т
это условие может нарушаться, система
становится неустойчивой флуктуациям
концентрации и способна разделяться
на две фазы в результате неограниченного
роста таких флуктуаций. Соотношение
![]() (89)
определяет
критическую
температуру нестабильности смеси как
функцию состава (при заданном χ). Линии
на диаграмме состояния в координатах
температура состав, проходящие через
Тс
(сходящиеся
в ней), разделяют устойчивую область от
метастабильной (бинодаль) и метастабильную
от неустойчивой (спинодаль). Бинодаль
получают, приравнивая химические
потенциалы компонентов в двух фазах, а
спинодаль определяется функцией
(89)
определяет
критическую
температуру нестабильности смеси как
функцию состава (при заданном χ). Линии
на диаграмме состояния в координатах
температура состав, проходящие через
Тс
(сходящиеся
в ней), разделяют устойчивую область от
метастабильной (бинодаль) и метастабильную
от неустойчивой (спинодаль). Бинодаль
получают, приравнивая химические
потенциалы компонентов в двух фазах, а
спинодаль определяется функцией
![]() (90).
В
критической точке и в области неустойчивости
(ниже спинодали) флуктуации концентрации
критически растут, т.е. происходит
выделение (на начальной стадии
спинодального распада) в растворе
растущих (без активационного потенциального
барьера) флуктуаций с повышенной
концентрацией одного из компонентов в
среде с его пониженной концентрацией,
т.е. происходит как бы непрерывное
перерождение системы из гомогенного
состояния в гетерофазное. Этот процесс
на начальной стадии протекает со всеми
характерными особенностями критических
явлений, обусловленными скоррелирванным
на большие расстояния кооперативным
движением молекул. На предельных стадиях
в системе устанавливается равновесное
распределение фаз и компонентов в них.
В метастабильной области (между бинодалью
и спинодалью) разделение фаз возможно
только как классический фазовый переход
первого рода в результате превышения
флуктуациями концентрации некоторого
критического размера с преодолением
потенциального барьера зарождения, или
нуклеации и роста новой фазы.
(90).
В
критической точке и в области неустойчивости
(ниже спинодали) флуктуации концентрации
критически растут, т.е. происходит
выделение (на начальной стадии
спинодального распада) в растворе
растущих (без активационного потенциального
барьера) флуктуаций с повышенной
концентрацией одного из компонентов в
среде с его пониженной концентрацией,
т.е. происходит как бы непрерывное
перерождение системы из гомогенного
состояния в гетерофазное. Этот процесс
на начальной стадии протекает со всеми
характерными особенностями критических
явлений, обусловленными скоррелирванным
на большие расстояния кооперативным
движением молекул. На предельных стадиях
в системе устанавливается равновесное
распределение фаз и компонентов в них.
В метастабильной области (между бинодалью
и спинодалью) разделение фаз возможно
только как классический фазовый переход
первого рода в результате превышения
флуктуациями концентрации некоторого
критического размера с преодолением
потенциального барьера зарождения, или
нуклеации и роста новой фазы.
По современным представлениям в метастабильных, сильно переохлажденных ниже равновесной температуры кристаллизации (некристаллизующихся или трудно кристаллизующихся) однокомпонентных (чистых) жидкостях (расплавах) также возможен критический спинодальный распад в результате критического роста флуктуаций плотности. Эти представления базируются на концепции метастабильной фазовой границы и наличия кривых метастабильного сосуществования двух жидких фаз (линии бинодали) и их термодинамической нестабильности (линии спинодали), скрытых внутри области равновесного сосуществования жидкой и кристаллической фаз. При достаточно большом переохлаждения расплава ниже равновесной температуры плавления Tm возможно пересечение линии спинодали с переходом расплава в нестабильную область и его критическим распадом на более упорядоченную твердоподобную и менее упорядоченную жидкоподобную фазы вследствие критического (непрерывного безактивационного) роста флуктуаций плотности (твердоподобных доменов) в менее упорядоченной (жидкоподобной) среде. Твердоподобные домены образуются из более способных к упорядоченной упаковке низкотемпературных транс-конформаций молекул (транс-конформеров), которые, в свою очередь, образуются из менее способных к упорядоченной упаковке более высокотемпературных гош-конформаций молекул (гош-конформеров) в результате конформационных гош/транс превращений при понижении температуры.
Теоретическое
построение линий бинодали и спинодали
сильно переохлажденной жидкости (без
учета линии кристаллизации) базируется
на расчете удельной свободной энергии
Гельмгольца в зависимости от средней
массовой плотности жидкости
![]() и доли транс-конформаций
η
и
на определении изобар в координатах
Т-
и доли транс-конформаций
η
и
на определении изобар в координатах
Т-![]() по
уравнению состояния
по
уравнению состояния
![]() (91).
При этом свободная энергия, приходящаяся
на единицу объема, складывается из двух
компонентов:
(91).
При этом свободная энергия, приходящаяся
на единицу объема, складывается из двух
компонентов:![]() .
Первый член в уравнении свободной
энергии
.
Первый член в уравнении свободной
энергии
![]() представляет собой свободную энергию
жидкости при η=0,
а второй член
представляет собой свободную энергию
жидкости при η=0,
а второй член
![]() - при η≠0,
т.е.
с
учетом распределения конформеров.
Кривая f
как функция
- при η≠0,
т.е.
с
учетом распределения конформеров.
Кривая f
как функция
![]() ,
имеющая при высокой температуре один
минимум, при некоторой критической
температуре Тс
разделяется на два минимума, соответствующих
двум сосуществующим термодинамически
стабильным состояниям, причем точки
минимумов на кривых f
(
,
имеющая при высокой температуре один
минимум, при некоторой критической
температуре Тс
разделяется на два минимума, соответствующих
двум сосуществующим термодинамически
стабильным состояниям, причем точки
минимумов на кривых f
(![]() )
соответствуют линии бинодали, а точки
перегибов – линии спинодали, которые
сходятся в критической точке Тс.
При критической и более низкой температуре,
т.е. в области ниже спинодали, должен
происходить спинодальный распад сильно
переохлажденной жидкости (расплава) в
результате неограниченного роста
твердоподобных флуктуаций. Физически
это соответствует тому, что в системе
уменьшается конформационная энтропия,
и в среде, образованной преимущественно
гош-конформерами,
начинают спонтанно выделяться образующиеся
из транс-конформеров
более плотные домены. Спинодальный
распад сильно переохлажденной жидкости
может служить начальной стадией
образования зародышей кристаллизации
или при дальнейшем охлаждении (при
неспособности жидкости, вследствие
стерических или кинетических ограничений,
образовывать сверхкритические зародыши
кристаллизации) быть причиной стеклования
жидкости из-за резкого возрастания
времени релаксации при образовании
твердопоподобных доменов и замораживания
молекулярного теплового движения.
)
соответствуют линии бинодали, а точки
перегибов – линии спинодали, которые
сходятся в критической точке Тс.
При критической и более низкой температуре,
т.е. в области ниже спинодали, должен
происходить спинодальный распад сильно
переохлажденной жидкости (расплава) в
результате неограниченного роста
твердоподобных флуктуаций. Физически
это соответствует тому, что в системе
уменьшается конформационная энтропия,
и в среде, образованной преимущественно
гош-конформерами,
начинают спонтанно выделяться образующиеся
из транс-конформеров
более плотные домены. Спинодальный
распад сильно переохлажденной жидкости
может служить начальной стадией
образования зародышей кристаллизации
или при дальнейшем охлаждении (при
неспособности жидкости, вследствие
стерических или кинетических ограничений,
образовывать сверхкритические зародыши
кристаллизации) быть причиной стеклования
жидкости из-за резкого возрастания
времени релаксации при образовании
твердопоподобных доменов и замораживания
молекулярного теплового движения.
Классические термодинамические теории стеклования базируются на экспериментально установленных фактах об отклонении (уходе) при стекловании в узком температурном интервале экстенсивных параметров (S,H,V) от равновесной для жидкого состояния кривой их температурной зависимости (Рис.1-2). При этом их производные по интенсивным параметрам (температуре и давлению), в частности теплоемкость, претерпевают изменение, близкое к ступенчатому (Рис.3), а если проэкстраполировать температурную зависимость разности энтропий жидкости и кристалла ΔS(Т) в область низких температур, то она обращается в нуль при конечной, сравнительно высокой температуре (парадокс Козмана - см. Рис.2). При приближении равновесным способом переохлажденной некристаллизующей жидкости к этой температуре (Тк) жидкость должна претерпеть фазовый переход 2-го рода с плавным приближением ее энтропии к энтропии кристалла. В основополагающей теории Адама-Гиббса уменьшение энтропии жидкости при приближении к Тк обусловлено резким уменьшением так называемого конфигурационного вклада в энтропию.
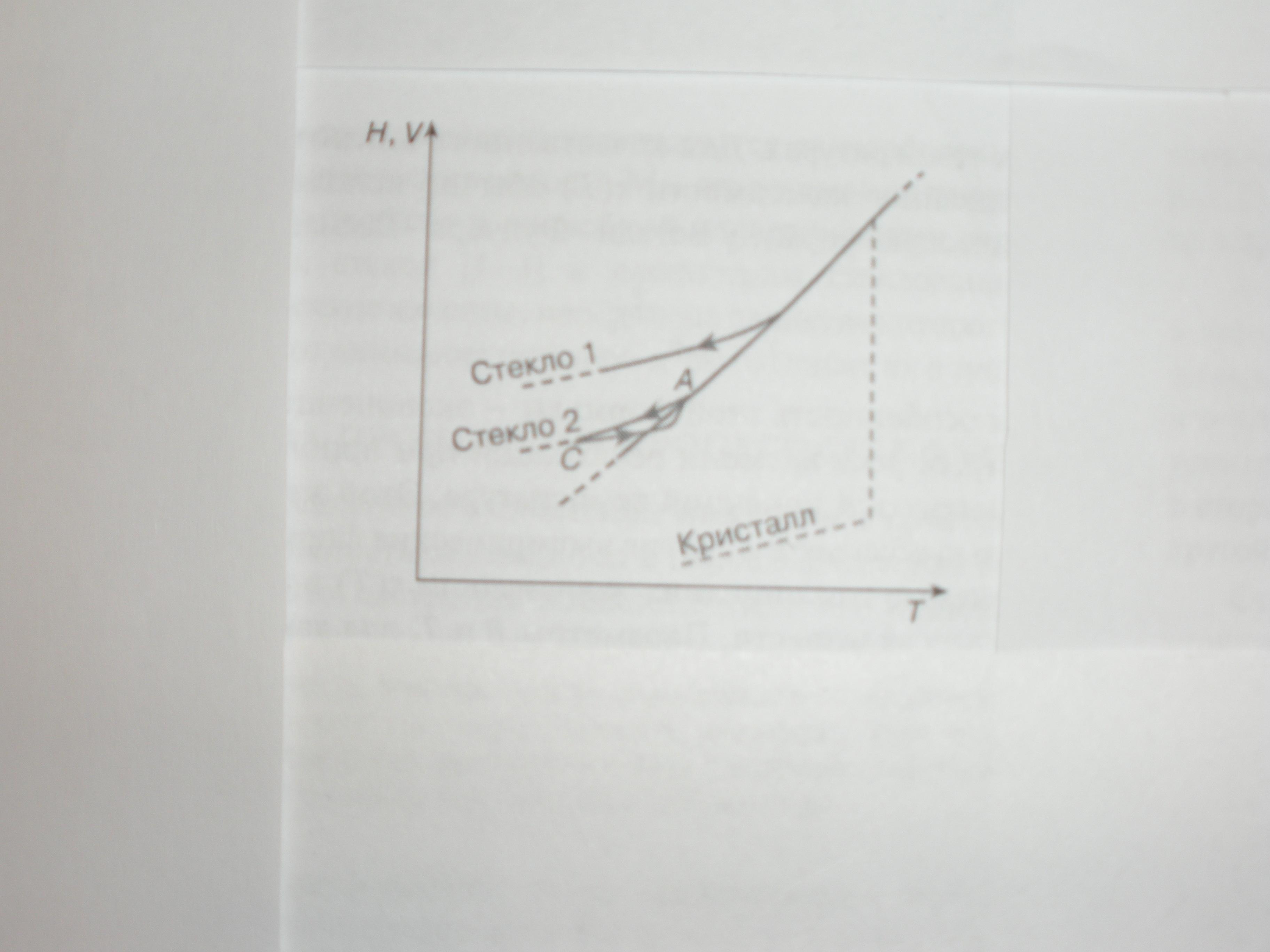
Рис.1. Температурные зависимости энтальпии и объема (H,V) некристаллизующейся жидкости при переохлаждении с различной скоростью: Стекло1- быстрое охлаждение; Стекло 2- медленное охлаждение (пунктиром показано их изменение при кристаллизации).
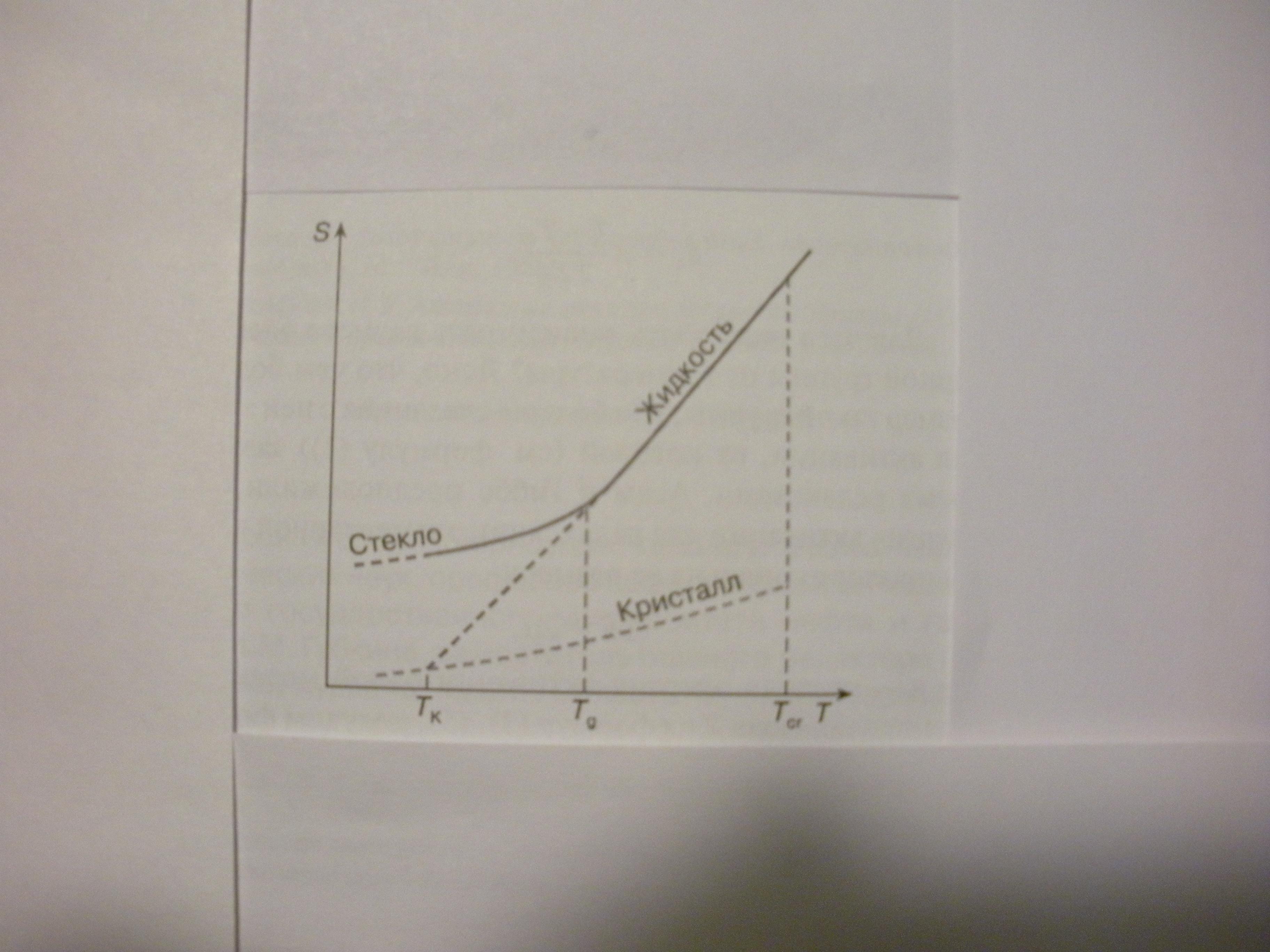
Рис.2. Температурные зависимости энтропии (S) некристаллизующейся жидкости при переохлаждении: Тcr – температура кристаллизации; Тg – температура стеклования; Тк – температура, при которой энтропия жидкости сравнивается с энтропией кристалла (эффект Козмана).

Рис.3. Температурные зависимости мольной теплоемкости при постоянном давлении некристаллизующейся жидкости при переохлаждении ниже Тg (кривые 1-2, стрелки влево, кривая 1 – при быстром, кривая 2 – при медленном охлаждении) и при обратном нагревании (кривая 2, стрелка направо).
Адам
и Гиббс связали уменьшение конфигурационной
энтропии жидкости при приближении к Тк
с резким возрастанием роли кооперативных
явлений при релаксации к равновесным
конфигурациям вследствие образования
твердоподобных флуктуаций. Элементарным
независимым объектом релаксации при
этом становится не один первичный
структурный элемент (молекула или
сегмент), а группа из Z
таких элементов (флуктуация плотности),
которая перестраивается как единое
целое. При понижении температуры ниже
![]() количество
таких элементов в группах возрастает,
что приводит к резкому уменьшению числа
микросостояний и, следовательно, вклада
конфигурационной энтропии. В простейшем
случае, если связать с каждой группой
из Z
элементов два состояния (до и после
замораживания крупномасштабной формы
теплового движения), то конфигурационная
энтропия для одного моля первичных
элементов (числа Авогадро) равна:
количество
таких элементов в группах возрастает,
что приводит к резкому уменьшению числа
микросостояний и, следовательно, вклада
конфигурационной энтропии. В простейшем
случае, если связать с каждой группой
из Z
элементов два состояния (до и после
замораживания крупномасштабной формы
теплового движения), то конфигурационная
энтропия для одного моля первичных
элементов (числа Авогадро) равна:
![]() .
Очевидно, что при уменьшении конфигурационной
энтропии размер групп растет и может
достигать макроскопических величин.
Исходя из предположения, что конфигурационная
энтропия обращается в нуль при Тк,
то
.
Очевидно, что при уменьшении конфигурационной
энтропии размер групп растет и может
достигать макроскопических величин.
Исходя из предположения, что конфигурационная
энтропия обращается в нуль при Тк,
то
 ,
где Ср(Т)
–
зависимость конфигурационной теплоемкости
при постоянном давлении от температуры.
Конфигурационная теплоемкость, как и
конфигурационная энтропия и энтальпия,
связана с релаксацией системы к
равновесным конфигурациям и в значительной
мере определяет уменьшение теплоемкости
жидкости при ее переохлаждении. Энтропия
и энтальпия при незавершенной релаксации
(при ξ<1,
где ξ
– степень полноты прохождения
конфигурационных превращений типа
«транс»/»гош» переходов), т.е. после
ухода от равновесной для жидкого
состояния кривой их температурной
зависимости (см. Рис.1-2) всегда меньше
их значений в равновесном состоянии,
когда ξ=1,
а температура ухода от равновесных
значений тем ниже, чем меньше скорость
охлаждения. Измеряемая теплоемкость
при незавершенной релаксации, т.е. при
ξ<1,
также всегда меньше теплоемкости в
равновесном состоянии при ξ=1,
а е изменение при переходе несколько
увеличивается с уменьшением скорости
охлаждения. Как видно из рис.3 вблизи
Тк,
которую считают термодинамической
температурой стеклования, функция Ср(Т)
имеет
довольно сложный характер и зависит от
темпа (скорости) охлаждения. В предположении
простой обратно пропорциональной
зависимости Ср(Т)=А/Т:
,
где Ср(Т)
–
зависимость конфигурационной теплоемкости
при постоянном давлении от температуры.
Конфигурационная теплоемкость, как и
конфигурационная энтропия и энтальпия,
связана с релаксацией системы к
равновесным конфигурациям и в значительной
мере определяет уменьшение теплоемкости
жидкости при ее переохлаждении. Энтропия
и энтальпия при незавершенной релаксации
(при ξ<1,
где ξ
– степень полноты прохождения
конфигурационных превращений типа
«транс»/»гош» переходов), т.е. после
ухода от равновесной для жидкого
состояния кривой их температурной
зависимости (см. Рис.1-2) всегда меньше
их значений в равновесном состоянии,
когда ξ=1,
а температура ухода от равновесных
значений тем ниже, чем меньше скорость
охлаждения. Измеряемая теплоемкость
при незавершенной релаксации, т.е. при
ξ<1,
также всегда меньше теплоемкости в
равновесном состоянии при ξ=1,
а е изменение при переходе несколько
увеличивается с уменьшением скорости
охлаждения. Как видно из рис.3 вблизи
Тк,
которую считают термодинамической
температурой стеклования, функция Ср(Т)
имеет
довольно сложный характер и зависит от
темпа (скорости) охлаждения. В предположении
простой обратно пропорциональной
зависимости Ср(Т)=А/Т:
![]() ,
и при Т→Тк
SK→0.
Температурная зависимость времени
релаксации перехода к равновесным
конфигурациям, определенная из
предположения, что энергия активации
такого процесса для элементарной группы
пропорциональна ее размеру, описывается
экспоненциальной функцией
,
и при Т→Тк
SK→0.
Температурная зависимость времени
релаксации перехода к равновесным
конфигурациям, определенная из
предположения, что энергия активации
такого процесса для элементарной группы
пропорциональна ее размеру, описывается
экспоненциальной функцией
![]() ,
где θ0
и В
– константы, причем
,
где θ0
и В
– константы, причем
![]() .
Эта функция аналогична известной
эмпирической формуле Фогеля-Фалчера-Таммана
(ФФТ)
.
Эта функция аналогична известной
эмпирической формуле Фогеля-Фалчера-Таммана
(ФФТ)
![]() ,
в соответствие с которой при Т→Тк
θ→∞.
Из этого следует, что при приближении
к Тк,,
равновесное состояние не может быть
достигнуто при любом самом большом
характерном для эксперимента временем
изменения температуры tэ
время релаксации превысит его, и жидкость
окажется в замороженном неравновесном
(стеклообразном) состоянии, когда тип
движения, ответственный за установление
равновесных конфигураций, становится
слишком медленным, чтобы успевать
подстраиваться к изменению температуры.
Поэтому стеклование как термодинамический
переход второго рода, если он существует,
является на практике скрытым, т.е.
практически ненаблюдаемым и всегда
проявляется как динамический, или
кинетический переход, температура
которого зависит от временных условий
эксперимента.
,
в соответствие с которой при Т→Тк
θ→∞.
Из этого следует, что при приближении
к Тк,,
равновесное состояние не может быть
достигнуто при любом самом большом
характерном для эксперимента временем
изменения температуры tэ
время релаксации превысит его, и жидкость
окажется в замороженном неравновесном
(стеклообразном) состоянии, когда тип
движения, ответственный за установление
равновесных конфигураций, становится
слишком медленным, чтобы успевать
подстраиваться к изменению температуры.
Поэтому стеклование как термодинамический
переход второго рода, если он существует,
является на практике скрытым, т.е.
практически ненаблюдаемым и всегда
проявляется как динамический, или
кинетический переход, температура
которого зависит от временных условий
эксперимента.
Б) Некристаллизующиеся бинарные системы (растворы, смеси).
К
этим системам относятся, в первую
очередь, растворы трудно кристаллизующихся
органических жидкостей и смеси (растворы)
расплавов некристаллизующихся
термопластичных полимеров друг с другом
или другими нелетучими некристаллизующимися
компонентами. Важнейшей особенностью
таких систем, при заданном давлении,
является ограниченная растворимость
(термодинамическая совместимость)
компонентов в аморфном состоянии и
неспособность кристаллизоваться при
температуре ниже Тm
вследствие кинетических и молекулярных
структурных (стерических) эффектов.
Вследствие ограниченной термодинамической
совместимости компонентов, определяемой
молекулярной массой и характером
межмолекулярного взаимодействия при
заданных параметрах состояния
(температуре, давлении и составе), эти
композиции могут находиться в гомогенном
однофазном состоянии (в виде раствора)
только при достаточно высокой температуре
и малом содержании одного из компонентов.
Для обобщенной характеристики равновесного
фазового состояния таких систем с
учетом термодинамической совместимости
компонентов используют зависимости
избыточной (по отношению к стандартному
состоянию – чистым компонентам) мольной
свободной энергии смешения или избыточных
значений химических потенциалов
компонентов от их мольных (![]() )
или объемных (
)
или объемных (![]() )
долей при заданных температуре и
давлении, из которых получают диаграммы
состояния в координатах температура-состав.
Диаграммы состоят из двух линий -
бинодали и спинодали, разделяющих
области равновесного, термодинамически
стабильного однофазного (выше бинодали)
и нестабильного, или двухфазного (ниже
спинодали) состояний с полной и
ограниченной совместимостью компонентов
соответственно. Области между бинодалью
и спинодалью характеризуют метастабильное,
термодинамически неустойчивое состояние.
При Т>ВКТР эта область исчезает.
Теоретическое построение таких диаграмм
базируется на статистической теории
растворов полимеров Флори-Хаггинса,
позволяющей рассчитывать избыточные
значения плотности средней свободной
энергии смешения, т.е. величины,
приходящейся на единицу объема (Δgсм)
в зависимости от температуры и природы
компонентов (молекулярной массы и
межмолекулярного взаимодействия). Ее
первые производные по числу молекул
или звеньев цепей полимеров, соответствуют
избыточным значениям химических
потенциалов компонентов (Δμ1
и Δμ2).
Равенство Δμ1
и Δμ2
характеризует равновесное сосуществование
аморфного гомогенного и гетерогенного
состояний, т.е дает линию бинодали.
Вторые производные плотности средней
свободной энергии смешения по составу
характеризуют границу метастабильной
области (спинодаль), а третьи – верхнюю
критическую точку растворимости
компонентов.
)
долей при заданных температуре и
давлении, из которых получают диаграммы
состояния в координатах температура-состав.
Диаграммы состоят из двух линий -
бинодали и спинодали, разделяющих
области равновесного, термодинамически
стабильного однофазного (выше бинодали)
и нестабильного, или двухфазного (ниже
спинодали) состояний с полной и
ограниченной совместимостью компонентов
соответственно. Области между бинодалью
и спинодалью характеризуют метастабильное,
термодинамически неустойчивое состояние.
При Т>ВКТР эта область исчезает.
Теоретическое построение таких диаграмм
базируется на статистической теории
растворов полимеров Флори-Хаггинса,
позволяющей рассчитывать избыточные
значения плотности средней свободной
энергии смешения, т.е. величины,
приходящейся на единицу объема (Δgсм)
в зависимости от температуры и природы
компонентов (молекулярной массы и
межмолекулярного взаимодействия). Ее
первые производные по числу молекул
или звеньев цепей полимеров, соответствуют
избыточным значениям химических
потенциалов компонентов (Δμ1
и Δμ2).
Равенство Δμ1
и Δμ2
характеризует равновесное сосуществование
аморфного гомогенного и гетерогенного
состояний, т.е дает линию бинодали.
Вторые производные плотности средней
свободной энергии смешения по составу
характеризуют границу метастабильной
области (спинодаль), а третьи – верхнюю
критическую точку растворимости
компонентов.
Наибольший
вклад в свободную энергию смешения и
химические потенциалы некристаллизующихся
компонентов в смеси дает комбинаториальная
энтропия смешения ΔSсм,
а особенности межмолекулярного
взаимодействия компонентов учитывается
через парный параметр взаимодействия
![]() ,
характеризующий изменение энергии при
разрыве связей между молекулами исходных
компонентов 1-1 (ω11)
и 2-2 (ω22)
и образования связей их друг с другом
1-2 (ω12):
,
характеризующий изменение энергии при
разрыве связей между молекулами исходных
компонентов 1-1 (ω11)
и 2-2 (ω22)
и образования связей их друг с другом
1-2 (ω12):
![]() ,
где k
–константа Больцмана; Т – абсолютная
температура. В усовершенствованных
теориях параметр χ
рассматривают состоящим из энтальпийного
(χH)
и энтропийного некомбинаториального
(χS)
вкладов: χ
= χH
+ χS.
В идеальных, или θ-условиях
χH
=0, а χS
=1/2.
Полуэмпирическим методов параметр χ
может быть рассчитан через разность
параметров растворимости компонентов
Δδ=
δ1-
δ2
, которые представляют собой корни
квадратные из плотности энергии когезии
ек:
,
где k
–константа Больцмана; Т – абсолютная
температура. В усовершенствованных
теориях параметр χ
рассматривают состоящим из энтальпийного
(χH)
и энтропийного некомбинаториального
(χS)
вкладов: χ
= χH
+ χS.
В идеальных, или θ-условиях
χH
=0, а χS
=1/2.
Полуэмпирическим методов параметр χ
может быть рассчитан через разность
параметров растворимости компонентов
Δδ=
δ1-
δ2
, которые представляют собой корни
квадратные из плотности энергии когезии
ек:
![]() ,
где Vr
– средний мольный объем повторяющихся
звеньев компонентов. Значения параметров
растворимости компонентов могут быть
рассчитаны непосредственно или через
мольную энергии когезии по вкладам
групп или другими методами. Предложено
также эмпирическое соотношение,
описывающее зависимость параметра
взаимодействия от состава смеси и
температуры:
,
где Vr
– средний мольный объем повторяющихся
звеньев компонентов. Значения параметров
растворимости компонентов могут быть
рассчитаны непосредственно или через
мольную энергии когезии по вкладам
групп или другими методами. Предложено
также эмпирическое соотношение,
описывающее зависимость параметра
взаимодействия от состава смеси и
температуры:![]() ,
где
,
где
![]() ,
χ1,
χ2,
А, В - константы, учитывающие молекулярную
массу и полидисперсность компонентов
и другие эффекты.
,
χ1,
χ2,
А, В - константы, учитывающие молекулярную
массу и полидисперсность компонентов
и другие эффекты.
Обобщенные
выражения для плотности энергии смешения
(Δgсм)
и химических потенциалов компонентов
с линейной формой макромолекул в бинарной
смеси как первых производных Δgсм
по составу:![]() ,
,
![]() в соответствие с теорией Флори-Хаггинса
записываются в следующем виде
соответственно:
в соответствие с теорией Флори-Хаггинса
записываются в следующем виде
соответственно:
![]() ;
;
![]() ;
;
![]() ,
,
где
n1,
n2,
Х1,
Х2
–
число молекул и степени полимеризации
компонентов соответственно: n1Х1,
n2Х2
– общее количество повторяющихся
звеньев полимерных компонентов (в
случае, если один компонентов
низкомолекулярный N1=1);
φ1,
φ2
– объемные доли компонентов. При примерно
равных объемах звеньев компонентов:
![]() .
.
Линия
бинодали
соответствует точкам минимума на кривых
зависимостей Δgсм
от состава смеси при различных температурах
и, соответственно, уравнения бинодали
составляются из условий равенства
химических потенциалов компонентов в
различных фазах. Число уравнений, которые
должны быть одновременно решены для
построения линии бинодали на фазовой
диаграмме, в соответствие с правилом
фаз Гиббса, равно: У=К(Ф-1),
где
К
–
число компонентов, Ф
– максимальное число сосуществующих
фаз. Для сосуществующих фаз, являющихся
только аморфными, не способными переходить
в парообразное и кристаллическое
состояние как в случае некристаллизующихся
полимерных композиций, максимальное
их число равно числу компонентов в смеси
вне зависимости от температуры и
давления. Поэтому для таких композиций
число уравнений, которые должны быть
решены одновременно, равно числу
компонентов, т.е. для бинарных систем
должны быть решены два уравнения для
двух сосуществующих фаз (I
и II):
Δμ1I=Δ
μ1
II
и
Δμ2I=
Δμ2II
, или
![]() и
и
![]() .
.
Линия спинодали соответствует точкам перегиба на кривых зависимостей Δgсм от состава смеси при различных температурах, а уравнение спинодали соответствует равенству нулю второй производной свободной энергии смешения по составу:
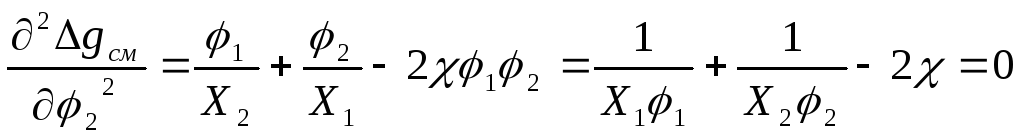 .
Если принять, что χ
есть функция только температуры (
.
Если принять, что χ
есть функция только температуры (![]() ),
то, то уравнение спинодали в терминах
температуры как функции состава
принимает вид:
),
то, то уравнение спинодали в терминах
температуры как функции состава
принимает вид:
![]() .
.
На
рис.4 приведены расчетные диаграммы
состояния смеси низкомолекулярного
(N1=1)
и высокомолекулярного компонента с
различной степенью полимеризации при
![]() .
.

Рис.4.
Расчетные диаграммы состояния смеси
низкомолекулярного (N1=1)
и высокомолекулярного компонента с
различной степенью полимеризации при
![]() и
и
![]()
Во
всех случаях диаграммы имеют верхнюю
критическую точку, где сходятся бинодаль
и спинодаль, координаты которой (Ткр
или
χкр
и
φкр)
определяются решением системы уравнений:
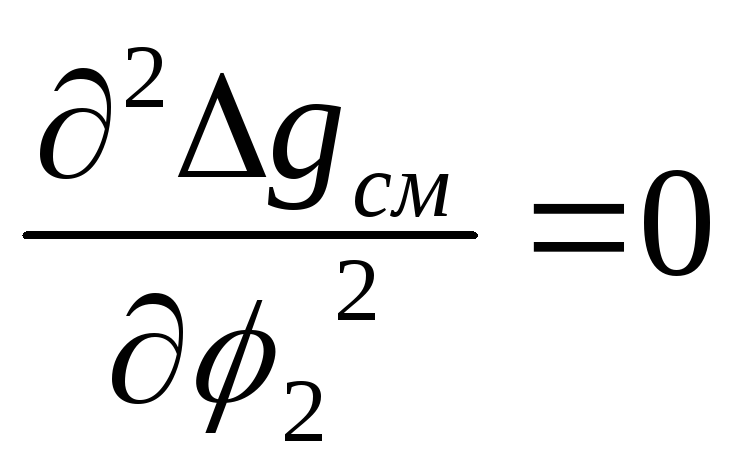 и
и
 .
Для параметров критической точки
получены сравнительно простые выражения:
.
Для параметров критической точки
получены сравнительно простые выражения:
![]() ;
;
![]() ;
;
![]() .
Для бинарной системы, компоненты которой
имеют равные степени полимеризации и
мольные объемы повторяющихся звеньев:
Х=Х1=Х2,
V=V1=V2)
фазовая диаграмма симметрична, причем
φкр
=1/2, а
χкр=2/Х.
Чем больше Х2
превышает
Х1,
тем более ассиметричной становится
фазовая диаграмма со смещением верхней
критической точки в сторону повышенной
концентрации низкомолекулярного
компонента.
.
Для бинарной системы, компоненты которой
имеют равные степени полимеризации и
мольные объемы повторяющихся звеньев:
Х=Х1=Х2,
V=V1=V2)
фазовая диаграмма симметрична, причем
φкр
=1/2, а
χкр=2/Х.
Чем больше Х2
превышает
Х1,
тем более ассиметричной становится
фазовая диаграмма со смещением верхней
критической точки в сторону повышенной
концентрации низкомолекулярного
компонента.
Если один из компонентов (второй) – сетчатый полимер, то в общее изменение плотности свободной энергии при его набухании в низкомолекулярном компоненте свой вклад вносит не только молекулярное перемешивание (Δgсм), но и упругое сопротивление сетки увеличению ее объема (Δgупр). Сумма этих компонентов рамках классической теории набухания сетчатых полимеров Флори-Ренера в равновесных условиях дает следующее выражение для общей Δg:
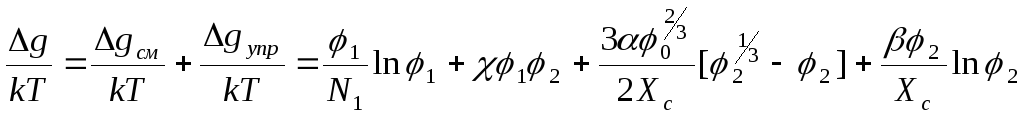 ,
где φ0
– константа, величина которой лежит
между 0 и 1 (при формировании полимерной
сетки непосредственно в присутствии
первого компонента φ0=φ2);
Хc
– степень полимеризации цепей сетчатого
полимера между узлами сетки; α
и β
– параметры упругости полимерной сетки
(по теории Флори-Ренера α=1
и β=2/f
,где
f
– функциональность узлов сетки, т.е.
число сходящихся в них цепей. В
усовершенствованных теориях α
и β
являются функциями объемной доли
сетчатого полимера и функциональности
узлов сетки:
,
где φ0
– константа, величина которой лежит
между 0 и 1 (при формировании полимерной
сетки непосредственно в присутствии
первого компонента φ0=φ2);
Хc
– степень полимеризации цепей сетчатого
полимера между узлами сетки; α
и β
– параметры упругости полимерной сетки
(по теории Флори-Ренера α=1
и β=2/f
,где
f
– функциональность узлов сетки, т.е.
число сходящихся в них цепей. В
усовершенствованных теориях α
и β
являются функциями объемной доли
сетчатого полимера и функциональности
узлов сетки:
![]() и
и
![]() .
.
При очень быстром переходе из однофазной стабильной области в нестабильную гетерофазную через метастабильую область (за время меньше времени жизни флуктуаций концентрации) или напрямую через верхнюю критическую точку процесс фазового разделения бинарных растворов на начальной стадии протекает по механизму критического, или спинодального распада системы на две аморфные фазы в результате критического (безактивационного) роста всех флуктуаций концентрации (возрастания их амплитуды), кинетика которого в решающей степени определяется диффузионными эффектами. Такой механизм разделения фаз обусловлен формой кривой зависимости плотности свободной энергии смешения в нестабильной области между точками перегиба. В отличие от метастабильных областей между точками минимумов и перегибов, где участки кривой являются вогнутыми и более крутыми в сторону точек перегиба, чем точек минимума, в нестабильной области кривая является выпуклой и более крутой в сторону точек перегиба, чем точки максимума. Соответственно, в метастабильных областях любые одинаковые отклонения концентрации от среднего значения сопровождаются меньшим уменьшением свободной энергии при отклонении в сторону точки минимума, чем ее возрастанием при отклонении в сторону точки перегиба, т.е. любые флуктуации концентрации при этом, если они не превысят некоторого критического, достаточно большого размера, когда начинает превалировать выигрыш в свободной поверхностной энергии, приводят к возрастанию свободной энергии и гасятся (демпфируют). В нестабильной области, наоборот, одинаковые отклонения концентрации от среднего значения сопровождаются большим уменьшением свободной энергии при отклонении в сторону точки перегиба, чем ее возрастание при отклонении в другую сторону, т.е. любые флуктуации концентрации ведут к уменьшению свободной энергии и должны самопроизвольно расти, ограничиваясь только кинетическими (диффузионными ) эффектами.
Теоретическое
описание механизма и кинетики спинодального
распада
некристаллизующихся бинарных полимерных
смесей базируется на определении
свободной энергии смеси состава φ,
содержащей малые флуктуации концентрации,
с помощью функционала (функции произвольных
функций) Гинзбурга-Ландау:
 ,
где
,
где
![]() ]
– плотность свободной энергии как
функция концентрации и вектора положения
r,
т.е. размера системы,
]
– плотность свободной энергии как
функция концентрации и вектора положения
r,
т.е. размера системы,
![]() - градиент концентрации, ς
– константа, учитывающая вклад флуктуаций
концентрации и характеризующая
естественную шкалу (масштаб) размеров
флуктуаций в данной конкретной системе.
Для аморфных полимерных бинарных смесей
она связана с размерами полимерных
клубков:
- градиент концентрации, ς
– константа, учитывающая вклад флуктуаций
концентрации и характеризующая
естественную шкалу (масштаб) размеров
флуктуаций в данной конкретной системе.
Для аморфных полимерных бинарных смесей
она связана с размерами полимерных
клубков:
![]() ,
где RGi
–
радиус инерции статистического клубка.
При N1=N2=N
и RG1=RG2=RG=AN1/2,
где А
–
длина статистического сегмента полимерных
цепей:
,
где RGi
–
радиус инерции статистического клубка.
При N1=N2=N
и RG1=RG2=RG=AN1/2,
где А
–
длина статистического сегмента полимерных
цепей:
![]() .
Предполагается, что параметр ς
является размерной константой системы,
аналогичной временной константе
колеблющейся системы типа периода
колебаний маятника, не зависящего от
амплитуды при малых ее величинах.
.
Предполагается, что параметр ς
является размерной константой системы,
аналогичной временной константе
колеблющейся системы типа периода
колебаний маятника, не зависящего от
амплитуды при малых ее величинах.
В
соответствие с классической теорией
спинодального распада Кана-Хилларда
разность свободной энергии статистически
гомогенной смеси и с флуктуациями
концентрации ΔG,
определенная с помощью функционала
Гинзбурга-Ландау и являющаяся
термодинамической движущей силой
спинодального распада, равна:
![]() ,
,
где δφ=φi-φi,0 – разность локальной и равновесной концентраций i-го компонента соответственно; V – общий объем смеси.
Кинетика
роста фаз при спинодальном распаде
описывается потоками компонентов,
связанными с коэффициентами трансляционной
диффузии макромолекул уравнением Фика,
в котором градиент концентрации или
активности заменен на разность химических
потенциалов, рассчитываемых как первая
производная свободной энергии по
составу. Так, поток компонента 1 в расплаве
смеси 1-2 равен:
![]() ,
а скорость роста флуктуаций (доменов):
,
а скорость роста флуктуаций (доменов):
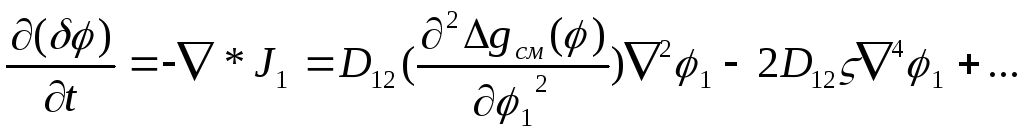 ,
где
,
где
![]() -
мера пространственного изменения потока
из бесконечно малого элемента объема,
или мера отклонения от установившегося
потока, когда вход и выход одинаковы.
-
мера пространственного изменения потока
из бесконечно малого элемента объема,
или мера отклонения от установившегося
потока, когда вход и выход одинаковы.
Коэффициент
диффузии макромолекул равен:
![]() при отсутствии зацеплений цепей и
при отсутствии зацеплений цепей и
![]() - при их наличии, где ξ
– коэффициенты трения мономерных
звеньев компонентов, Ne
– степень полимеризации цепей между
зацеплениями; А0
– длина сегмента Куна, принимаемая
равной длине мономерного звена, одинаковая
для обоих компонентов.
- при их наличии, где ξ
– коэффициенты трения мономерных
звеньев компонентов, Ne
– степень полимеризации цепей между
зацеплениями; А0
– длина сегмента Куна, принимаемая
равной длине мономерного звена, одинаковая
для обоих компонентов.
Решение приведенного выше кинетического уравнения роста фаз при спинодальном распаде дает экспоненциальное выражение для локального градиента концентрации во времени t в точке пространства, определяемой вектором положения r, в виде разложения Фурье с суммированием по всем волновым векторам (волновым числам) β или длинам волн λ, (β=2π/λ) флуктуаций концентрации:
![]() ,
,
где А и В – константы, определяемые Фурье-анализом флуктуаций в исходном состоянии (t=0); R(β) –коэффициент усиления амплитуды флуктуаций концентрации, или линейная скорость роста флуктуаций с волновым числом β:
![]()
Разложение
Фурье позволяет анализировать его
составляющие с термодинамических и
кинетических точек зрения независимо.
Анализ разложения Фурье показывает,
что синусоидальные компоненты флуктуаций
концентрации возрастают или спадают
по амплитуде в зависимости от того,
какой знак имеет коэффициент усиления.
При
![]() >0,
т.е. выше спинодали (вне нестабильной
области), R(β)
отрицателен при любом значении β,
и любая существующая флуктуация в эти
условиях рассасывается. В нестабильной
области, где
>0,
т.е. выше спинодали (вне нестабильной
области), R(β)
отрицателен при любом значении β,
и любая существующая флуктуация в эти
условиях рассасывается. В нестабильной
области, где
![]() <0
, R(β)
положителен, и все флуктуации
самопроизвольно растут с образованием
периодической или квазипериодической
доменной структуры, периодичность
которой определяется длиной волны
флуктуаций концентрации. Соответствующее
условиям
<0
, R(β)
положителен, и все флуктуации
самопроизвольно растут с образованием
периодической или квазипериодической
доменной структуры, периодичность
которой определяется длиной волны
флуктуаций концентрации. Соответствующее
условиям
![]() =0
и R(β)=0
критическое значение β
(βс)
характеризует волновое число, выше
которого амплитуда флуктуаций концентрации
растут, а ниже – рассасываются. Введение
βс
позволяет записать уравнение для R(β)
в виде:
=0
и R(β)=0
критическое значение β
(βс)
характеризует волновое число, выше
которого амплитуда флуктуаций концентрации
растут, а ниже – рассасываются. Введение
βс
позволяет записать уравнение для R(β)
в виде:
![]() .
.
Из
этого уравнения видно, что максимальной
величине R(β)
соответствует волновому вектору βm,
равному: ![]() ,
который связан с длиной волны флуктуаций
концентрации, характеризующей
периодичность образующейся доменной
структуры:
,
который связан с длиной волны флуктуаций
концентрации, характеризующей
периодичность образующейся доменной
структуры:
![]() .
.
На
начальной стадии спинодального распада
формируется уникальная фазовая
морфология, состоящая из статистически
распределенных доменов сосуществующих
фаз (растущих флуктуаций концентрации)
и диффузионной зоны между ними, толщина
которой возрастает при приближении к
температуре спинодали Тs
и
становится бесконечной при Т= Тs.
Параметр периодичности структуры λm
связан с модулем разности температур
|Т- Тs|
соотношением:
![]() ,
где q
– константа (Рис.5). На более глубоких
стадиях спинодального распада рост
амплитуды флуктуаций концентрации
замедляется, и начинает превалировать
процессы поглощения мелких доменов
более крупными вследствие выигрыша в
свободной поверхностной энергии. Эти
процессы ничем не отличаются от последней
стадии нуклеационного механизма
фазового распада. При этом рост объема
частиц пропорционален времени:
,
где q
– константа (Рис.5). На более глубоких
стадиях спинодального распада рост
амплитуды флуктуаций концентрации
замедляется, и начинает превалировать
процессы поглощения мелких доменов
более крупными вследствие выигрыша в
свободной поверхностной энергии. Эти
процессы ничем не отличаются от последней
стадии нуклеационного механизма
фазового распада. При этом рост объема
частиц пропорционален времени:
![]() ,
где d
и d0
– средний диаметр частиц во время t
и t0
соответственно, k
– константа скорости.. На предельных
стадиях фазового разделения аморфные
смеси в вязко-текучем состоянии стремятся
к расслоению, если предыдущая структура
не была кинетически стабилизирована
вследствие возрастания диффузионных
ограничений, в первую очередь при
стекловании одной или обоих фаз.
,
где d
и d0
– средний диаметр частиц во время t
и t0
соответственно, k
– константа скорости.. На предельных
стадиях фазового разделения аморфные
смеси в вязко-текучем состоянии стремятся
к расслоению, если предыдущая структура
не была кинетически стабилизирована
вследствие возрастания диффузионных
ограничений, в первую очередь при
стекловании одной или обоих фаз.

Рис.5. Изменение фазовой морфологии во время спинодального распада (с.) при фотополимеризации ЭГА, содержащем 80% ЖК
В) Блоксополимеры
Особое место среди конденсированных полимерных систем занимают блоксополимеры, к которым относится огромное число линейных, разветвленных и сетчатых полимеров, состоящих из двух или нескольких типов достаточно длинных полимерных цепей, химически связанных по концевым звеньям с образованием различной молекулярной топологии (архитектуры). Простейшим случаем являются линейные некристаллизующиеся и кристаллизующиеся бинарные диблоксополимеры типа АБ. С термодинамической точки зрения диблоксополимеры являются типичными бинарными полимерными смесями. При этом попарное соединение макромолекул двух типов, как и их смесь без химического связывания, мало влияет на их молекулярное (броуновское) тепловое движение и межмолекулярное взаимодействие (термодинамический параметр χ) и, следовательно, на их равновесное фазовое состояние. Однако, попарное соединение макромолекул двух типов резко изменяет возможности распределения компонентов в условиях фазового разделения.
Схематически расчетная диаграмма состояния диблок сополимера А-В в координатах χN (Т-1) – nА и типичные периодические структуры, проявляющиеся в различных ее областях, приведены на Рис. 6-7.

Рис.6. Схемы расчетных диаграмма состояния диблок сополимера А-В в координатах χN (Т-1) – nА и типичные периодические структуры, проявляющиеся в различных областях диаграммы

Рис. 7. Схема фазовой диаграммы симметричной смеси гомополимеров и формирования фазовой морфологии при разделении фаз в метастабильной области (зарождение, рост и слияние фаз) NG и в нестабильной области (спинодальный распад) SD
Основным процессом фазового разделения блоксополимеров является не макро-, а микрофазное разделение, или локальное сегрегирование блоков, протекающее по механизму нуклеации или спинодального распада с упорядоченным (периодическим) распределением микрофазных доменов. Положительный вклад энтальпии в свободную энергию в результате уменьшения числа контактов блоков А и В в процессе их локального сегрегирования компенсируется уменьшением энтропии системы в результате локализации узлов соединения блоков на границе раздела фаз и необходимого растяжения цепей от этой границы для обеспечения равномерной плотности их упаковки. Поэтому при повышенной температуре, когда превалирующую роль играет энтропийный фактор, локальное сегрегирование отсутствует. Более низкая температура, при которой энтальпийный фактор становится превалирующим, соответствует температуре упорядоченного микрофазного разделения, или перехода «беспорядок-порядок» c образованием так называемой суперкристаллической (супрамолекулярной) структуры с заданным размером и регулярным расположением структурных элементов (микрофаз в виде тонких пластин, или ламелей, сфер, цилиндров и др.) при неупорядоченной надмолекулярной структурой микрофаз. При этом формирование фазовой морфологии в решающей степени определяется произведением: χN, где N=NA+NB (χкрN=2) и относительной длиной блоков:nА=NA/(NA+NB:
χN<1 соответствует неупорядоченному состоянию и отсутствию локального сегрегирования блоков;
χN≈10 соответствует переходу «беспорядок-порядок» и проявлению сегрегирования блоков по механизму спинодального распада со сравнительно слабой движущей силой и формированием периодической микрофазной структуры;
χN>>10 соответствует сегрегированию блоков цепей с формированием периодической структуры с резко выраженной границей раздела между практически индивидуальными А и В доменами с вытянутыми конформациями цепей до RG~N2/3.
Одинаковая длина блоков обеспечивает образование ламелярных упорядоченных структур (суперкристаллов), а различная – преимущественно формироваие цилиндрических или сферических микрофаз, состоящих из более коротких блоков (миноргого компоента).
Направленное регулирование морфологии суперкристаллической структуры регулированием длины и природы блоков, а также совмещением блоксополимеров с различной длиной блоков, блоксополимеров с гомополимерами, диблоксополимера А-В с гетерофазной смесью гомополимеров А и В, триблоксопролимера АВС со сравнительно низкомолекулярным диблок сополимером ас и др. (Рис.6).

Рис.6. Схематическая модель (а) и ПЭМ микрофотография (в) взаимопроникающей спиралевидной морфологии диблоксополимера Полистирол/ Полиизобутилен после селективного вытравления УФ/озоном ПИ
Г) Механизм Киббла-Зурека
В настоящее время для описания динамики формирования структур в непрерывных (исходно гомогенных) средах любого масштаба в условиях, далеких от равновесия, широкое распространение находит обобщенная модель, называемая механизмом Киббла-Зурека (МКЗ). МКЗ описывает превращение гомогенной среды (скалярного поля) с большей симметрией (меньшей упорядоченностью) в среду с меньшей симметрией (с большей упорядоченной) в результате формирования структур (паттернов, ячеек или узоров), состоящих из коррелированных областей (доменов) и топологических дефектов, или фазовых сингулярностей (локальных состояний бифуркации) с еще меньшей симметрией, возникающих по границам коррелированных областей. Топологические дефекты, играющие определяющую роль в превращениях с изменением симметрии, являются результатом ограничений, накладываемых на эволюцию доменов окружающей средой. Физически это означает несогласование по фазе двух (или более) эквивалентных доменов и возникновение топологических дефектов в местах, где отсутствует фазовое согласование. Расстояния между топологическими дефектами дают, в среднем, размер (длину) коррелированных областей.
Киббл
использовал такие представления при
разработке космологической теории
формирования Галактик после Большого
взрыва, предположив, что образование
топологических дефектов (струн или
вихрей) определяет свойства Галактик.
Зурек распространил такой подход к
описанию динамики критических (непрерывных
фазовых) переходов, т.е. фазовых переходов
второго рода по определению Эренфеста,
в гомогенных конденсированных средах
для получения возможности проверки в
лабораторных условиях космологических
теорий. Применительно к непрерывным
фазовым превращениям в конденсированных
материальных системах МКЗ предполагает,
что определяющий (контрольный) параметр
порядка распространяется линейно с
заданной лимитирующей скоростью,
примерно равной для конденсированных
систем скорости звука. При охлаждении
до некоторой критической температуры
состояние системы изменяется адиабатически
и соответствует локальным равновесным
состояниям, которые определяются
мгновенным значением контрольного
параметра. При приближении к критической
температуре равновесная корреляционная
длина изменяется быстрее, чем лимитирующая
скорость и, соответственно, резко
изменяется время релаксации вследствие
замедления определяющих релаксационные
процессы мод (форм) движения. В критической
точке (Тс)
потенциальный барьер коррелированных
областей достигает или превышает энергию
теплового движения, процесс формирования
узора, т.е. динамика системы, «замораживается»,
размеры доменов и распределение дефектов
стабилизируются, а корреляционная длина
достигает предельного значения. Таким
образом, критическая температура
лимитирует размеры корреляционных
областей (доменов) ξ.
Она соответствует температуре Гинзбурга
(TG),
при которой энергия теплового движения
сопоставима со свободной энергией
коррелированных областей
![]() :
:![]() (97).
(97).
В
случаях больших градиентов температуры
или высоких скоростей ее изменения при
охлаждении, в том числе при переохлаждении
метастабильных жидкостей, МКЗ предполагает
универсальные степенные соотношения
(скейлинг) для зависимостей корреляционной
длины параметра порядка (ξ)
и времени релаксации (τ)
от скорости (характерного времени)
охлаждения, причем критические показатели
степени (экспоненты) в этих законах
зависят только от типа модели (размерности
пространства, топологии и характера
диссипативных процессов в системе):
![]() (98),
где
(98),
где
![]() ,
Тс
–
критическая температура, ν
и μ
- критические экспоненты. В простейшем
случае среднего поля, в предположении,
что взаимодействие любой молекулы с
окружающими молекулами описывается их
средним полем, ν=1/2,
μ=1.
Характерное время охлаждения τq
связано c
ε,
т.е. с удаленностью от Тс,
и со скоростью охлаждения (dT/dt)
примерными соотношениями: τq=t/ε
и
,
Тс
–
критическая температура, ν
и μ
- критические экспоненты. В простейшем
случае среднего поля, в предположении,
что взаимодействие любой молекулы с
окружающими молекулами описывается их
средним полем, ν=1/2,
μ=1.
Характерное время охлаждения τq
связано c
ε,
т.е. с удаленностью от Тс,
и со скоростью охлаждения (dT/dt)
примерными соотношениями: τq=t/ε
и
![]() (99),
где
t
– текущее время. В момент времени t*
система стабилизируется («замораживается»)
при приближении к температуре Гинзбурга,
и в соответствие с МКЗ предельно
достигаемый размер коррелированных
областей (доменов) зависит только от
скорости охлаждения (характерного
времени закалки) τq
в соответствие со скейлинговым
соотношением:
(99),
где
t
– текущее время. В момент времени t*
система стабилизируется («замораживается»)
при приближении к температуре Гинзбурга,
и в соответствие с МКЗ предельно
достигаемый размер коррелированных
областей (доменов) зависит только от
скорости охлаждения (характерного
времени закалки) τq
в соответствие со скейлинговым
соотношением:
![]() (100).
В случае среднего поля критическая
экспонента σ=1/4.
(100).
В случае среднего поля критическая
экспонента σ=1/4.
