
- •2. Как влияет температура на различные виды поляризации ( электронную, атомную, ориентационную).
- •28.Что называется термодинамическими параметрами системы. Приведите примеры интенсивных и экстенсивных параметров состояния.
- •39. Стандартное состояние вещества. Стандартная энтальпия химической реакции.
- •Первый закон Коновалова
- •92.У одного из двух водных 0,005 м растворов – раствора глюкозы или раствора сульфата натрия – осмотическое давление (при одинаковой температуре ) больше. Почему
- •130.Роль свободных радикалов в химической кинетике. Механизм возникновения свободных радикалов.
- •Образование
- •20. Используя данные таблицы 3 вычислить величину электричеcкого дипольного момента молекулы вещества .
- •125.При 40 с давление пара хлороформа равно 49 198 Па, а при температуре 50 с 71 330 Па. Вычислить энтальпию испарения , температуру кипения и энтропию испарения при температуре испарения.
- •178. Вычислить энергии активации химических реакций по данным о константах скоростей k при разных температурах t
- •Для большинства реакции зависимость скорости реакции и константы скорости реакции зависит от температуры и выражается экспоненциальной зависимостью
- •Список литературы
2. Как влияет температура на различные виды поляризации ( электронную, атомную, ориентационную).
Поляризуемость атомов, ионов и молекул, способность этих частиц приобретать дипольный момент р в электрическом поле Е. Появление р обусловлено смещением электрических зарядов в атомных системах под действием поля Е; такой индуцированный момент р исчезает при выключении поля Различают несколько видов Поляризуемость Электронная Поляризуемость обусловлена смещением в поле Е электронных оболочек относительно атомных ядер; ионная Поляризуемость (в ионных кристаллах) — смещением в противоположных направлениях разноимённых ионов из положения равновесия; атомная Поляризуемость обусловлена смещением в поле Е атомов разного типа в молекуле (она связана с несимметричным распределением в молекуле электронной плотности). Температурная зависимость этих видов Поляризуемость слабая: с ростом температуры. Поляризуемость несколько уменьшается Поляризуемость диэлектрика включает составляющие – электронную, ионную и ориентационную (дипольную). Рис.1. иллюстрирует механизм этих видов поляризуемости.
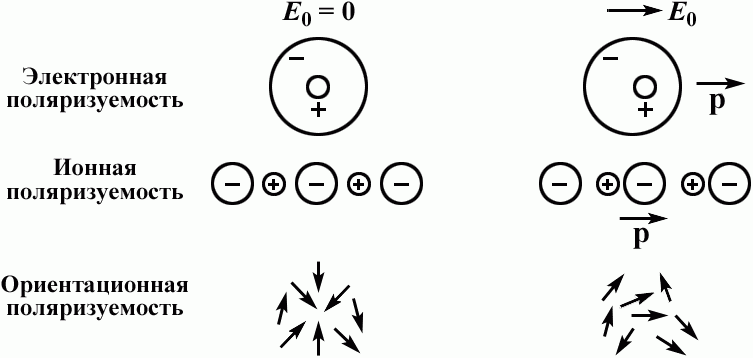
Рис. 1
Электронная поляризуемость обусловлена смещением электронной оболочки атома относительно ядра. Ионная поляризуемость вызвана смещением заряженных ионов по отношению к другим ионам. Ориентационная (дипольная) поляризуемость возникает, когда вещество состоит из молекул, обладающих постоянными электрическими дипольными моментами, которые могут более или менее свободно изменять свою ориентацию во внешнем электрическом поле. В физике твёрдых и жидких диэлектриков под поляризуемость понимают среднюю Поляризуемость (поляризацию Р, рассчитанную на 1 частицу и приходящуюся на единицу поля: a = P/EN, где N — число частиц). Поляризуемость полярных диэлектриков называется ориентационной. Поляризация диэлектриков при скачкообразных переходах его частиц из одного возможного состояния в другое под действием поля Е можно описывать, вводя релаксационную поляризуемость Характерной особенностью этих видов поляризуемость является их резкая зависимость от температуры.
28.Что называется термодинамическими параметрами системы. Приведите примеры интенсивных и экстенсивных параметров состояния.
Термодинамической системой называется совокупность материальных тел, взаимодействующих, как между собой, так и с окружающей средой. Поскольку одно и тоже тело, одно и тоже вещество при разных условиях может находится в разных состояниях, (пример: лед – вода – пар , одно вещество при разной температуре) вводятся, для удобства, характеристики состояния вещества – так называемые параметры состояния. Параметры состояния, термодинамические параметры — физические величины, характеризующие состояние термодинамической системы: температура, давление, удельный объём, намагниченность, электрическая поляризация и др.
Перечислим основные параметры состояния вещества:
Температура тел - определяет направление возможного самопроизвольного перехода тепла между телами. Температура, выраженная по абсолютной шкале, называется абсолютной температурой.
Соотношение для перехода от градусов Цельсия к градусам Кельвина:
T [K] = t [°C] + 273.15
где: T - температура в Кельвинах, t – температура в градусах Цельсия.
Давление - представляет собой силу, действующею по нормали к поверхности тела и отнесенную к единице площади этой поверхности. Для измерения давления применяются различные единицы измерения. В стандартной системе измерения СИ единицей служит Паскаль (Па).
Соотношение между единицами:
1 бар = 105 Па
1 кг/см2 (атмосфера) = 9.8067×104 Па
1мм рт. ст (миллиметр ртутного столба) = 133 Па
1 мм вод. ст. (миллиметр водного столба) = 9.8067 Па
Плотность – отношение массы вещества к объему занимаемому эти веществом.
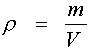
Удельный объем - величина обратная плотности т.е. отношения объема занятого веществом к его массе.
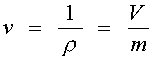 (обратно
к содержанию)
(обратно
к содержанию)
Различают экстенсивные параметры состояния, пропорциональные массе системы:
-
объём,
-
внутренняя энергия,
-
энтропия,
-
энтальпия,
-
энергия Гиббса,
-
энергия Гельмгольца (свободная энергия),
и интенсивные параметры состояния, не зависящие от массы системы:
-
давление,
-
температура,
-
концентрация,
-
магнитная индукция и др.
