
- •26. Реальные растворы. Метод активностей. Определение активности по давлению пара.
- •Методы определения активности
- •По равновесному давлению пара
- •По равновесию химической реакции с газовой фазой
- •По значению э. Д. С. Гальванического элемента
- •27. Коллигативные свойства растворов неэлектролитов. Зависимость химического потенциала растворителя от температуры и мольной доли.
- •28. Понижение температуры плавления (замерзания) и повышение температуры кипения растворов.
- •29. Осмотическое давление. Уравнение Вант-Гоффа.
- •30. Коллигативные свойства растворов электролитов. Изотонический коэффициент.
- •31. Условие химического равновесия. Термодинамический вывод закона действующих масс.
- •32. Изотерма химической реакции Вант-Гоффа.
- •33. Различные константы равновесия и связь между ними. Химическое равновесие в идеальных и реальных системах.
- •34. Зависимость константы равновесия от температуры. Уравнение изобары (изохоры) Вант-Гоффа в дифференциальной и интегральной форме. Принцип Ле Шателье.
- •35. Движение ионов в растворе. Удельная и эквивалентная электропроводность. Электропроводность растворов электролитов
- •36. Закон Кольрауша для растворов сильных электролитов. Зависимость эквивалентной электропроводности от концентрации. Подвижность ионов. Числа переноса.
- •37. Теория Аррениуса для слабых электролитов. Закон разведения Оствальда.
- •38. Активность иона. Средний ионный коэффициент активности. Теория Дебая-Хюккеля. Активность электролитов
- •39. Электродный потенциал. Электродвижущая сила (эдс).
- •40. Основные типы электродов и гальванических элементов.
- •Типы гальванических элементов
- •41. Зависимость электродного потенциала от концентрации (активности). Уравнение Нернста.
- •42. Определение термодинамических функций методом эдс.
- •43. Скорость химической реакции. Основной постулат химической кинетики (закон действующих масс).
- •44. Порядок и молекулярность реакции. Методы определения порядка и константы скорости реакции.
- •45. Простые и сложные химические реакции. Кинетические уравнения простых реакций нулевого, первого и второго порядков. Кинетика сложных реакций
- •Реакция нулевого порядка
- •Реакция первого порядка
- •Реакция второго порядка
- •47. Сложные реакции и их классификация. Анализ кинетических кривых последовательных реакций первого порядка. Кинетика сложных реакций
- •48. Обратимые реакции как частный случай последовательных реакций. Кинетическое уравнение обратимой реакции первого порядка.
- •49. Параллельные (конкурирующие) реакции первого порядка. Анализ кинетических кривых для двух параллельных реакций первого порядка.
26
26. Реальные растворы. Метод активностей. Определение активности по давлению пара.
Реальными называются р-ры, кот. не подчиняются законам ид. р-ров. Обычно они составлены из компонентов с различными св-вами, строением молекул и силами взаимодействия между молекулами компонентов. Образование таких р-ров сопровождается изменением объема и тепловыми эффектами. С уменьшением концентрации реального раствора его свойства приближаются к свойствам идеального раствора.
Методы определения активности
Экспериментальные методы определения активности компонентов в растворе основаны на изучении какого-либо гетерогенного равновесия в системе. При рассмотрении этих методов следует помнить, что в условиях равновесия химические потенциалы i-го компонента в разных фазах (I и II) равны:
![]()
Это соотношение является исходной точкой для вывода расчетных уравнений в некоторых из методов определения активности. Кроме того, активности компонентов в некоторой фазе связаны между собой уравнением:
![]()
По равновесному давлению пара
В основе этого метода лежит соотношение:
![]()
где
![]() —
парциальное давление пара компонента
над раствором, а
—
парциальное давление пара компонента
над раствором, а
![]() —
давление пара этого компонента для
стандартного состояния (см. выше).
Соответственно, если за стандартное
состояние принято состояние чистого
компонента, то
—
давление пара этого компонента для
стандартного состояния (см. выше).
Соответственно, если за стандартное
состояние принято состояние чистого
компонента, то
![]() .
.
Эксериментальные методы определения давления пара компонентов над раствором весьма разнообразны; выбор того или иного из них определяется, в частности, исследуемой системой (водный раствор или иная низкотемпературная система, либо расплавленный металл, шлак, штейн и т. п.).
По повышению температуры кипения раствора
Т
кипения
раствора
![]() выше
Т кипения чистого р-ля
выше
Т кипения чистого р-ля
![]() .
Данные об изменении Т кипения р-ра могут
быть использованы для расчета активности
р-ля,
в соответствии с ур-ем:
.
Данные об изменении Т кипения р-ра могут
быть использованы для расчета активности
р-ля,
в соответствии с ур-ем:
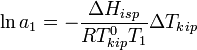 ,
,
где
![]() —
теплота испарения р-ля, в интервале от
Т кипения чистого р-ля до Т кипения р-ра
принимаемая постоянной. Индексом «1»
обычно обозначается р-ль.
—
теплота испарения р-ля, в интервале от
Т кипения чистого р-ля до Т кипения р-ра
принимаемая постоянной. Индексом «1»
обычно обозначается р-ль.
По понижению температуры замерзания раствора
Т
замерзания
р-ра
![]() ниже
Т замерзания чистого растворителя
ниже
Т замерзания чистого растворителя
![]() .
Соответственно, активность р-ля
можно рассчитать, используя зависимость:
.
Соответственно, активность р-ля
можно рассчитать, используя зависимость:
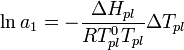 ,
,
где
![]() —
теплота плавления р-ля.
—
теплота плавления р-ля.
По осмотическому давлению раствора
Величина осмотического давления раствора может быть использована для определения активности растворителя в соответствии с соотношением:
![]()
где
![]() —
осмотическое давление,
—
осмотическое давление,
![]() —
парциальный молярный объём р-ля.
—
парциальный молярный объём р-ля.
По распределению компонента между конденсированными фазами
Активность компонента раствора можно определить, изучая равновесное распределение его между двумя контактирующими конденсированными фазами (различными растворителями, сплавом и шлаком, шлаком и штейном и т. п.), одна из которых — исследуемый раствор, а для другой активность или коэфф. активности уже известны. В общем случае:
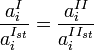
В
частности, если выбор стандартного
состояния компонента для фаз таков, что
![]() ,
это выражение принимает более простой
вид:
,
это выражение принимает более простой
вид:
![]()
Экспериментально в этом методе определяют равновесные концентрации компонента или коэффициент распределения компонента между р-рами.
По равновесию химической реакции с газовой фазой
При исслед. оксидных р-вов активность компонентов часто определяют, использ. следующие хим. р-ции:
MeO + H2 = Me + H2O
MeO + CO = Me + CO2
Для первой из приведенных реакций константа равновесия имеет вид:
![]()
Если
оксидный и металлический расплавы
взаимно нерастворимы и восстанавливается
индивидуальный оксид, то
![]() ,
и тогда:
,
и тогда:
![]()
Если металл выделяется в виде сплава с другими компонентами или растворяется в фазе-коллекторе, его активность не равна единице и формула принимает вид:
![]()
Активность металла в сплаве здесь должна быть известна из независимых измерений.
Опытным
путем в данном методе определяют
отношение
![]() .
.
Кроме того, активность оксидного компонента связана с равновесным давлением кислорода над расплавом, с учетом реакций в газовой фазе, например:
![]()
или
![]()
Тогда
можно показать, что

Для сульфидных расплавов используют реакцию:
![]()
или (значительно реже):
![]()
