
- •26. Реальные растворы. Метод активностей. Определение активности по давлению пара.
- •Методы определения активности
- •По равновесному давлению пара
- •По равновесию химической реакции с газовой фазой
- •По значению э. Д. С. Гальванического элемента
- •27. Коллигативные свойства растворов неэлектролитов. Зависимость химического потенциала растворителя от температуры и мольной доли.
- •28. Понижение температуры плавления (замерзания) и повышение температуры кипения растворов.
- •29. Осмотическое давление. Уравнение Вант-Гоффа.
- •30. Коллигативные свойства растворов электролитов. Изотонический коэффициент.
- •31. Условие химического равновесия. Термодинамический вывод закона действующих масс.
- •32. Изотерма химической реакции Вант-Гоффа.
- •33. Различные константы равновесия и связь между ними. Химическое равновесие в идеальных и реальных системах.
- •34. Зависимость константы равновесия от температуры. Уравнение изобары (изохоры) Вант-Гоффа в дифференциальной и интегральной форме. Принцип Ле Шателье.
- •35. Движение ионов в растворе. Удельная и эквивалентная электропроводность. Электропроводность растворов электролитов
- •36. Закон Кольрауша для растворов сильных электролитов. Зависимость эквивалентной электропроводности от концентрации. Подвижность ионов. Числа переноса.
- •37. Теория Аррениуса для слабых электролитов. Закон разведения Оствальда.
- •38. Активность иона. Средний ионный коэффициент активности. Теория Дебая-Хюккеля. Активность электролитов
- •39. Электродный потенциал. Электродвижущая сила (эдс).
- •40. Основные типы электродов и гальванических элементов.
- •Типы гальванических элементов
- •41. Зависимость электродного потенциала от концентрации (активности). Уравнение Нернста.
- •42. Определение термодинамических функций методом эдс.
- •43. Скорость химической реакции. Основной постулат химической кинетики (закон действующих масс).
- •44. Порядок и молекулярность реакции. Методы определения порядка и константы скорости реакции.
- •45. Простые и сложные химические реакции. Кинетические уравнения простых реакций нулевого, первого и второго порядков. Кинетика сложных реакций
- •Реакция нулевого порядка
- •Реакция первого порядка
- •Реакция второго порядка
- •47. Сложные реакции и их классификация. Анализ кинетических кривых последовательных реакций первого порядка. Кинетика сложных реакций
- •48. Обратимые реакции как частный случай последовательных реакций. Кинетическое уравнение обратимой реакции первого порядка.
- •49. Параллельные (конкурирующие) реакции первого порядка. Анализ кинетических кривых для двух параллельных реакций первого порядка.
32. Изотерма химической реакции Вант-Гоффа.
Изменение rG или rF в химической реакции при заданных (не обязательно равновесных) парциальных давлениях Pi или концентрациях Ci компонентов можно рассчитать по уравнению изотермы химической реакции (изотермы Вант-Гоффа):
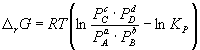 .
.
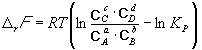 .
.
33
33. Различные константы равновесия и связь между ними. Химическое равновесие в идеальных и реальных системах.
Химическим равновесием называется такое состояние обратимой химической реакции
aA + bB = cC + dD,
при котором с течением времени не происходит изменения концентраций реагирующих веществ в реакционной смеси. Состояние химического равновесия характеризуется константой химического равновесия:
,
где Ci – концентрации компонентов в равновесной идеальной смеси.
Константа равновесия может быть выражена также через равновесные мольные доли Xi компонентов:
.
Для реакций, протекающих в газовой фазе, константу равновесия удобно выражать через равновесные парциальные давления Pi компонентов:
.
Для идеальных газов Pi = CiRT и Pi = XiP, где P – общее давление, поэтому KP, KC и KX связаны следующим соотношением:
KP = KC (RT) c+d–a–b = KXP c+d–a–b.
Константа равновесия связана с rGo химической реакции:
![]()
В случае идеальных р-ров вместо активностей компонентов используют их молярные доли xi.

где k1 и k-1 - константы скорости прямой и обратной р-ций.
34
34. Зависимость константы равновесия от температуры. Уравнение изобары (изохоры) Вант-Гоффа в дифференциальной и интегральной форме. Принцип Ле Шателье.
Согласно принципу Ле Шателье, если на систему, находящуюся в равновесии, оказать внешнее воздействие, то равновесие сместится так, чтобы уменьшить эффект внешнего воздействия. Так, повышение давления сдвигает равновесие в сторону уменьшения количества молекул газа. Добавление в равновесную смесь какого-либо компонента реакции сдвигает равновесие в сторону уменьшения количества этого компонента. Повышение (или понижение) температуры сдвигает равновесие в сторону реакции, протекающей с поглощением (выделением) теплоты.
Количественно зависимость константы равновесия от температуры описывается уравнением изобары химической реакции (изобары Вант-Гоффа)
![]()
и изохоры химической реакции (изохоры Вант-Гоффа)
![]() .
.
Интегрирование уравнения в предположении, что rH реакции не зависит от температуры (что справедливо в узких интервалах температур), дает:
![]()
![]()
где C – константа интегрирования. Таким образом, зависимость ln KP от 1/Т должна быть линейной, а наклон прямой равен – rH /R.
Интегрирование в пределах K1, K2, и T1, T2 дает:
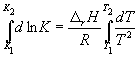

По этому уравнению, зная константы равновесия при двух разных температурах, можно рассчитать rH реакции. Соответственно, зная rH реакции и константу равновесия при одной температуре, можно рассчитать константу равновесия при другой температуре.
35
35. Движение ионов в растворе. Удельная и эквивалентная электропроводность. Электропроводность растворов электролитов
Электропроводность ("Каппа") раствора - величина, обратная его сопротивлению R, имеет размерность Ом-1. Для проводника постоянного сечения
![]() ,
,
где - удельное сопротивление; S - площадь сечения проводника; l - длина проводника; - удельная электропроводность.
Удельной электропроводностью ("каппа") раствора называется электропроводность слоя раствора длиной 1 см, заключенного между электродами площадью 1см2. Она выражается в Ом-1. см-1. В системе СИ удельная электропроводность измеряется в Ом-1. м-1.
Эквивалентной электропроводностью ("лямбда") называется электропроводность такого объема раствора, в котором содержится 1 г-экв растворенного вещества; при условии, что электроды находятся на расстоянии 1 см друг от друга, она выражается в Ом-1. см2. г-экв-1.
![]() ,
,
где V = 1/C - разведение (или разбавление) раствора, т.е. объем, в котором содержится 1 г-экв растворенного вещества, а C - эквивалентная концентрация (нормальность) раствора. В системе СИ эквивалентная электропроводность выражается в Ом-1. м2. кг-кв-1.
Эквивалентная электропроводность растворов электролитов возрастает с ростом разбавления раствора и при бесконечном разбавлении (т.е. при бесконечно малой концентрации) достигает предельного значения 0. которое называется эквивалентной электропроводностью раствора при бесконечном разведении.
В разбавленных растворах сильных электролитов выполняется эмпирический закон Кольрауша (закон квадратного корня):
![]() ,
,
где и 0 - эквивалентная электропроводность раствора при концентрации С и при бесконечном разведении, A - константа (при данной температуре) для данного электролита и растворителя.
В растворах слабых электролитов и 0 связаны со степенью диссоциации электролита уравнением Аррениуса:
![]() .
.
Кроме того, выполняется закон разведения Оствальда, который для бинарного электролита записывается следующим образом:
![]() ,
,
где K - константа диссоциации слабого электролита.
Электропроводность электролитов связана со скоростями движения ионов в р-ре. Скорость движения vi [м.с-1] иона в р-ре пропорциональна напряженности приложенного электрического поля E [В.м-1]:
vi = uiE.
Коэфф. пропорциональности u [м2. с-1. В-1] называется абсолютной подвижностью иона.
Произведение uiF (F - постоянная Фарадея) называется подвижностью иона i[Ом-1. м2. кг-экв-1]:
i = uiF.
Подвижность иона при бесконечном разбавлении называется предельной подвижностью иона и обозначается i0. Предельные подвижности i0 некоторых ионов в водном растворе [Ом-1. см2. г-экв-1] приведены в Таблице 10.1.
Согласно закону Кольрауша о независимой миграции ионов, эквивалентная электропроводность раствора при бесконечном разведении равна сумме предельных подвижностей катионов и анионов:
0 = 0+ + 0-.
Доля тока, переносимая данным ионом, называется числом переноса ti иона:
![]() ,
,
причем
по определению
![]() .
.
Согласно закону Стокса, предельная подвижность 0 иона с зарядом z и радиусом r в растворителе с вязкостью h описывается формулой:
![]() ,
,
где e - элементарный заряд, F - постоянная Фарадея.
Из этого уравнения следует правило Вальдена-Писаржевского, согласно которому для любого иона или электролита:
![]() .
.
36
